3.01-3.10
3.01
僥僉僗僩pp72-73乮傑偨偼屻傠尒奐偒乯偺丄姱擻婎偺峔憿傪帵偟偨昞傪嶲徠偡傞偙偲丅 偨偩偟丄乽姱擻婎柤乿偲丄乽偦偺姱擻婎傪帩偮壔崌暔偺堦斒柤乿傪崿摨偟側偄偙偲丅
嫵壢彂壓姫丄姫枛晅榐偺椺夝偱偼丄姱擻婎柤傪帵偝偢偵丄偦偺姱擻婎傪帩偮壔崌暔偺堦斒柤乮働僩儞丄僄僗僥儖丄傾儖僐乕儖側偳乯傪梌偊偰偍傝丄乽姱擻婎傪帵偣乿偲偺栤偄偵懳偟偰昁偢偟傕揔愗偱側偄偲敾抐偱偒傞晹暘傕偁傞丅拲堄偝傟偨偟丅
儊僠僆僯儞 偺俁師尦柾宆
僀僽僾儘僼僃儞 偺俁師尦柾宆
僇僾僒僀僔儞 偺俁師尦柾宆
乮夝摎椺乯
姱擻婎乮偦偺姱擻婎傪傕偮堦斒柤乯偺弴偱帵偡丅
(a) methionine, (IUPAC柤丗2-amino-4-(methylsulfanyl)butanoic acid)
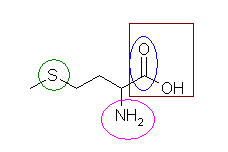
椢娵丗僗儖僼傿僪寢崌乮僗儖僼傿僪乯丅抁偄傎偆偺傾儖僉儖婎偱偁傞儊僠儖婎傕娷傔偨師偺晹暘丄CH3-S- 偼丄儊僠儖僠僆婎丄傑偨偼儊僠儖僗儖僼傽僯儖婎偲偄偆偙偲偑偱偒傞丅乮敪揥偺崁傪嶲徠乯
僺儞僋娵丗傾儈僲婎乮傾儈儞乯
拑巐妏丗僇儖儃僉僔婎乮僇儖儃儞巁乯
惵娵丗僇儖儃僯儖婎丄晅偗崻偺扽慺傪彍偄偰 =O 偺傒偱尵偆応崌偼丄僆僉僜婎丅偙偺僇儖儃僯儖婎偼僇儖儃僉僔婎偺堦晹側偺偱傢偞傢偞巜揈偡傞昁梫偼柍偄丅
(b) ibuprofen, (IUPAC柤丗2-(4-isobutylphenyl)propanoic acid)
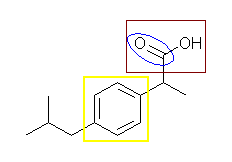
墿巐妏丗朏崄娐乮朏崄懓壔崌暔丄傾儗乕儞乯
拑巐妏丗僇儖儃僉僔婎乮僇儖儃儞巁乯
惵娵丗僇儖儃僯儖婎丄晅偗崻偺扽慺傪彍偄偰 =O 偺傒偱尵偆応崌偼丄僆僉僜婎丅偙偺僇儖儃僯儖婎偼僇儖儃僉僔婎偺堦晹側偺偱傢偞傢偞巜揈偡傞昁梫偼柍偄丅
(c) capsaicin, (IUPAC柤丗N-(4-hydroxy-3-methoxybenzyl)-8-methylnon-6-enamide)
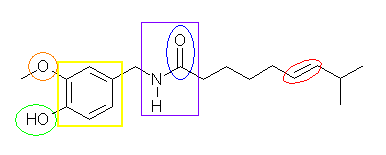
烌娵丗僄乕僥儖寢崌乮僄乕僥儖乯丅抁偄傎偆偺傾儖僉儖婎偱偁傞儊僠儖婎傕娷傔偨師偺晹暘丄CH3-O- 偼丄儊僠儖僆僉僔婎丄傑偨偼儊僩僉僔婎偲偄偆偙偲傕偱偒傞丅
墿椢娵丗悈巁婎丄傑偨偼丄僸僪儘僉僔婎乮僼僃僲乕儖乯丅悈巁婎偑傾儖僇儞偵寢崌偟偰偄傞応崌偼傾儖僐乕儖偩偑丄朏崄娐偵寢崌偟偰偄傞応崌偼僼僃僲乕儖偱偁傞丅乮嫹媊偱偼丄儀儞僛儞娐忋偵悈巁婎傪傕偮 C6H5-OH 偑僼僃僲乕儖乮壔崌暔偺柤徧乯偱偁傞偑丄峀媊偱偼丄朏崄娐忋偵悈巁婎傪傕偮 Ar-OH 傕堦斒偵僼僃僲乕儖乮壔崌暔孮偺柤徧乯偲憤徧偡傞偙偲偑偁傞丅嬫暿偺偨傔丄屻幰傪僼僃僲乕儖椶偲偄偆尵偄曽傪偡傞恖傕偄傞丅乯
墿巐妏丗朏崄娐乮朏崄懓壔崌暔丄傾儗乕儞乯
巼巐妏丗傾儈僪寢崌乮巁傾儈僪乯
惵娵丗僇儖儃僯儖婎丄晅偗崻偺扽慺傪彍偄偰 =O 偺傒偱尵偆応崌偼丄僆僉僜婎丅偙偺僇儖儃僯儖婎偼僇儖儃僉僔婎偺堦晹側偺偱丄傢偞傢偞姱擻婎偲偟偰庢傝忋偘傞昁梫偼柍偄丅
愒娵丗擇廳寢崌乮傾儖働儞乯
乮敪揥乯
棸墿偺扨妀悈慺壔崌暔丄SH2 傪乽僗儖僼傽儞丄sulfane乿偲偟偰桿摫偡傞偲丄儊僠儖僠僆婎 CH3-S- 偼丄儊僠儖僗儖僼傽僯儖婎偱偁傞偲偄偆尵偄曽偵側傞丅
IUPAC 1979 偱偼丄傾儖僉儖僠僆婎偲偄偆尵偄曽偑丄IUPAC 1993 偱偼 傾儖僉儖僗儖僼傽僯儖婎偲偄偆尵偄曽傪悇彠偟偰偄傞偲偺偙偲丅
嶲峫丗乮奜晹儕儞僋乯乽壔崌暔柦柤朄択媊乮儊僯儏乕乯乿傛傝丄乽僇儖僐僎儞偺抲姺婎乿
http://homepage1.nifty.com/nomenclator/text/chalco.htm
乮敪揥俀乯
僇儖儃僉僔婎偲僇儖儃僉僔儖婎
僇儖儃儞巁傪梌偊傞傛偆側姱擻婎 -CO2H 傪丄僇儖儃僉僔婎偲偄偆丅尰嵼丄僂僃僽忋傗丄嫵壢彂摍偵偍偄偰偼丄僇儖儃僉僔儖婎偲昞婰偝傟傞偙偲傕偁傝傑偡偑丄IUPAC偺1993擭姪崘偱丄僇儖儃僉僔儖婎偲偄偆昞尰偼攑巭偝傟偨偦偆偱偡丅廬偭偰丄奆偝傫偼乽僇儖儃僉僔婎乿偲偄偆昞婰偑惓偟偄乮傑偨偼丄岲傑偟偄乯偲偄偆擣幆傪帩偭偰偄偰偔偩偝偄丅乮偨偲偊偽乽but-2-ene乿昞婰偡傞偙偲偑悇彠偝傟偰偄傞壔崌暔偵偮偄偰丄傑偩 乽2-butene乿偲偄偆昞婰偑懡乆尒傜傟傞傛偆側傕偺偱偡丅僇儖儃僉僔儖婎偑娫堘偄偲傑偱偼尵偊側偄偲偙傠偱偟傚偆丅乯
傑偨丄偙傟偼丄悈巁婎乮僸僪儘僉僔婎乯偵偮偄偰傕摨條偱偡丅埲慜偼丄僸僪儘僉僔儖婎偲偄偆昞婰傪偟偰偄傑偟偨偑丄IUPAC偺1993擭姪崘偱丄僸僪儘僉僔儖婎偲偄偆昞尰偼攑巭偲側偭偰偄傑偡丅
3.02
乮岆乯偮偓偺姱擻婎傪傕偮娙扨側暘巕傪帵偣丅
乮惓乯偮偓偺姱擻婎傗堦斒柤傪傕偮娙扨側暘巕傪帵偣丅
偨偲偊偽 (a) 傾儖僐乕儖偼丄姱擻婎偺柤徧偱偼側偄丅
側偍丄乽暘巕傪帵偣乿偲偄偆栤偄偵懳偟偰丄彮側偔偲傕丄乽峔憿幃乮傑偨偼丄帵惈幃乯乿偲乽柤徧乿傪摎偊傞傋偒丅
僥僉僗僩pp72-73乮傑偨偼屻傠尒奐偒乯偺丄姱擻婎偺峔憿傪帵偟偨昞傪嶲徠偡傞偙偲丅
乮夝摎椺乯
帵偝傟偨姱擻婎傪帩偮傛偆側暘巕偵偼丄偝傑偞傑側傕偺偑偁傞丅偙偙偱偼丄偦偺拞偺悢椺偺傒傪帵偡丅
(a) CH3OH乮儊僞僲乕儖乯
懠偵僄僞僲乕儖丄僾儘僷僲乕儖側偳傕壜丅
(b) 壓恾乮嵍偼儀儞僛儞丄塃偼僫僼僞儗儞乯
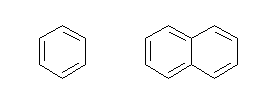
(c) CH3CO2H乮僄僞儞巁乮姷梡柤丗恷巁乯乯
懠偵傕儊僞儞巁乮姷梡柤丗僊巁乯丄僾儘僷儞巁側偳傕壜丅
(d) CH3NH2乮儊僠儖傾儈儞乯丄(CH3)NH
2乮僕儊僠儖傾儈儞乯
(e) CH3COCH2NH2乮1-傾儈僲-2-僾儘僷僲儞乯丗壓恾嵍丅
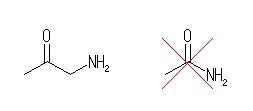
乽働僩儞乿偱偁傞偨傔偵偼丄僇儖儃僯儖婎偵俀偮偺傾儖僉儖婎偑寢崌偟偰偄側偗傟偽側傜側偄丅恾塃偺 CH3CONH2乮僄僞儞傾儈僪乮姷梡柤丗傾僙僩傾儈僪乯乯偼丄1-傾儈僲-2-僾儘僷僲儞傛傝傕峏偵扨弮側峔憿偱偁傞偑丄僇儖儃僯儖婎乮C=O乯偵寢崌偟偰偄傞堦曽偑傾儖僉儖婎偱偼側偄偺偱丄働僩儞偱偼側偄丅
傑偨乽傾儈儞乿偱偁傞偨傔偵偼丄拏慺忋偺俁偮偺抲姺婎偑丄悈慺傑偨偼傾儖僉儖婎偱偁傞昁梫偑偁傞丅恾塃偺僄僞儞傾儈僪偱偼丄拏慺偵寢崌偟偰偄傞偺偑傾儖僉儖婎偱偼側偄偺偱丄傾儈儞偱傕側偄丅乮傾儖僉儖婎偑侾偮寢崌偟偨僇儖儃僯儖婎丄RC(=O)-偼丄傑偲傔偰傾僔儖婎偲屇偽傟傞丅乯
(f) CH2=CH-CH=CH2乮1,3-僽僞僕僄儞乯丗
壓恾塃乮1,3-僔僋儘僿僉僒僕僄儞乯傗丄CH2=C=CH2乮1,2-僾儘僷僕僄儞乯側偳偱傕椙偄丅
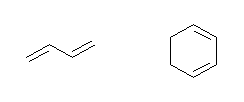
拲堄丗乽姱擻婎乿偲偟偰偺乽擇廳寢崌乿偑巜偡偺偼丄堦斒揑偵扽慺扽慺偺娫偺擇廳寢崌偵尷掕偝傟傞丅偟偨偑偭偰丄擇巁壔扽慺 O=C=O 偺條側椺偼丄晄惓夝偲偡傞丅傑偨丄儀儞僛儞 C6H6 傕俁偮偺扽慺扽慺擇廳寢崌傪帩偮偑丄朏崄娐偺拞偺擇廳寢崌偼丄屄暿偺扽慺扽慺擇廳寢崌偲偼堎側傞嫇摦傪帵偡偨傔偵乽朏崄懓壔崌暔乿偼乽傾儖働儞乿偲偼暿偺堦孮偵暘椶偝傟偰偄傞丅偦偺偨傔丄偙偺栤偄偺摎偊偲偟偰儀儞僛儞傪帵偡偙偲偼丄偁傑傝椙偄椺偲偼偄偊側偄丅
乮敪揥乯
傾儈儞椶偺柦柤傕偦偆偲偆傗傗偙偟偄丅CH3NH2 偼丄methylazane, methanamine, methylamine 偺偄偢傟傕惓偟偄丅(CH3)NH
2 偼丄dimethylazane, dimethylamine 側偳偲側傞丅
嶲峫丗乮奜晹儕儞僋乯乽壔崌暔柦柤朄択媊乮儊僯儏乕乯乿傛傝丄乽傾儈儞偲僀儈儞乿
http://homepage1.nifty.com/nomenclator/text/amine.htm
3.03
昤夋忋丄堿偵側偭偰偄傞悈慺傪尒棊偲偝側偄傛偆偵偟側偑傜丄傑偢偼峔憿幃傪彂偄偰傒偰偔偩偝偄丅埲壓偺俁師尦柾宆傕嶲徠偟側偑傜丄奺曽岦偐傜挱傔偰傒偰丄峔憿幃偵娫堘偄側偄偙偲傪妋擣偟偰偔偩偝偄丅
側偍丄偙偙偱忋偘傞傋偒姱擻婎偼俁偮丅
傾儗僐儕儞 偺俁師尦柾宆
乮夝摎椺乯
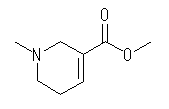
峔憿幃偼忋恾丅暘巕幃偼丄C8H13NO2 偲側傞丅
傾儗僐儕儞 arecoline 偵娷傑傟傞俁偮偺姱擻婎傪師偵帵偡丅
乮俁媺偺乯傾儈僲婎
擇廳寢崌
僄僗僥儖寢崌乮傑偨偼丄傾儖僐僉僔僇儖儃僯儖婎乯
側偍丄傾儗僐儕儞偺IUPAC柤偼丄偙偺暘巕峔憿拞偱偼僄僗僥儖偑嵟傕桪愭偝傟傞姱擻婎偱偁傞偐傜丄 methyl 1-methyl-1,2,5,6-tetrahydropyridine-3-carboxylate 偱偁傞丅
3.04
乮悈慺悢乯14 亖 2 亊 乮扽慺悢乯6 亄 2 偱偁傞偐傜丄堦斒幃 CnH(2n+2) 傪枮偨偟偰偍傝丄晄朞榓搙亖侽偱丄懡廳寢崌傕娐偺峔憿傕帩偨側偄傾儖僇儞偱偁傞偙偲偑傢偐傞丅廬偭偰丄暘巬偺巇曽偵傛傞僿僉僒儞偺崪奿堎惈懱偺傒傪扵偣偽傛偄丅
傑偢丄庡嵔偺扽慺悢偑俇偺傕偺丄師偵庡嵔偺扽慺悢偑俆偺傕偺丄偲偄偆傛偆偵弴偵扵偡偲尒棊偲偟偑側偄丅乮仺敪揥乯
乮夝摎椺乯
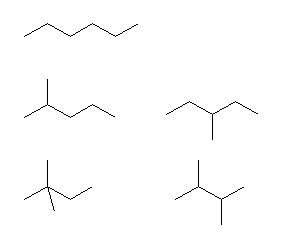
側偍丄柤徧偼師偺捠傝
hexane,
2-methylpentane, 3-methylpentane,
2,2-dimethylbutane, 2,3-dimethylbutane
乮敪揥乯
晄朞榓搙0偱偁傞傾儖僇儞偺崪奿峔憿幃偺扵偟曽
庡嵔偑挿偄弴偵応崌傪恠偔偟側偑傜扵偡丅CnH2n+2 偺偲偒
- 庡嵔偺扽慺悢偑 n 偺偲偒丅 仺 巬暘偐傟側偟丅
- 庡嵔偺扽慺悢偑 n-1 偺偲偒丅 仺 C1婎偑侾偮懁嵔丅
- 庡嵔偺扽慺悢偑 n-2 偺偲偒丅 仺 C2婎侾偮丄傑偨偼C1婎俀偮偑懁嵔丅
- 庡嵔偺扽慺悢偑 n-3 偺偲偒丅 仺 C3婎侾偮丄傑偨偼丄C2婎偲C1婎侾偮偢偮丄傑偨偼丄C1婎俁偮丅
- 懁嵔偑偮偔偙偲偵傛傝庡嵔偺挿偝偑挿偔側傞傛偆側慻傒崌傢偣偼悢偊側偔偰傛偄丅乮偡偱偵丄忋埵偱悢偊嵪傒偱偁傞丅乯
- C1婎偼丄奜懁偐傜俀斣栚埲撪偺扽慺偵抲偔丅堦斣奜懁偺扽慺忋偵偼抲偐側偄丅
- C2婎偼丄奜懁偐傜俁斣栚埲撪偺扽慺偵抲偔丅
- 偦偺傾儖僉儖婎偺嵟挿偺扽慺悢偑 倣 偺応崌丄奜偐傜 倣+1 斣栚埲撪丅偨偲偊偽僀僜僾儘僺儖婎偼丄C2婎偲摨條丄奜偐傜俁斣栚埲撪偵抲偔偙偲偑壜擻丅師偺恾偼丄C3婎傪奜偐傜俁斣栚丄係斣栚偵抲偄偨椺丅奜偐傜俁斣栚偵抲偄偨応崌偼丄庡嵔偺挿偝偑侾偮憹偊傞丅乮仏報偺暘丅偙偺応崌偼摨偠峔憿傪丄庡嵔偺扽慺悢偑侾偮懡偄僌儖乕僾偲偟偰丄奜懁偐傜係斣栚偵C2婎傪抲偄偨傕偺偲偟偰偡偱偵悢偊嵪傒偱偁傞偼偢丅乯乮偙偙偱丄壓恾偺惵悢帤偼丄懁嵔偵偍偗傞斣崋晅偗偱偼側偄偙偲偵拲堄偟偰偔偩偝偄丅懁嵔偵偍偗傞斣崋晅偗偼丄昁偢晅偗崻偺埵抲偺扽慺傪侾斣偵偟傑偡丅乯
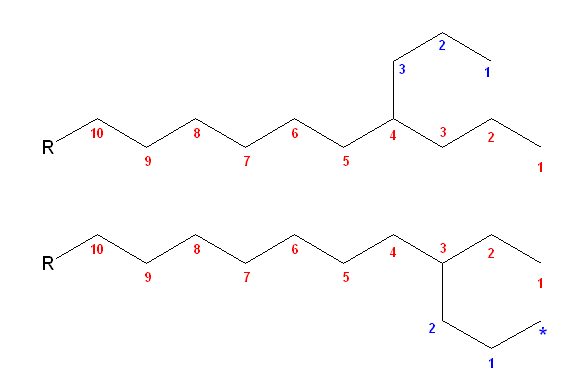
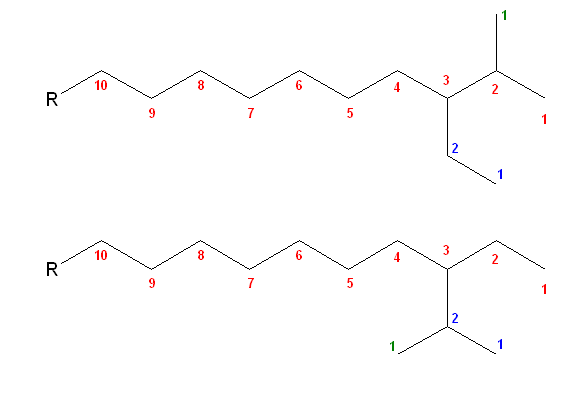
- 懁嵔傪攝抲偡傞偲偒偼丄扽慺悢偑戝偒偄傕偺偐傜抲偔傛偆偵偡傞偲傛偄丅側偍丄C2 埲忋偺懁嵔忋偵偼丄峏偵懁嵔傪抲偔偙偲傕壜擻偲偡傞偙偲偱丄懁嵔傾儖僉儖婎偺堎惈懱偵懳墳偡傞偙偲傕壜擻丅偦偺応崌偼丄懳徠惈偵拲堄偡傞偙偲丅師偺椺偱偼丄C2婎亄C1婎偺抲偒曽俀捠傝傪帵偟偰偄傞偑丄偳偪傜傕摨偠峔憿偵側偭偰偄傞丅
3.05
(a) 儊僠儖僄僗僥儖乮-CO2CH3乯傪帩偮傕偺偲壖掕偟丄暘巕幃偐傜偙偺晹暘傪嵎偟堷偔偲丄C3H7 偲側傞偙偲偐傜丄帵惈幃偱昞偡偲丄C3H7-CO2CH3丄C2H5-CO2C2H5丄 CH3-CO2C3H7丄 H-CO2C4H9丄偺係庬偺壜擻惈偑偁傞丅儊僠儖婎偲僄僠儖婎偼捈嵔傾儖僉儖婎偟偐懚嵼偟側偄偑丄僾儘僺儖婎偲僽僠儖婎偵偼暘巬偟偨峔憿偺堎惈懱偑懚嵼偡傞偙偲偵傕拲堄偡傞丅
慡晹偱俋庬椶偺僄僗僥儖偺堎惈懱偑懚嵼偡傞丅
(b) 僔傾僲婎乮僯僩儕儖婎乯乮-C佭N)傪帩偮偺偱丄偙傟傪暘巕幃偐傜嵎偟堷偔偲C3H7 偲側傞偙偲偐傜丄帵惈幃偼丄C3H7
(c) 僕僗儖僼傿僪寢崌乮 -S-S- 乯傪帩偮丅僕僗儖僼傿僪偲尵偭偨応崌丄尩枾偵偼丄儌僲傾儖僉儖僕僗儖僼傿僪 R-S-S-H 偲丄僕傾儖僉儖僕僗儖僼傿僪 R-S-S-R' 偲偑偁傝摼傞偑丄慜幰偼擬揑偵晄埨掕偱梕堈偵暘夝偡傞偺偱丄幚幙忋丄捠忢僕僗儖僼傿僪偲偄偆応崌偵偼僕傾儖僉儖僕僗儖僼傿僪偺傒傪偝偡偙偲傕懡偄丅側偍丄R-S-S-R' 偵偍偄偰丄R 偲 R' 偑摍偟偄昁梫惈偼側偄丅
乮夝摎椺乯
(a) 埲壓俋庬偺偆偪傛傝彂偔丅
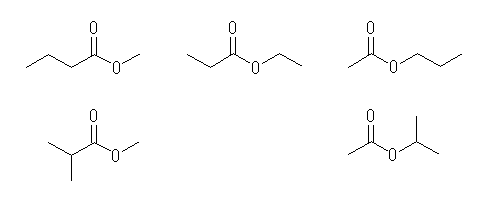
methyl butanoate,
ethyl propanoate,
propyl acetate,
methyl 2-methylpropanoate,
isopropyl acetate
忋恾丄嵍俀偮偼丄C4僇儖儃儞巁偺儊僠儖僄僗僥儖丅
拞墰偼丄C3僇儖儃儞巁偺僄僠儖僄僗僥儖丅
塃俀偮偼丄C2僇儖儃儞巁偺僾儘僺儖僄僗僥儖丅僾儘僺儖婎偵偼俀偮偺峔憿堎惈懱偑偁傞丅
壓恾偼丄C1僇儖儃儞巁偺僽僠儖僄僗僥儖丅僽僠儖婎偵偼係偮偺峔憿堎惈懱偑偁傞丅
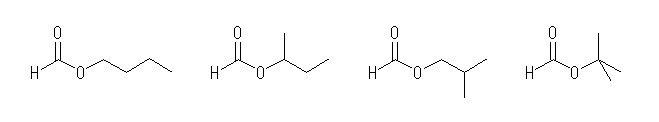
butyl formate,
sec-butyl formate
isobutyl formate
tert-butyl formate
(b) 僾儘僷儞偺堎側傞埵抲偵僔傾僲婎偑抲姺偟偨峔憿偼丄埲壓偺俀偮丅
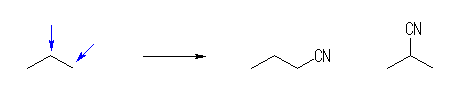
butanenitrile,
2-methylpropanenitrile
峔憿傪扵偡栚揑偱偼乽僾儘僷儞乿偺悈慺傪乽僔傾僲婎偱抲姺乿偟偰偄傞偑丄柦柤偵偍偄偰偼丄僔傾僲婎偺扽慺傕娷傫偩庡嵔偱柦柤偟偰偄傞偙偲偵拲堄偡傞丅
(c) 僕僗儖僼傿僪寢崌傪帩偮峔憿偼丄係偮偺扽慺傪嵍塃偱暘攝偡傞偐傜丄埲壓偺拞偐傜彂偔丅
儌僲傾儖僉儖僕僗儖僼傿僪偲偟偰丄埲壓偺係庬椶丅

嵍傛傝
n-butyl hydrodisulfide (傑偨偼丄butyldisulfane),
sec-butyl hydrodisulfide (傑偨偼丄(1-methylpropyl)disulfane),
isobutyl hydrodisulfide (傑偨偼丄(2-methylpropyl)disulfane),
tert-butyl hydrodisulfide (傑偨偼丄(1,1-dimethylethyl)disulfane)
僕傾儖僉儖僕僗儖僼傿僪偲偟偰丄埲壓偺俁庬椶丅
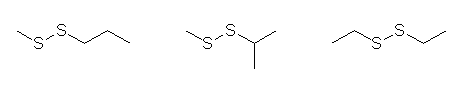
嵍傛傝
methyl propyl disulfide (傑偨偼丄1-(methyldisulfanyl)propane),
isopropyl methyl disulfide (傑偨偼丄2-(methyldisulfanyl)propane),
diethyl disulfide (傑偨偼丄ethyldisulfanylethane)
乮敪揥乯
僀僜僾儘僺儖婎丄僀僜僽僠儖婎摍偵偮偄偰
堦斒偵丄iso 偼丄塸岅偱偼乽摨偠乿乽摍偟偄乿傪昞偡楢寢岅偱偁傝丄isotope乮摨埵懱乯側偳丄乽摨乿乽摍乿偺娍帤偵抲偒姺偊傜傟傞偙偲傕偁傞偑丄乽isopropyl乿乽isobutyl乿偲偄偭偨扨岅偼丄乽iso乿偲乽propyl乿偵暘棧偟偰偦偺傛偆側栿傪梌偊傞傛偆側偙偲偼側偔晄壜暘偱偁傝丄扨偵乽僀僜僾儘僺儖乿乽僀僜僽僠儖乿側偳偲側傞丅
柦柤偵偍偄偰傾儖僼傽儀僢僩弴傪峫椂偡傞嵺偼丄攞悢愙摢岅傗丄埵抲傪昞偡悢帤傗婰崋側偳偑柍帇偝傟傞偺偲偼堎側傝丄偙傟傜偺抲姺婎偼 i 偐傜巒傑傞傂偲偮偺扨岅偲偟偰悢偊傞丅
偙傟傜偼丄嫵壢彂p80偐傜偺仒3.3偵偁傞傛偆偵丄傾儖僉儖婎乮傾儖僇儞傛傝丄悈慺傪侾偮彍偄偨傕偺乯偺偆偪偺堎惈懱偺侾偮偵梌偊傜傟傞姷梡柤偱偁傞丅
嫟捠偟偨峔憿傪尒傞偵丄枛抂傛傝傂偲偮撪懁偺扽慺偵儊僠儖婎偑抲姺偟偨宍乮愭抂偑丄Y偺帤偺傛偆側宍偵暘婒偟偰偄傞宍乯偱偁傞丅
僀僜僾儘僺儖丄僀僜僽僠儖偑嫋偝傟傞偺側傜丄摨條偵丄偡傋偰偺傾儖僉儖婎偵懳偟偰丄摨條偺暘婒峔憿傪帩偮堎惈懱偵丄僀僜傾儖僉儖婎偲昞尰偱偒傞偺偐偲偄偆偲丄偦偆偱傕側偄丅IUPAC偱嫋梕偝傟偰偄傞姷梡柤偺拞偵丄isopropyl, isobutyl, isopentyl, isohexyl 傑偱偼尒摉偨傞偑丄偦傟埲忋偺扽慺悢偺僀僜傾儖僉儖婎偼柍偄丅偮傑傝丄isoheptyl婎丄isooctyl婎側偳偲昞尰偡傞偲丄IUPAC偺婯懃忋丄岆傝偱偁傞偲偄偆偙偲偵側傞丅乮isooctane 偼嫋梕偝傟偨姷梡柤偱偁傞偑丄僀僜僽僞儞乮 Me2CHCH3 乯丄僀僜儁儞僞儞乮 Me2CHCH2CH3 乯丄僀僜傊僉僒儞乮 Me2CHCH2CH2CH3 乯偐傜椶悇偝傟傞偺偲偼堎側傝丄僀僜僆僋僞儞偺峔憿偼丄Me2CHCH2CMe3 偱偁傞丅
偡側傢偪丄乽柦柤朄偵偍偄偰乽iso乿偲偄偆愙摢岅偼丄摨偠扽慺悢偺傾儖僇儞傗傾儖僉儖婎偺枛抂偑丄亅CHMe2 偺峔憿傪帩偮傕偺乿偲偄偆堦斒揑側昞尰偼丄岆傝偱偁傞丅
乮堦斒揑偵乽iso側傫偨傜乿偑偳偆偄偆峔憿偱偁傞偲偄偆婯懃傪弎傋傞偙偲偼偱偒側偄丅偨偩丄嫋梕偝傟偰偄傞椺傪傒偰偔偩偝偄丄偲偟偐尵偊側偄丅乯
3.06
(a) 悈巁婎傪帩偮偺偩偐傜丄帵惈幃偼 C3H7-OH 偱偁傞丅悈巁婎傪悈慺偵抲偒姺偊偨傾儖僇儞 C3H8 偵偮偄偰崪奿堎惈懱傪慡偰扵偟偩偟丄偦傟偧傟傪曣妀偲偡傞傾儖僐乕儖偵偮偄偰悈巁婎傪抲姺偡傞嵺偺埵抲堎惈懱傪偡傋偰扵偡丅
(b) 廘慺傪悈慺偵抲偒姺偊偨傾儖僇儞 C4H10 偵偮偄偰崪奿堎惈懱傪慡偰扵偟丄偦傟偧傟傪曣妀偲偡傞僽儘儌傾儖僇儞偵偮偄偰廘慺傪抲姺偡傞嵺偺埵抲堎惈懱傪偡傋偰扵偡丅
乮夝摎椺乯
(a) 僾儘僷儞 C3H8 偵偼丄崪奿堎惈懱偼懚嵼偟側偄丅偦偺撪偺堦偮偺悈慺傪悈巁婎偵抲偒姺偊偨傕偺偼丄師恾偺捠傝俀庬偱偁傞丅
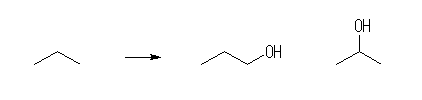
1-propanol,
2-propanol
(b) 僽僞儞 C4H10 偵偼丄崪奿堎惈懱偼俀庬懚嵼偡傞丅偦傟偧傟偺堦偮偺悈慺傪廘慺偵抲偒姺偊偨傕偺偼丄師恾偺捠傝係庬偱偁傞丅
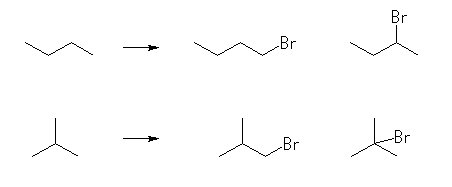
1-bromobutane,
2-bromobutane,
1-bromo-2-methylpropane,
2-bromo-2-methylpropane
3.07
3-06 偲摨條偵峫偊傟偽椙偄丅俆扽慺偺傾儖僉儖婎側偺偱丄俆扽慺偺傾儖僇儞 C5H12 偵偮偄偰崪奿堎惈懱傪慡偰扵偟偩偟丄偦傟偧傟傪曣妀偲偡傞傾儖僉儖婎乮傾儖僇儞偺悈慺傪堦偮庢傝彍偄偨傕偺乯傪扵偣偽傛偄丅
乮夝摎椺乯
儁儞僞儞 C5H12 偵偼丄崪奿堎惈懱偼俁庬懚嵼偡傞丅偦傟偧傟偺堦偮偺悈慺傪庢傝彍偒傾儖僉儖婎偲偟偨傕偺偼丄師恾偺捠傝俉庬偱偁傞丅
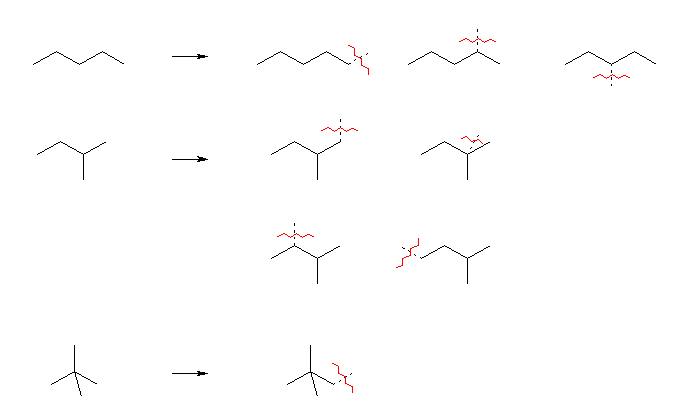
傾儖僉儖婎偺柤徧偼埲壓偺捠傝
pentyl,*1
1-methylbutyl,
1-ethylpropyl,
2-methylbutyl,
1,1-dimethylpropyl,*2
1,2-dimethylpropyl,
3-methylbutyl,*3
2,2-dimethylpropyl*4
拹丗
*1 乽 n- 乿傪偮偗偰捈嵔傾儖僉儖偱偁傞偙偲傪帵偟偰傕椙偄丅乮椺丗n-pentyl 乯
*2 姷梡柤偱偼丄 tert-pentyl
*3 姷梡柤偱偼丄 isopentyl
*4 姷梡柤偱偼丄 neopentyl
乮扽慺俆偺傾儖僉儖婎偱姷梡柤偑嫋偝傟傞偺偼忋婰俁庬偺傒丅傑偨丄偙傟傜偺傾儖僉儖婎偺姷梡柤徧偼丄偦偺桿摫懱傪嶌傞偙偲傪嫋偝側偄丅乮 phenyl婎乮 亅C6H5 乯偐傜偼偦偺桿摫懱偲偟偰椺偊偽 2-chlorophenyl 婎傪嶌傞偙偲偑偱偒傞偑丄chloroisopentyl 婎側偳偺傛偆側暋崌揑側柤徧偺晹暘偲偟偰梡偄傞偙偲偼偱偒側偄丅乯乯
3.08
拲栚偟偰偄傞扽慺偵寢崌偟偰偄傞傾儖僉儖婎偺悢乮 C亅C 寢崌偺悢乯傪悢偊傞丅
乮夝摎椺乯
崪奿峔憿偱帵偝傟偨恾拞偺扽慺尨巕偺偆偪丄愒偱埻傫偩傕偺偑侾媺丄惵偱埻傫偩傕偺偑俀媺丄椢偱埻傫偩傕偺偑俁媺丄墿偱埻傫偩傕偺偑係媺偱偁傞丅
(a) 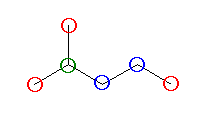
(b) 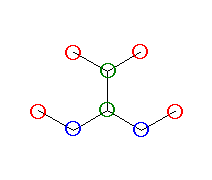
(c) 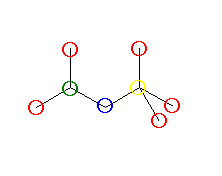
3.09
戞侾媺扽慺偵寢崌偟偨悈慺傪戞侾媺悈慺丄戞俀媺扽慺偵寢崌偟偨悈慺傪戞俀媺悈慺丄戞俁媺扽慺偵寢崌偟偨悈慺傪戞俁媺悈慺偲屇傇偙偲偑偁傞丅
乮夝摎椺乯
3.08 偺夝摎偱戞侾媺扽慺偵寢崌偟偨悈慺偑戞侾媺悈慺丄戞俀媺扽慺偵寢崌偟偨悈慺偑戞俀媺悈慺丄戞俁媺扽慺偵寢崌偟偨悈慺偑戞俁媺悈慺偱偁傞丅戞係媺扽慺偼係杮偺俠亅俠寢崌傪帩偪悈慺偲寢崌偟側偄偐傜丄戞係媺悈慺偲偄偆傕偺偼懚嵼偟側偄丅
峔憿幃偲偺懳墳偵偮偄偰偼丄3.08 偺夝摎椺傪嶲徠丅
3.10
忦審傪枮偨偡傛偆側壔崌暔偼柍尷偵懚嵼偡傞丅乮僔僋儘傾儖僇儞傗傾儖働儞偱偼側偔乯傾儖僇儞偺拞偐傜梌偊傜傟偨忦審偵崌偆傕偺傪傂偲偮慖傋偽傛偄丅
(a) 俀偮偺戞俁媺扽慺埲奜偵扽慺傪帩偨側偄傛偆側傾儖僇儞偼懚嵼偟側偄偺偱丄揔媂丄戞侾媺傗戞俀媺偺扽慺傪曗偭偰峫偊傟偽傛偄丅
(b) 僀僜僾儘僺儖婎偺峔憿偼 亅CH(CH3)2 偱偁傞丅乮嫵壢彂81儁乕僕偺恾3.3傕嶲徠偺偙偲乯
(c) 傕偪傠傫丄(a) 偲摨條偵戞侾媺側偳偺扽慺傪曗偭偰峫偊傟偽傛偄丅
偙偺傛偆側栤戣偱偼丄帺暘偱彂偄偰傒偨峔憿幃偑忦審傪枮偨偟偰偄傞偐偳偆偐丄栤戣 3.08 偲摨條偺曽朄偱妋擣偟偰傒傞偙偲偑廳梫偱偁傞丅
乮夝摎椺乯
埲壓偵偼丄偄偔偮偐偺椺傪帵偡偑丄偐側傜偢丄栤戣 3.08 偲摨條偺曽朄摍偱丄帺暘偺彂偄偨峔憿偑忦審傪枮偨偟偰偄傞偐偳偆偐傪妋擣偡傞偙偲丅
恾偺偆偪丄嵍抂偺傕偺偑嵟掅偺扽慺悢偱梌偊偨傕偺丅偨偩偟(b)偵偮偄偰偼壓偺夝愢傪嶲徠偡傞偙偲丅傑偨恾偺拞偁傞偄偼塃偼巜掕偝傟偰偄側偄媺悢偺扽慺傪捛壛偟偨傕偺丅偙傟傜偱傕忦審傪枮偨偟偰偄傞偺偱惓夝偲偟偰傛偄丅
(a) 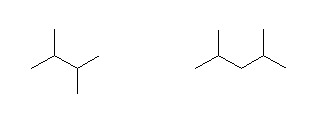
2,3-dimethylbutane,
2,4-dimethylpentane
(b) 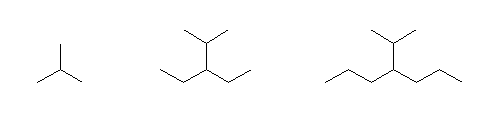
2-methylpropane,
3-ethyl-2-methylpentane,
4-isopropylheptane*1
(c) 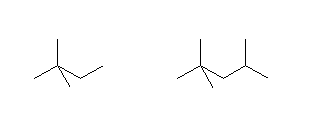
2,2-dimethylbutane,
2,2,4-trimethylpentane
(b) 嵍抂偺暘巕偼丄抲姺婎乮僀僜僾儘僺儖婎乯傪拞怱偵峫偊傞偲丄偦偺抲姺婎偑曣妀偲偟偰偺儊僞儞偵晅偄偰偄傞偙偲偵側傝乮偡側傢偪丄
側偍丄僔僋儘僾儘僷儞偵僀僜僾儘僺儖婎偑抲姺偟偨傕偺乮 isopropylcyclopropane 乯偑丄傾儖僇儞偍傛傃僔僋儘傾儖僇儞偺拞偱丄僀僜僾儘僺儖婎傪柤徧偺拞偵娷傓嵟掅偺暘巕偱偁傞丅偦偺懠丄暘巕撪偵擇廳寢崌傗懠偺抲姺婎偑偁傞応崌傕柦柤忋偱尦偲側傞庡嵔偲偟偰堦斣挿偄扽慺嵔埲奜偑慖偽傟傞応崌偑偁傝丄彮側偄扽慺悢偺傕偺偱傕僀僜僾儘僺儖婎傪抲姺婎偲偟偰柦柤偡傞偙偲偵側傞偙偲傕偁傞丅乮椺丗2-isopropyl-1,3-butadiene 乯
拹 *1 isopropyl婎偼姷梡柤偱丄僔僗僥儉揑側柤徧偱偼 1-methylethyl婎偲側傞丅偟偨偑偭偰偙偺暘巕偼
拹 *2 嫵壢彂p83 柦柤婯懃 抜奒侾 b) 乽挿偝偺摍偟偄擇偮偺堘偭偨扽慺嵔偑懚嵼偡傞応崌偼丄曣懱偵側傞傋偔懡偔偺暘巬揰偑偁傞傕偺傪慖傇乿傛傝丄拞墰偺 3-ethyl-2-methylpentane 偵偮偄偰丄 3-isopropylpentane 偲柦柤偡傞偺偼岆傝偱偁傞丅
3.11-3.20
3.11
(a) C5H12 偼丄堦斒幃 CnH(2n亄2) 偵廬偆偺偱朞榓偺傾儖僇儞偱偁傞丅偦偺崪奿堎惈懱偵偼丄庡嵔偺扽慺悢偑俆偺傕偺丄係偺傕偺丄俁偺傕偺偑懚嵼偡傞丅
(b) 乣 (d) 庡嵔偑偳偙偱偁傞偲偡傞偲堦斣挿偔側傞偐丅傑偨偦偺斣崋偼乮嵍塃偺乯偳偪傜偐傜怳傞曽偑抲姺婎偺埵抲斣崋偑庒偔側傞偐丅
側偍丄(CH3)2CH亅 傗丄(CH3)3C亅 偲偄偆峔憿幃偼師偺峔憿偵懳墳偟偰偄傞丅
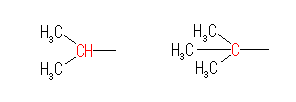
嫵壢彂乮戞俈斉丄戞侾嶞乯乮壓乯偺摎偊丄 3.11(b),(d) 偼娫堘偄偺傛偆偱偡丅傑偁丄庡嵔偺挿偝偵偮偄偰偺偲偙傠偱偡偺偱丄柪偆梋抧偼側偄偲巚偄傑偡偑丅
乮夝摎椺乯
(a) 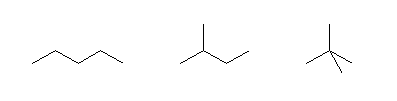
pentane,
2-methylbutane,
2,2-dimethylpropane
(b) 乣 (d) 偱偼丄栤戣暥拞偱摨偠峴撪偱彂偐傟偰偄傞晹暘傪墿怓偺攚宨偱帵偟偨丅偙傟傜偺峔憿偺拞偱堦斣挿偄扽慺嵔偼丄愒偱帵偝傟偨晹暘乮懠偺摍壙側庢傝曽偑偁傞傕偺傕偁傞乯偱偁傞丅
(b) 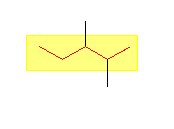
2,3-dimethylpentane
(c) 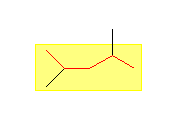
2,4-dimethylpentane
(d) 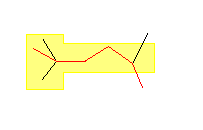
2,2,5-trimethylhexane
乮敪揥乯
壔崌暔柤偵偮偄偰偼丄庼嬈偱傕愢柧偟偨傛偆偵塸岅偱惓偟偔昞婰偱偒傞傛偆偵側傞偙偲丅偙傟偼丄塸岅 仺 擔杮岅偺曄姺偼斾妑揑娙扨偱偁傞偺偵懳偟丄擔杮岅偱偺昞婰偟偐妎偊偰偄側偄応崌偵塸岅偵捈偡偙偲偑偱偒側偄偽偐傝偐丄柦柤偺婯懃拞偵傾儖僼傽儀僢僩弴偲偄偭偨惂栺偑偁傝丄偙傟偼塸岅偺僗儁儖傪抦傜側偄偲懳墳偱偒側偄偐傜偱偁傞丅
傑偨丄暋嶨側壔崌暔偺柦柤偵偮偄偰偼丄扨弮側傾儖僇儞偺柦柤偵桪愭偡傞婯懃偑偁傞丅乮庼嬈偱傗偭偨偲偍傝丅乯嫵壢彂壓姫丄姫枛晅榐A傪嶲徠偡傞偙偲丅偦偺奣梫傪埲壓偵傑偲傔偰偍偔偑丄偙傟傪愭偵奣娤偟偰偍偔偲傛偄丅
- 庡婎乮堦斣桪愭偝傟傞姱擻婎乯傪寛傔傞丅偙傟偑柤慜偺愙旜岅偺晹暘傪寛傔傞丅
- 庡嵔乮曣懱偺扽壔悈慺乯傪尒偮偗傞丅偙偺偲偒丄扨弮側傾儖僇儞偱偼楢懕偟偨嵟傕挿偄扽慺嵔傪尒偮偗傞(師偺 3. 偲 4. 偵奩摉偡傞晹暘偑柍偄)偺偱偁傞偑丄堦斒揑偵偼師偺弴偵寛傔傞丅
- 乮庡姱擻婎悢乯庡婎偑嵟懡偺嵔傪戞侾桪愭偲偡傞丅
- 乮懡廳寢崌悢乯忋偱傂偲偮偵寛傑傜側偄応崌丄懡廳寢崌乮擇廳寢崌偲嶰廳寢崌傪嬫暿偟側偄乯偺悢偑嵟戝偵側傞傕偺傪慖傇丅
- 乮嵔偺挿偝丗扽慺悢乯忋偱傂偲偮偵寛傑傜側偄応崌丄楢懕偟偨扽慺嵔偺挿偝偑挿偄傕偺傪慖傇丅
- 乮擇廳寢崌偺悢亜嶰廳寢崌乯忋偱傂偲偮偵寛傑傜側偄応崌丄擇廳寢崌偺悢偑懡偄傕偺傪慖傇丅
- 乮庡婎偺埵抲乯忋偱傂偲偮偵寛傑傜側偄応崌丄庡婎偺埵抲斣崋偑嵟彫偲側傞傛偆側扽慺嵔傪慖傇丅
- 乮懡廳寢崌偺埵抲乯忋偱傂偲偮偵寛傑傜側偄応崌丄懡廳寢崌偺埵抲斣崋偑丄慻偲偟偰嵟彫乮偼偠傔偵弌偰偔傞斣崋偑嵟彫丄摨偠応崌偵偼師偵偱偰偔傞斣崋偑傛傝彫偝偄丄乧乯偲側傞嵔傪慖傇丅
- 乮懁嵔偺悢乯忋偱傂偲偮偵寛傑傜側偄応崌丄愙摢帿偱昞偝傟傞抲姺婎偺悢乮傾儖僉儖婎偺応崌偵偼丄曣懱忋偺暘婒揰丅僴儘僎儞側偳傕娷傔偰丄懁嵔偺抲姺婎偺悢乯偑嵟懡偺嵔傪慖傇丅
- 乮懁嵔偺埵抲乯忋偱傂偲偮偵寛傑傜側偄応崌丄愙摢帿偱昞偝傟傞抲姺婎偺埵抲斣崋偑丄慻偲偟偰嵟彫乮偼偠傔偵弌偰偔傞悢帤偑嵟彫丄摨偠応崌偵偼師偵偱偰偔傞斣崋偑傛傝彫偝偄丄埲壓摨偠傛偆偵乯偲側傞嵔傪慖傇丅
- 乮彫偝偄懁嵔偺扽慺尨巕悢乯拹忋偱傂偲偮偵寛傑傜側偄応崌丄懁嵔偺扽慺尨巕悢傪彫偝偄曽偐傜斾傋丄嵎偑尒偮偐偭偨偲偙傠偺懁嵔偺扽慺尨巕悢偑戝偒偄傕偺傪慖傇丅
- 忋偱傂偲偮偵寛傑傜側偄応崌丄懁嵔偺暘婒偑嵟彫偺傕偺傪慖傇丅
拹乯弌揟偼乽桳婡壔崌暔丂柦柤朄偺庤堷偒乿乮壔妛摨恖丄1990擭乯ISBN 4-7598-0205-3
偙偺儖乕儖偵傛傟偽丄師偺壔崌暔偼
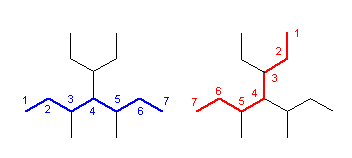
扽慺悢俈偺庡嵔傪俀捠傝慖傋傞偑丄懁嵔偺悢偼偄偢傟傕俁偱摍偟偄丅懁嵔偺埵抲傕偄偢傟傕俁丄係丄俆埵偱摍偟偄丅廬偭偰偙偺儖乕儖偺揔梡偲側傞丅堦曽偺慖傃曽偱偼丄懁嵔偺扽慺悢偑乮侾丄侾丄俆乯偱偁傞偺偵懳偟丄傕偆堦曽偺慖傃曽偱偼懁嵔偺扽慺悢偑乮侾丄俀丄係乯偲側傞丅偦偙偱丄俀斣栚偵彫偝偄懁嵔偺扽慺尨巕悢偱嵎偑傒傜傟偨偺偱丄偙偙偱傛傝戝偒偄屻幰傪慖傇丅偡側傢偪丄
亊丂4-(1-ethylpropyl)-3,5-dimethylheptane
仜丂3-ethyl-5-methyl-4-(1-methylpropyl)heptane
偲偄偆偙偲偵側傞丅側偍丄(1-methylpropyl) 婎偺姷梡柤偼 sec-butyl 婎偱偁傞丅
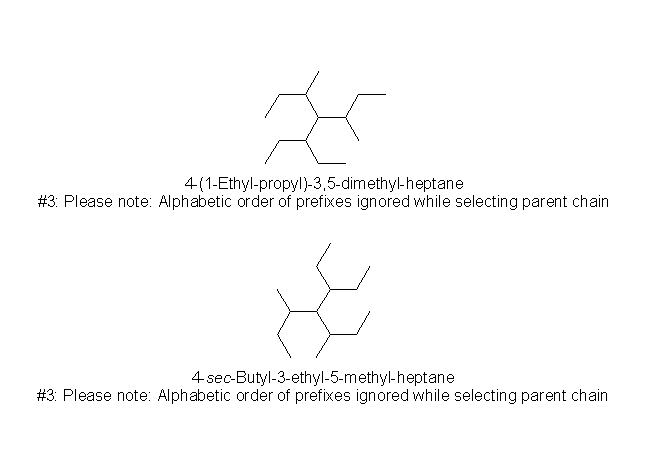
側偍丄巗斕偺壔妛峔憿幃昤夋僜僼僩偱偁傞 ChemBioDraw 傗丄屄恖巊梡偼壽嬥側偟偱巊梡偱偒傞 SymyxDraw 側偳偱偼丄峔憿幃傪彂偄偰柤慜傪昞帵偝偣傞婡擻偑偮偄偰偄傞偑丄昁偢偟傕惓妋偱偼側偄丅埲壓偼乮彂偒曽偑堎側傞偩偗偱乯摨偠暘巕偵懳偟丄偙偺柦柤婡擻傪梡偄偨偲偒偵俀捠傝偺柤慜偑昞帵偝傟偰偄傞椺丅乮忋婰儖乕儖偵傛傟偽丄恾忋曽偺柦柤偼娫堘偄偱丄恾壓曽偺柦柤偑惓偟偄丅乯
3.12
捈嵔傾儖僇儞偺峔憿乮扽慺悢乯偲柤徧偵偮偄偰偼丄庼嬈偱攝晍偟偨僾儕儞僩乮偺側偺側偙傫偨偺側偔偨偺側傝偁傫丄偱偒傘偆偣傫偒傘偆傂傖偔偒傘偆偠傘偆偔両丂亜兌兌兌乯側傜傃偵丄嫵壢彂79儁乕僕偺昞 3.3 傪嶲徠偟丄傛偔暅廗偟偰偍偔偙偲丅
乮夝摎椺乯
壓恾偺捠傝丅側偍丄壓恾偵偍偄偰庡嵔偺扽慺偺嵍偐傜塃傊斣崋傪怳傞傛偆偵帵偟偨丅
(a) 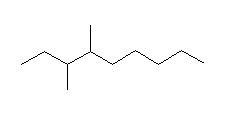
(b) 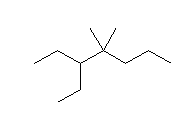
(c) 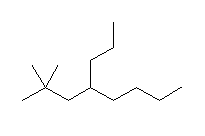
(d) 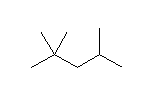
3.13
扨偵傾儖僉儖婎偺柤徧傪梾楍偡傞偺偱偼側偔丄峔憿偲偺娭學偱柦柤偱偒傞傛偆偵偡傞偙偲丅嫵壢彂85儁乕僕丄傾儖僇儞偺柦柤朄婯懃偺乽抜奒俆乿傪嶲徠偟丄暋嶨側傾儖僉儖婎偵偮偄偰偼偦偺拞偵庡嵔晹暘偲暘巬晹暘偵傢偗偰峫偊傞丅
乮夝摎椺乯
乮3.07 偺夝摎傛傝丂嵞宖乯

傾儖僉儖婎偺柤徧偼埲壓偺捠傝
pentyl,*1
1-methylbutyl,
1-ethylpropyl,
2-methylbutyl,
1,1-dimethylpropyl,*2
1,2-dimethylpropyl,
3-methylbutyl,*3
2,2-dimethylpropyl*4
拹丗
*1 乽 n- 乿傪偮偗偰捈嵔傾儖僉儖偱偁傞偙偲傪帵偟偰傕椙偄丅乮椺丗n-pentyl 乯
*2 姷梡柤偱偼丄 tert-pentyl
*3 姷梡柤偱偼丄 isopentyl
*4 姷梡柤偱偼丄 neopentyl
3.14
帵偝傟偨恾傛傝丄偡傋偰偺扽慺尨巕偐傜偼係杮偺扨寢崌偑偱偰偄傞偐傜丄朞榓偺傾儖僇儞偱偁傞偙偲偑傢偐傞丅扽慺摨巑偺寢崌偺弴斣偵拲堄偟偰崪奿峔憿傪婰偡偙偲丅
栤戣偵梌偊傜傟傜暘巕 偺俁師尦柾宆
乮夝摎椺乯
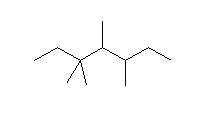 崪奿峔憿幃偼丄嵍恾偺傛偆偵側傞丅
崪奿峔憿幃偼丄嵍恾偺傛偆偵側傞丅
庡嵔偼扽慺悢俈偺僿僾僞儞偵係偮偺儊僠儖婎偑抲姺偟偰偄傞丅斣崋偼恾偺塃偐傜怳傞偲 3,4,5,5- 偲側傞偑丄嵍偐傜怳傞偲 3,3,4,5- 偲側傝乮弶傔偺悢帤偼俁偱摨偠偩偑丄俀斣栚偺悢帤偑係偲俁偱斾傋偰乯傛傝彫偝偔側傞丅
3,3,4,5-tetramethylheptane
3.15
埲壓偺庤弴偱偲偔丅
1) 僾儘僷儞偺 C1亅C2 寢崌幉偵増偭偰傒偨偲偒偺 Newman 搳塭恾傪丄擟堄偺廳側傝宍丄傑偨偼偹偠傟宆偺棫懱攝嵗偵懳偟偰彂偔丅僾儘僷儞偼丄 H3C1-C2H2-CH3 偩偐傜丄C1 偐傜偼俁偮偺悈慺偑丄C2 偐傜偼俀偮偺悈慺偲侾偮偺儊僠儖婎偑寢崌偟偰偄傞丅
2) C1亅C2 寢崌幉偵増偭偰60搙偛偲偵侾夞揮乮0搙偐傜360搙傑偱乯偝偣丄偦傟偧傟偺棫懱攝嵗偵懳墳偡傞 Newman 搳塭幃傪彂偔丅
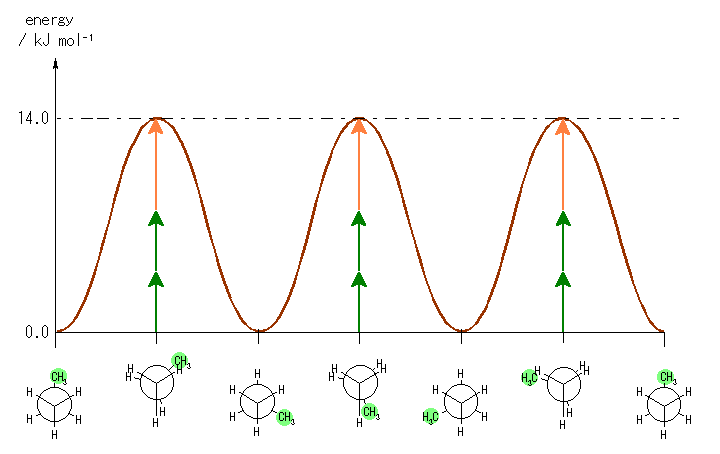
3) 偦傟偧傟偺揰偵偍偗傞僄僱儖僊乕傪媮傔傞丅
偹偠傟宍偵懳偟偰偼丄摿偵憡屳嶌梡偑側偄偺偱丄侽偲偡傞丅廳側傝宍偺憡屳嶌梡偵娭偟偰偼丄嫵壢彂 92 儁乕僕偺恾3.8 傪嶲峫偲偟丄悈慺亅悈慺偺廳側傝侾慻偵懳偟偰 4.0 kJ/mol丄悈慺亅儊僠儖婎偺廳側傝侾慻偵懳偟偰 6.0 kJ/mol 偲峫偊傞丅
4) 僌儔僼偺墶幉偵丄夞揮妏乮擟堄偺揰傪侽搙偲偟偰傛偄乯傪丄廲幉偵偼偦傟偧傟偺棫懱攝嵗偵懳偡傞僄僱儖僊乕傪僾儘僢僩偡傞丅
5) 偙傟傜偺揰傪側傔傜偐偵寢傇丅
乮夝摎椺乯
3.16
壓偺弴彉偱夝偔偲傛偄丅
1) 2-儊僠儖僾儘僷儞偺 C1亅C2 寢崌幉偵増偭偰傒偨偲偒偺 Newman 搳塭恾傪丄擟堄偺廳側傝宍丄傑偨偼偹偠傟宆偺棫懱攝嵗偵懳偟偰彂偔丅
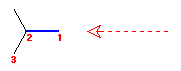
C1 偐傜偼俁偮偺悈慺偑丄C2 偐傜偼侾偮偺悈慺偲俀偮偺儊僠儖婎偑寢崌偟偰偄傞丅
2) C1亅C2 寢崌幉偵増偭偰60搙偛偲偵侾夞揮乮0搙偐傜360搙傑偱乯偝偣丄偦傟偧傟偺棫懱攝嵗偵懳墳偡傞 Newman 搳塭幃傪彂偔丅
3) 偦傟偧傟偺揰偵偍偗傞僄僱儖僊乕傪媮傔傞丅偙偙偱寁嶼偡傞寢壥偑丄(d) 偺偙偨偊偲側傞丅
偹偠傟宍偵懳偟偰偼丄摿偵憡屳嶌梡偑側偄偺偱丄侽偲偡傞丅廳側傝宍偺憡屳嶌梡偵娭偟偰偼丄嫵壢彂 92 儁乕僕偺恾3.8 傪嶲峫偲偟丄悈慺亅悈慺偺廳側傝侾慻偵懳偟偰 4.0 kJ/mol丄悈慺亅儊僠儖婎偺廳側傝侾慻偵懳偟偰 6.0 kJ/mol 偲峫偊傞丅
4) 埲忋偺寢壥傪傕偲偵丄(a) 嵟傕埨掕側丄(b) 嵟傕晄埨掕側 棫懱攝嵗傪寛傔傞丅 5) (c) 僌儔僼偺墶幉偵丄夞揮妏乮擟堄偺揰傪侽搙偲偟偰傛偄乯傪丄廲幉偵偼偦傟偧傟偺棫懱攝嵗偵懳偡傞僄僱儖僊乕傪僾儘僢僩偟丄偙傟傜偺揰傪側傔傜偐偵寢傇丅
乮夝摎椺乯
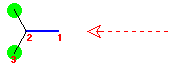
惵偱帵偟偨寢崌幉偑庤慜偐傜岦偙偆偵廳側傞傛偆偵帇揰傪庢傞丅
(a) 嵟傕埨掕側攝嵗偼丄偹偠傟宍攝嵗偺拞偺傂偲偮偱偁傞丅2-儊僠儖僾儘僷儞偱偼丄夞揮妏傪偐偊偰彂偄偨偹偠傟宍攝嵗偼師偺俁偮偲側傞偑丄偙偺僄僱儖僊乕偼偄偢傟傕摍偟偔丄晄埨掕壔傪彽偔憡屳嶌梡偼僛儘偱偁傞丅
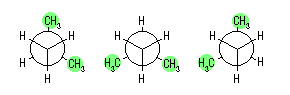
(b) 嵟傕晄埨掕側攝嵗偼丄廳側傝宍攝嵗偺拞偺傂偲偮偱偁傞丅2-儊僠儖僾儘僷儞偱偼丄夞揮妏傪偐偊偰彂偄偨廳側傝宍攝嵗偼師偺俁偮偲側傞偑丄偙偺僄僱儖僊乕偼偄偢傟傕摍偟偄丅乮廳側傝宆憡屳嶌梡偺抣偵偮偄偰偼丄僸儞僩偺 (3) 傪嶲徠偺偙偲乯
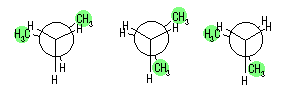
(c) (d) 僌儔僼偺奣宍偍傛傃丄偦偺嬌戝丄嬌彫揰偺僄僱儖僊乕偺憡懳抣偼師偺僌儔僼偺捠傝丅
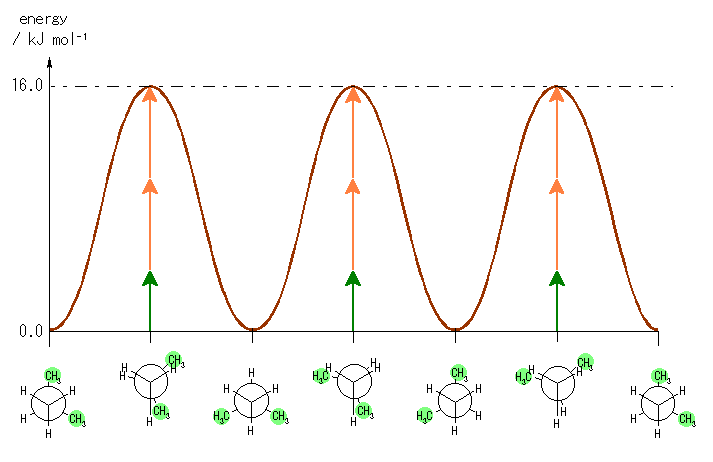
3.17
埲壓偺弴彉偱夝偔偲傛偄丅
1) 2,3-僕儊僠儖僾儘僷儞偺 C2亅C3 寢崌幉偵増偭偰傒偨偲偒偺 Newman 搳塭恾傪丄擟堄偺廳側傝宍丄傑偨偼偹偠傟宆偺棫懱攝嵗偵懳偟偰彂偔丅
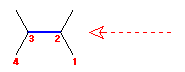
C2 偐傜偼侾偮偺悈慺偲俀偮偺儊僠儖婎偑丄C3 偐傜傕侾偮偺悈慺偲俀偮偺儊僠儖婎偑寢崌偟偰偄傞丅
2) C2亅C3 寢崌幉偵増偭偰60搙偛偲偵侾夞揮乮0搙偐傜360搙傑偱乯偝偣丄偦傟偧傟偺棫懱攝嵗偵懳墳偡傞 Newman 搳塭幃傪彂偔丅
3) 偦傟偧傟偺揰偵偍偗傞僄僱儖僊乕傪媮傔傞丅
3.15丄3.16 偱偼尒傜傟側偐偭偨憡屳嶌梡偲偟偰丄偹偠傟宍偵懳偟偰傕丄俀偮偺儊僠儖婎偑 Gauche 宍偵側偭偰偄傞偲偒偺憡屳嶌梡乮嫵壢彂 93 儁乕僕丄昞3.5傛傝丄侾慻偺儊僠儖婎偵懳偟偰 3.8 kJ/mol 乯傪峫偊傞昁梫偑偁傞丅
廳側傝宍偺憡屳嶌梡偵娭偟偰偼丄嫵壢彂 92 儁乕僕偺恾3.8 傪嶲峫偲偟丄悈慺亅悈慺偺廳側傝侾慻偵懳偟偰 4.0 kJ/mol丄悈慺亅儊僠儖婎偺廳側傝侾慻偵懳偟偰 6.0 kJ/mol 偲峫偊傞丅
4) 埲忋偺寢壥傪傕偲偵丄(a) 嵟傕埨掕側丄(b) 嵟傕晄埨掕側 棫懱攝嵗傪寛傔傞丅
乮夝摎椺乯
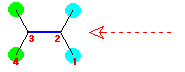
惵偱帵偟偨寢崌幉偑庤慜偐傜岦偙偆偵廳側傞傛偆偵帇揰傪庢傞丅
(a) 嵟傕埨掕側攝嵗偼丄偹偠傟宍攝嵗偺拞偺傂偲偮偱偁傞丅2,3-僕儊僠儖僾儘僷儞偱偼丄夞揮妏傪偐偊偰彂偄偨偹偠傟宍攝嵗偼師偺俁偮偲側傞丅
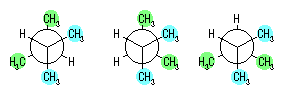
嵍偺傕偺偱偼丄Gauche 憡屳嶌梡偑俀売強丄拞墰偍傛傃塃偺傕偺偱偼丄Gauche 憡屳嶌梡偑俁売強懚嵼偡傞丅廬偭偰丄嵍偺傕偺偑堦斣埨掕側攝嵗偱偁傞丅
(b) 嵟傕晄埨掕側攝嵗偼丄廳側傝宍攝嵗偺拞偺傂偲偮偱偁傞丅2,3-僕儊僠儖僾儘僷儞偱偼丄夞揮妏傪偐偊偰彂偄偨廳側傝宍攝嵗偼師偺俁偮偲側傞丅
拞墰偺傕偺偼丄俀慻偺儊僠儖亅儊僠儖偺廳側傝憡屳嶌梡乮11.0 kJ/mol乯偲丄悈慺亅悈慺偺廳側傝憡屳嶌梡乮4.0 kJ/mol乯傪帩偮丅嵍塃偺俀偮偼丄侾慻偺儊僠儖亅儊僠儖偺廳側傝憡屳嶌梡偲丄俀慻偺悈慺亅儊僠儖偺廳側傝憡屳嶌梡乮6.0 kJ/mol乯傪傕偮丅
埲忋傪峫椂偡傞偲丄拞墰偺傕偺偑堦斣晄埨掕側棫懱攝嵗偱偁傞丅
3.18
C2丄C3 偲傕偵侾偮偺悈慺偲俀偮偺儊僠儖婎偑寢崌偟偰偄傞丅
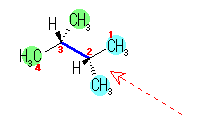
恾傪尒側偑傜丄偙偺夞揮妏偵懳墳偟偨棫懱攝嵗偺 Newman 搳塭幃傪彂偔丅偨偲偊偽丄忋恾偺 2,3-僕儊僠儖僽僞儞傪峔惉偡傞扽慺偺偆偪丄巻柺撪偵偁傞扽慺乮 C1 乣 C4 偲斣崋傪怳偭偨傕偺乯傪丄悅捈側慄忋偵攝抲偡傞偲丄巻柺傛傝庤慜偵偱偰偄傞俀偮偺悈慺偼悅捈側慄偺嵍懁偵丄傑偨巻柺傛傝墱偵偁傞俀偮偺儊僠儖婎偼悅捈側慄偺塃懁偵丄偦傟偧傟昤偔偙偲偲側傞丅
乮夝摎椺乯
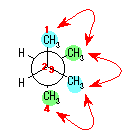
忋恾偺傛偆偵側傝丄俁慻偺儊僠儖亅儊僠儖偺 Gauche 憡屳嶌梡偵傛傞傂偢傒僄僱儖僊乕偑偁傞偐傜丄慡傂偢傒僄僱儖僊乕偼丄
3.8 kJ/mol 亊 3 = 11.4 kJ/mol
偱偁傞丅
3.19
暘巕幃偼 C, H, O, N 偺弴丄偦傟埲奜偺尦慺偼偙偺屻偵傾儖僼傽儀僢僩弴偱婰偡丅
崪奿峔憿幃傪昤偒丄姱擻婎傪儅儖偱埻傫偱丄姱擻婎柤傪婰偡偙偲丅姱擻婎柤偲丄偦偺姱擻婎傪傕偮壔崌暔偺堦斒柤偲偼偒偪傫偲嬫暿偡傞偙偲丅
(a) 庡偵俁庬偺姱擻婎傪傕偮丅
(b) 庡偵俁庬偺姱擻婎傪傕偮丅
摿偵 (b) 偺峔憿幃傪彂偔嵺偵丄栤戣偱梌偊傜傟偰偄傞棫懱揑側恾偱偼丄廳側偭偨傝堿偵塀傟偨傝偟偰尒偊偵偔偄尨巕偑偁傞偺偱丄棊偲偝側偄傛偆偵婥傪偮偗傞偙偲丅
僼僃僯儖傾儔僯儞 偺俁師尦柾宆
儕僪僇僀儞 偺俁師尦柾宆
乮夝摎椺乯
姱擻婎柤偵懕偔僇僢僐撪偼丄偦偺姱擻婎傪帩偮壔崌暔偺堦斒柤丅
(a) phenylalanine, C9H11O2N
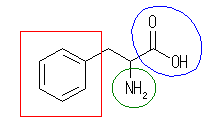
朏崄娐乮傾儗乕儞乯丗愒
傾儈僲婎乮傾儈儞乯丗椢
僇儖儃僉僔婎乮僇儖儃儞巁乯丗惵
(b) lidocaine 乮儕僪僇僀儞乯, C14H22ON2
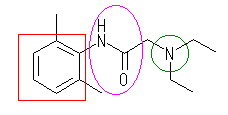
朏崄娐乮傾儗乕儞乯丗愒
傾儈儞拏慺乮傾儈儞乯丗椢
傾儈僪寢崌乮僇儖儃儞巁傾儈僪乯丗搷
乮敪揥乯
lidocaine 乮儕僪僇僀儞乯偺IUPAC柤偼丄
2-diethylamino-N-(2,6-dimethylphenyl)acetamide 偱偁傞丅斣崋偺晅偗曽偼壓恾嶲徠丅乮恾拞丄墿怓攚宨偑柦柤忋偺曣妀偲側偭偰偄傞 acetamide (傑偨偼丄ethanamide乯偱偁傞丅
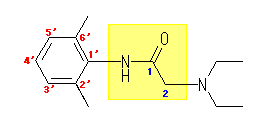
側偍丄戝暥帤偺 N- 偼丄扽慺偺埵抲斣崋偵憡摉偟丄拏慺忋偺抲姺婎傪昞偡丅乮巬暘偐傟偺側偄傾儖僉儖婎偱偁傞丄彫暥帤偺 n- 偲偼堎側傞偺偱拲堄丅乯
3.20
傾儖僇儞偺柦柤朄偵廬偆丅嫵壢彂 3.4 愡傪嶲徠偺偙偲丅
乮夝摎椺乯
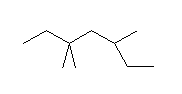
(a) 3,3,5-trimethylheptane
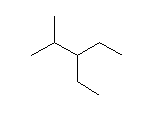
(b) 3-ethyl-2-methylpentane
(c) 2,2,4-trimethylpentane
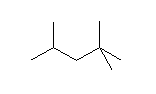
(d) 2-methyl-4-(1-methylethyl)heptane (傑偨偼丄4-isopropyl-2-methylheptane乯*
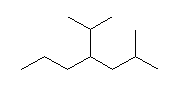
拹*丗懁嵔抲姺婎偼丄傾儖僼傽儀僢僩弴偵暲傋傞丅IUPAC 偱巊梡偺擣傔傜傟偰偄傞姷梡柤僀僜僾儘僺儖婎偺 "iso" 偲 "propyl"偺娫偵偼僴僀僼儞嬫愗傝傕側偔丄i 偱巒傑傞傂偲偮偺扨岅偲偟偰埖傢傟傞丅偦偺偨傔丄摨偠抲姺婎偱傕丄isopropyl婎偲昞婰偡傞偐丄1-methylethyl婎偲昞婰偡傞偐偵傛偭偰丄宯摑柤忋丄暲傃弴偑曄傢傞偙偲偑偁傞丅
3.21-3.30
3.21
姱擻婎傪儅儖偱埻傫偱丄姱擻婎柤傪婰偡偙偲丅姱擻婎柤偲丄偦偺姱擻婎傪傕偮壔崌暔偺堦斒柤偲偼偒偪傫偲嬫暿偡傞偙偲丅
(a) 庡偵俁庬偺姱擻婎傪傕偮丅
(b) 庡偵俀庬偺姱擻婎傪傕偮丅
(c) 庡偵俀庬偺姱擻婎傪傕偮丅偦偺撪偺堦偮偼僇儖儃僯儖婎傪撪曪偡傞丅
(d) 庡偵俀庬偺姱擻婎傪傕偮丅
(e) 庡偵俀庬丄俁売強偺姱擻婎
乮夝摎椺乯
(a) (2-methylaminophenyl)methanol
傑偨偼丄2-(methylamino)benzyl alcohol (benzyl alcohol 偼丄PhCH2OH 偺姷梡柤乯
傑偨偼丄2-hydroxymethyl-N-methylaniline (aniline 偼丄PhNH2 偺姷梡柤乯
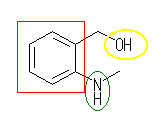
朏崄娐乮傾儗乕儞乯丗愒
傾儈僲婎乮傾儈儞乯丗椢
悈巁婎乮傾儖僐乕儖乯丗墿
(b) cyclohex-2-en-1-one
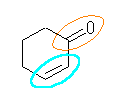
擇廳寢崌乮僔僋儘傾儖働儞乯丗悈怓
僇儖儃僯儖婎乮働僩儞乯丗烌
(c) N-phenylethanamide
傑偨偼丄 N-phenylacetamide
傑偨偼丄 acetoanilide
傑偨偼丄 acetylaminobenzene
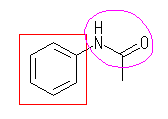
朏崄娐乮傾儗乕儞乯丗愒
傾儈僪寢崌乮僇儖儃儞巁傾儈僪乯丗搷
(d) alanine (姷梡柤乯
傑偨偼丄 2-aminopropanoic acid
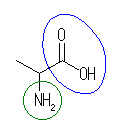
傾儈僲婎乮傾儈儞乯丗椢
僇儖儃僉僔婎乮僇儖儃儞巁乯丗惵
(e) nootkatone (姷梡柤乯
傑偨偼丄4,4a-dimethyl-6-(1-methylvinyl)-4,4a,5,6,7,8-hexahydro-3H-naphthalene-2-one *
傑偨偼丄 5,6-dimethyl-8-(1-methylvinyl)bicyclo[4.4.0]dec-1-ene-3-one
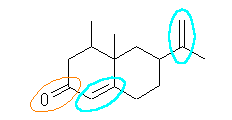
擇廳寢崌乮僔僋儘傾儖働儞乯丗悈怓
僇儖儃僯儖婎乮働僩儞乯丗烌
(f) 4-methylpent-2-ynoyl chloride
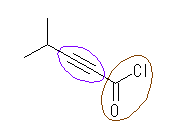
嶰廳寢崌乮傾儖僉儞乯丗巼
僋儘儘僇儖儃僯儖婎乮僇儖儃儞巁墫壔暔乯丗拑
拹*丗乽hydro乿偼丄悈慺尨巕偺晅壛傪帵偡愙摢岅丅hexahydrobenzene 偱 cyclohexane 偺偙偲丄decahydronaphthalene 偱 decalin 偲側傞乮僨僇儕儞偺岅枛偵 e 偼柍偄乯丅
乮敪揥乯
側偍丄戝暥帤偺 N- 偼丄扽慺偺埵抲斣崋偵憡摉偟丄拏慺忋偺抲姺婎傪昞偡丅乮巬暘偐傟偺側偄傾儖僉儖婎偱偁傞丄彫暥帤偺 n- 偲偼堎側傞偺偱拲堄丅乯
3.22
暘巕幃傪枮偨偡傛偆側峔憿傪偲傝偁偊偢堦偮彂偄偰傒傞偲傛偄丅摨偠暘巕幃傪帩偮暘巕摨巑偼丄偐側傜偢暘巕撪偺乮懡廳寢崌悢亄娐峔憿偺悢乯偑堦掕偵側傞丅
(a) 梌偊傜傟偨暘巕幃偼 CnH(2n+2) 偺堦斒幃偵廬偆偺偱丄朞榓側傾儖僇儞偱偁傞丅
(b) 巁慺偼俀杮偺寢崌傪帩偮偙偲傪峫椂偟偰暘巕偺峔憿傪彂偔偲丄暘巕撪偵擇廳寢崌偑堦売強丄傑偨偼娐忬峔憿偑堦売強偁傞偙偲偑傢偐傞丅
乮夝摎椺乯
埲壓偺拞偐傜丄巜掕偝傟偨悢傪夝摎偡傟偽傛偄丅偙偙偱偼丄岝妛堎惈懱傪彍偄偰偡傋偰偺峔憿傪嫇偘偨乮偲巚偆乯丅
(a)
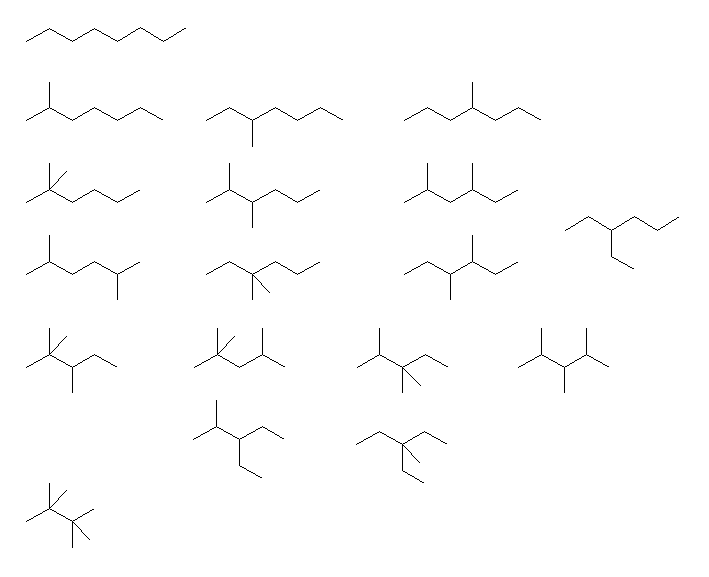
忋傛傝弴偵,
octane,
2-methylheptane,
3-methylheptane,
4-methylheptane,
2,2-dimethylhexane,
2,3-dimethylhexane,
2,4-dimethylhexane,
2,5-dimethylhexane,
3,3-dimethylhexane,
3,4-dimethylhexane,
3-ethylhexane,
2,2,3-trimethylpentane,
2,2,4-trimethylpentane,
2,3,3-trimethylpentane,
2,3,4-trimethylpentane,
3-ethyl-2-methylpentane,
3-ethyl-3-methylpentane,
2,2,3,3-tetramethylbutane
(b)
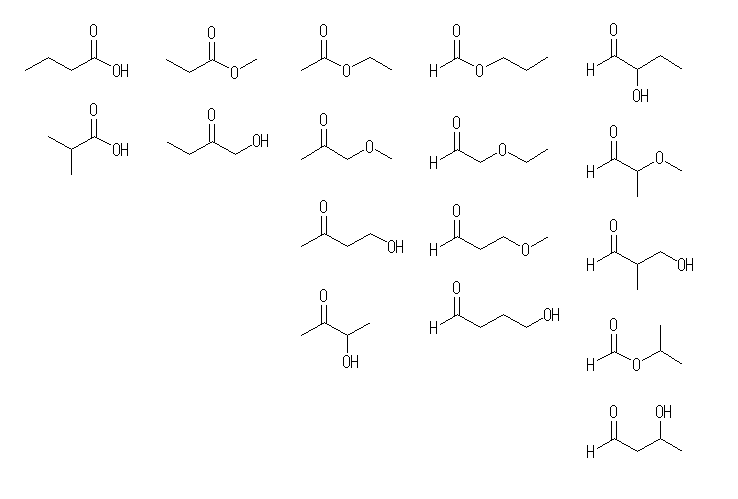
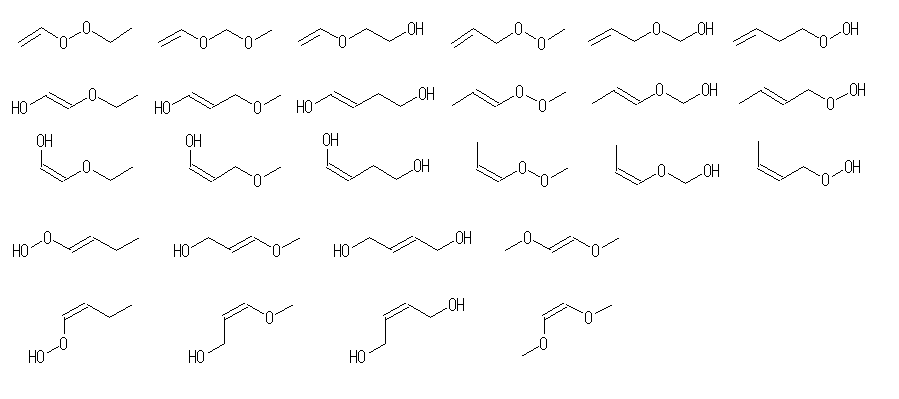
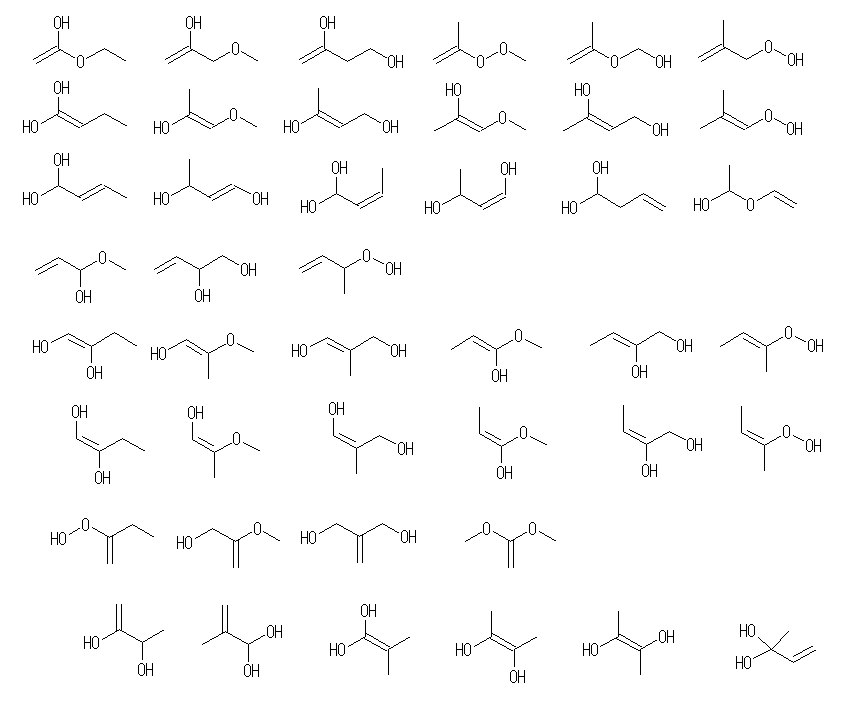
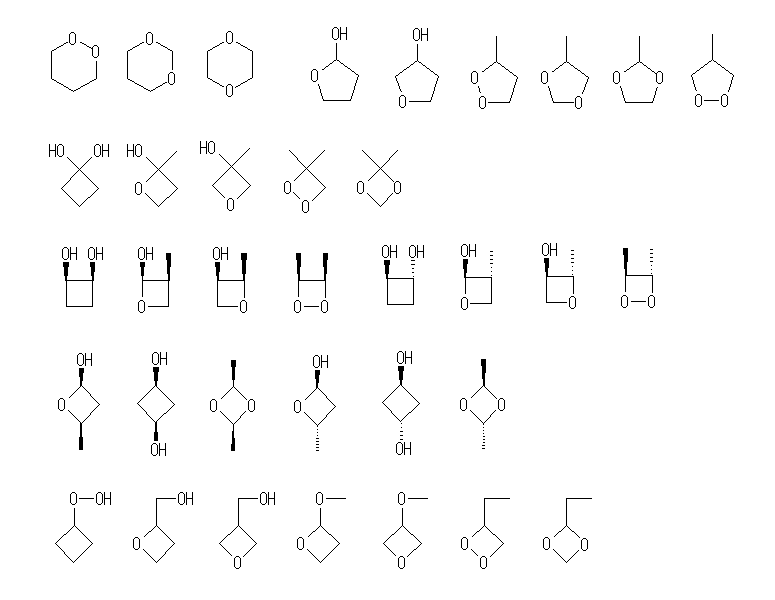
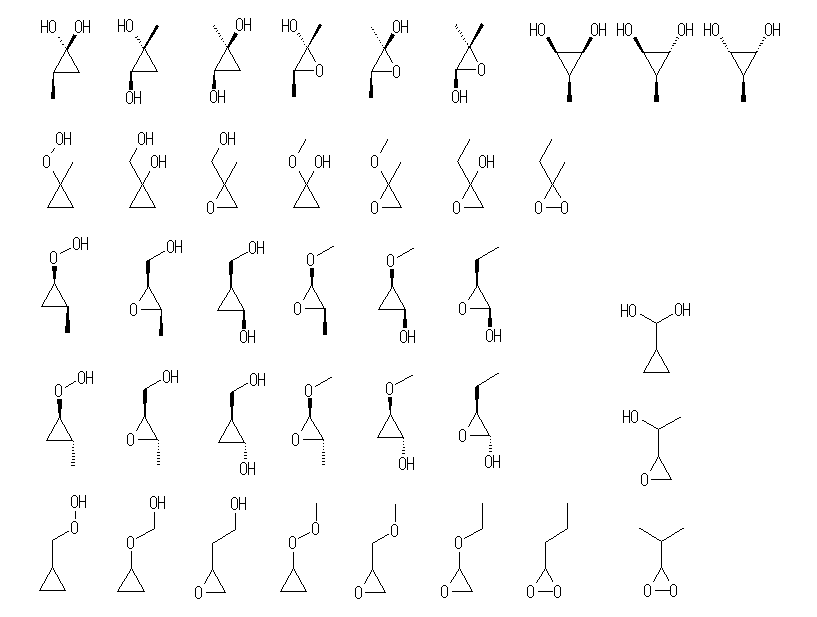
悢偑懡偄偺偱丄柤徧偼徣棯丅
乮敪揥乯
楙廗偺偨傔偵丄側傞傋偔慡偰偺壜擻惈傪峫偊偰傒傞丅
(a) 堎惈懱偼偡傋偰偱18庬椶丄懚嵼偡傞丅
柦柤帪偺曣懱偲側傞乮暘巕撪偱楢懕偟偨堦斣挿偄乯扽慺嵔悢偱暘椶偡傞偲丄
丂俉偺傕偺丂侾庬
丂俈偺傕偺丂俁庬
丂俇偺傕偺丂俈庬丂乮僄僠儖婎傪帩偮傕偺侾庬傪娷傓乯
丂俆偺傕偺丂俇庬丂乮僄僠儖婎傪帩偮傕偺俀庬傪娷傓乯
丂係偺傕偺丂侾庬
偑懚嵼偡傞丅
(b) 堎惈懱偼侾俆俋庬椶乮悢偊娫堘偄偁偭偨傜偛傔傫側偝偄乯懚嵼偡傞丅乮擇廳寢崌偺婔壗乮僔僗亅僩儔儞僗乯堎惈懱丄娐偺棫懱攝抲乮僔僗亅僩儔儞僗乯堎惈懱偼偲傕偵暿偺峔憿偲偟偰悢偊丄岝妛堎惈懱偼嬫暿偟側偄傕偺偲偡傞丅乯
姱擻婎偛偲偵暘椶乮僇僢僐撪偼暘椶偟偨姱擻婎埲奜偺巁慺偺宍懺偲偡傞乯偡傞偲丄
僇儖儃僯儖婎傪娷傓傕偺丂侾俈庬椶
丂僇儖儃儞巁丂俀庬
丂僄僗僥儖丂係庬
丂働僩儞乮悈巁婎乯丂俁庬
丂働僩儞乮僄乕僥儖寢崌乯丂侾庬
丂傾儖僨僸僪乮悈巁婎乯丂俆庬
丂傾儖僨僸僪乮僄乕僥儖寢崌乯丂俀庬
俠亖俠傪娷傓傕偺係俉庬椶乮婔壗堎惈懱俀侾庬傪娷傔傞偲俇俋庬椶乯
丂傾儖働儞乮悈巁婎亊俀乯丂侾俉亄俉庬
丂傾儖働儞乮僄乕僥儖寢崌亄悈巁婎乯丂侾俆亄俇庬椶
丂傾儖働儞乮僄乕僥儖寢崌亊俀乯丂俁亄侾庬椶
丂傾儖働儞乮亅俷俷俼乯丂係亄侾庬椶
丂傾儖働儞乮亅俷俷俫乯丂俉亄俁庬椶
娐忬峔憿偺傕偺俆俇庬椶乮棫懱攝抲堎惈懱侾俈庬傪娷傔傞偲俈俁庬椶乯
丂僔僋儘傾儖僇儞乮悈巁婎亊俀乯丂俋亄俇庬丂乮係堳娐乮俁亄俀乯丄俁堳娐乮俇亄係乯乯
丂僔僋儘傾儖僇儞乮僄乕僥儖寢崌亄悈巁婎乯丂俁亄侾庬
丂僔僋儘傾儖僇儞乮亅俷俷俼乯丂侾庬
丂僔僋儘傾儖僇儞乮亅俷俷俫乯丂係亄侾庬
丂俷傪侾偮娷傓娐乮悈巁婎乯丂侾俈亄俇庬丂乮俆堳娐乮俀乯丄係堳娐乮俈亄俁乯丄俁堳娐乮俉亄俁乯乯
丂俷傪侾偮娷傓娐乮僄乕僥儖寢崌乯丂俇亄侾庬
丂俷傪俀偮娷傓娐丂侾俇亄俀庬丂乮俇堳娐乮俁乯丄俆堳娐乮係乯丄係堳娐乮俇亄俀乯丄俁堳娐乮俁乯乯
側偍丄(b) 偺傛偆側栤戣偵懳偟偰丄乽偡傋偰偺応崌乿傪峫偊傞偨傔偵偼丄埲壓偺傛偆側傾僾儘乕僠偑偍偦傜偔桳梡偱偁傠偆丅
- 傑偢丄C6H12 偺偡傋偰偺崪奿堎惈懱傪嫇偘傞丅
- 擇廳寢崌傕偮傕偺偡傋偰乮婔壗堎惈懱傪彍偄偰侾俁庬椶乯傪扵偡偨傔丄傑偢 C6H14 偺偡傋偰偺崪奿堎惈懱傪嫇偘傞丅俆庬椶偁傞丅偦傟偧傟偵偮偄偰丄堦売強偺扨寢崌傪擇廳寢崌偵岎姺偡傞丅
- 師偵丄娐偺峔憿傪傕偮傕偺偡傋偰乮棫懱攝抲堎惈懱傪彍偄偰侾侾庬椶乯傪扵偡偨傔丄娐偺峔憿偑俇堳娐丄俆堳娐丄係堳娐丄俁堳娐偺弴偵挷傋傞丅
- 擇廳寢崌傕偮傕偺偡傋偰乮婔壗堎惈懱傪彍偄偰侾俁庬椶乯傪扵偡偨傔丄傑偢 C6H14 偺偡傋偰偺崪奿堎惈懱傪嫇偘傞丅俆庬椶偁傞丅偦傟偧傟偵偮偄偰丄堦売強偺扨寢崌傪擇廳寢崌偵岎姺偡傞丅
- 師偵俀係庬椶偺偦傟偧傟偺峔憿偵偮偄偰丄擟堄偺俀売強偺扽慺傪巁慺偵岎姺偟丄偡傋偰偺壜擻惈傪挷傋傞丅
- 嵟屻偵侾俀侾庬椶偺偦傟偧傟偺峔憿偵偮偄偰丄棫懱堎惈懱乮婔壗堎惈懱丄棫懱攝抲堎惈懱丄岝妛堎惈懱乯偑偁傞傕偺偼偳傟偐丄挷傋傞丅
3.23
梌偊傜傟偨暘巕幃偼 CnH(2n+2) 偺堦斒幃偵廬偆偺偱丄朞榓側傾儖僇儞偱偁傞丅
偙偺傛偆側栤戣偺傛偆偵慡偰偺堎惈懱偺峔憿傪昤偐偣傞応崌偱偼丄巚偄偮偄偨傕偺偐傜昤偔偺偱偼側偔丄宯摑揑偵扵偡昁梫偑偁傞丅柦柤帪偺曣懱偲側傞乮暘巕撪偱楢懕偟偨堦斣挿偄乯扽慺嵔悢偱暘椶偟側偑傜扵偡偲傛偄丅
乮夝摎椺乯
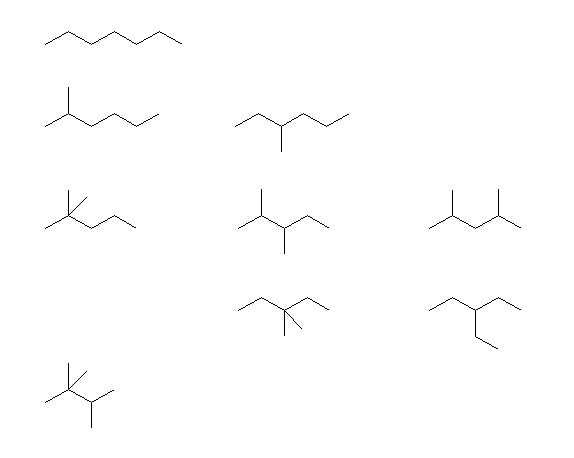
忋傛傝弴偵,
heptane,
2-methylhexane,
3-methylhexane,
2,2-dimethylpentane,
2,3-dimethylpentane,
2,4-dimethylpentane,
3,3-dimethylpentane,
3-ethylpentane,
2,2,3-trimethylbutane
3.24
(a) 傗 (c) 偼丄傑偢偦傟偧傟偺幃傪丄崪奿峔憿幃偱昤偒捈偟偰傒傞偲屳偄偵斾妑偟傗偡偄丅尨巕偺寢崌偺弴彉偺傒偵拲栚偡傟偽傛偄偺偱丄
丒夞揮偝偣偨傝丄棤曉偟偨傝偲偄偭偨憖嶌偱屳偄偵廳偹崌傢偣傞偙偲偑偱偒傞傕偺
丒擟堄偺扽慺傪拞怱偲偟偨寢崌偺曽岦傪擖傟懼偊偰丄扽慺嵔偺嬋偑傝曽傪曄偊傞偙偲偱屳偄偵廳偹偁傢偣傞偙偲偑偱偒傞傕偺
偼摨偠峔憿偱偁傞丅
乮夝摎椺乯
(a) 俁偮偲傕摨偠峔憿偱偁傞丅
(b) 嵍偺俀偮偼摨偠峔憿偩偑丄塃抂偼堎側傞丅
(c) 塃偺俀偮偼摨偠峔憿偩偑丄嵍抂偼堎側傞丅
(a) 2-bromo-3-methylbutane
(b) 1,2-dihydroxybenzene 偲 1,3-dihydroxybenzene
(c) 傪崪奿峔憿幃偵捈偡偲丄師恾偺傛偆偵側傞丅
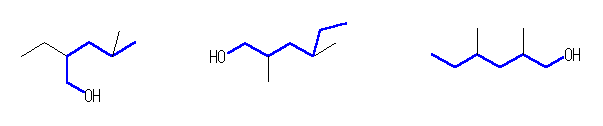
2-ethyl-4-methylpentanol 偲 2,4-dimethylhexanol
3.25
係庬椶偺傾儖僐乕儖偍傛傃俁庬椶偺僄乕僥儖偑堎惈懱偲偟偰懚嵼偡傞丅
暘巕幃傪枮偨偡傛偆側峔憿傪偲傝偁偊偢堦偮彂偄偰傒傞偲傛偄丅摨偠暘巕幃傪帩偮暘巕摨巑偼丄偐側傜偢暘巕撪偺乮懡廳寢崌悢亄娐峔憿偺悢乯偑堦掕偵側傞丅
C4H10O 偼丄暘巕撪偵擇廳寢崌傕娐峔憿傕慡偔傕偨側偄暘巕偱偁傞偙偲偑傢偐傞丅俀杮偺扨寢崌傪傕偭偨巁慺傪娷傓姱擻婎偼丄悈巁婎傑偨偼僄乕僥儖寢崌偱偁傞偐傜丄偙偺暘巕偼傾儖僐乕儖傑偨偼僄乕僥儖偱偁傞偲峫偊傜傟傞丅
傾儖僐乕儖偵偮偄偰偼丄傑偢丄懳墳偡傞傾儖僇儞丄C4H10偺峔憿堎惈懱傪偡傋偰昤偒丄偦傟偧傟偺堎惈懱偵偮偄偰丄堦偮偺悈慺傪悈巁婎偵抲姺偡傞丄偲偄偆庤弴偱峫偊傞偲傛偄丅
僄乕僥儖偵偮偄偰偼丄僄乕僥儖寢崌偺嵍塃偺扽慺偺悢偺彫偝偄傕偺偑侾偱偁傞乮偡側傢偪儊僠儖僄乕僥儖峔憿亖儊僩僉僔婎乮 -O-CH3 乯傪傕偮乯傕偺丄俀偱偁傞乮偡側傢偪僄僠儖僄乕僥儖峔憿亖僄僩僉僔婎傪傕偮乯傕偺丄偲偄偆傛偆偵弴偵峫偊傟偽傛偄丅
儊僩僉僔婎乮 -O-CH3 乯傪傕偮 C4H10O 傪偡傋偰宯摑偩偰偰扵偡偨傔偵偼丄乽 C4H10O 乿亅乽 -O-CH3 乿亄乽 -H 乿亖乽 C3H8 乿偺峔憿堎惈懱傪偡傋偰昤偒丄偦傟偧傟偺堎惈懱偵偮偄偰丄堦偮偺悈慺傪儊僩僉僔婎偵抲姺偡傞丄偲偄偆庤弴偱峫偊傞偲傛偄丅乮偙偺寁嶼幃偼丄C4H10O 暘巕偺拞偺儊僩僉僔婎 -O-CH3 傪丄悈慺 -H 偵抲偒姺偊傞偲偳偺傛偆側暘巕幃偵側傞偐丄偲偄偆偙偲偵懳墳偟偰偄傞丅乯
乮夝摎椺乯
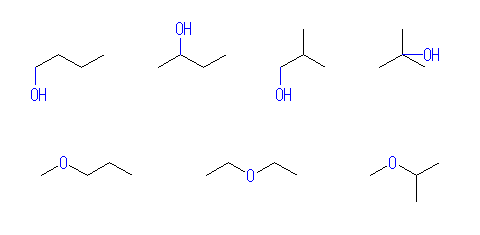
1-butanol,
2-butanol,
2-methyl-1-propanol,
2-methyl-2-propanol,
(n-butyl alohol,
sec-butyl alohol,
isobutyl alohol,
tert-butyl alohol,)
methyl propyl ether,
diethyl ether,
isopropyl methyl ether
乮敪揥乯
暘巕幃傪枮偨偡傛偆側峔憿傪偲傝偁偊偢堦偮彂偄偰傒側偔偰傕丄晄朞榓搙傪媮傔偰傗傟偽丄
C4H10O 偑丄暘巕撪偵擇廳寢崌傕娐峔憿傕慡偔傕偨側偄暘巕偱偁傞偙偲偑敾抐偱偒傞丅
側偍丄巁慺偼俀杮偺寢崌傪帩偮偺偩偐傜丄宍幃揑偵偼 C亅H 寢崌偺娫偵巁慺傪憓擖偡傟偽丄悈慺偺悢偺憹尭側偟偵丄偨偲偊偽 傾儖僇儞 R亅H 傪傾儖僐乕儖 R亅O亅H 偵曄姺偡傞偙偲偑偱偒偰偟傑偆丅偮傑傝丄偙傟偼偁傞暘巕幃偺暘巕偺傕偮晄朞榓搙傪敾抐偡傞偨傔偵偼丄巁慺偺悢偼慡偔柍帇偟偰乮 C4H10O 偺戙傢傝偵 C4H10 傪梡偄偰乯傾儖僇儞偺堦斒幃偵偁偰偼傔偰峫偊偰峔傢側偄偙偲傪帵偡丅
3.26
(a) 揔摉側傾儖僇儞傪峫偊丄偦偺偆偪偺堦売強偺儊僠儗儞乮亅CH2亅乯傪僇儖儃僯儖偵曄偊傟偽傛偄丅偨偩偟丄枛抂偺扽慺偺応崌偼傾儖僨僸僪偵側偭偰偟傑偄丄働僩儞偱偼側偄偺偱拲堄偡傞丅
(b) 姱擻婎偺昞傛傝傾儈僪偺峔憿傪妋擣偟丄扽慺悢偑慡晹偱係偵側傞傛偆偵揔媂傾儖僉儖婎偺挿偝摍傪挷惍偡傞丅
偨偩偟丄拏慺忋偵偼擟堄偺悢偺傾儖僉儖婎傪攝偟偰傕峔傢側偄偑丄拏慺忋偵傾僔儖婎乮 R-CO- 乯傪俀偮帩偮応崌偵偼丄傾儈僪偱偼側偔僀儈僪偲屇偽傟傞偺偱拲堄偡傞丅
(c) 姱擻婎偺昞傛傝僄僗僥儖寢崌偺峔憿傪妋擣偟丄扽慺悢偑慡晹偱俆偵側傞傛偆偵揔媂傾儖僉儖婎偺挿偝摍傪挷惍偡傞丅
偨偩偟丄R-CO2- 偺塃懁偵悈慺偑偔傞偲丄僄僗僥儖偱偼側偔僇儖儃儞巁偲側傞偺偱拲堄偡傞丅
(d) 朏崄娐偐傜傾儖僨僸僪婎偑捈寢偟偰偄傞傕偺傪巜偡丅暘巕撪偵朏崄娐傪帩偭偰偄偰傕丄傾儖僨僸僪婎偲偺娫偵帀朾嵔偑偁傞応崌偵偼帀朾懓傾儖僨僸僪偲偟偰埖傢傟傞丅
(e) 揔摉側僄僗僥儖峔憿傪昤偒丄偦偺偆偪偺堦売強偺儊僠儗儞乮亅CH2亅乯傪僇儖儃僯儖偵曄偊傟偽傛偄丅偨偩偟丄R-CO2-CO-R' 偺峔憿偲側傞応崌偼丄巁柍悈暔偱偁傞偺偱働僩僄僗僥儖偲偼屇偽側偄丅
(f) 揔摉側傾儖僇儞傪昤偒丄揔摉側埵抲偵傾儈僲婎偲悈巁婎傪抲姺偡傞丅乮偨偩偟丄堦斒揑偵偼偦傟偧傟堎側傞扽慺忋偵抲姺偡傞丅乯
乮夝摎椺乯
埲壓偺椺偺傎偐丄乮娐忬峔憿傗乯懡廳寢崌傪帩偮傕偺傕夝偱偁傞丅
(a) 埲壓偺峔憿傛傝丄擟堄偺傂偲偮傪摎偊傞丅
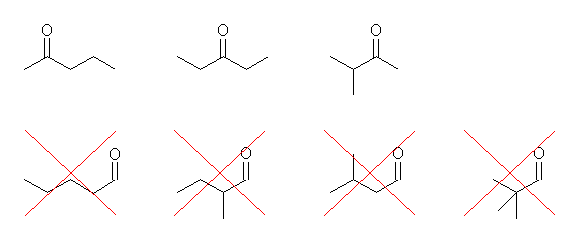
忋偺恾偺壓抜偼丄摨偠僇儖儃僯儖婎傪帩偮偑丄働僩儞偱偼側偔傾儖僨僸僪側偺偱栤戣偺忦審偵偼崌抳偟側偄丅
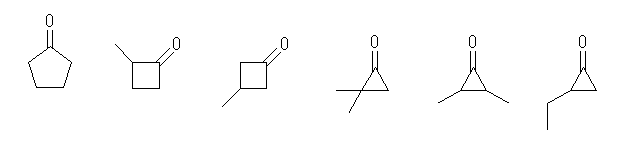
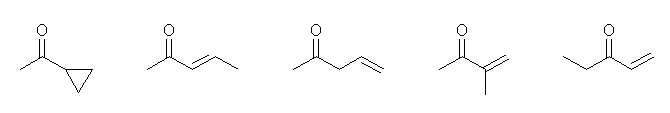
(b) 埲壓偺峔憿傛傝丄擟堄偺傂偲偮傪摎偊傞丅
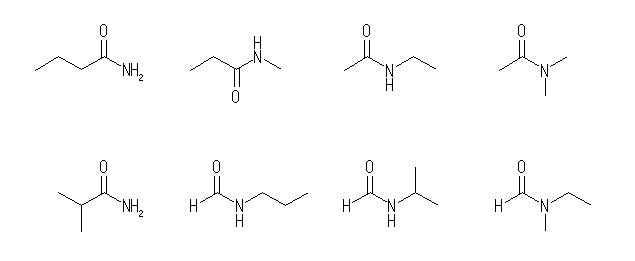
側偍丄壓恾偺偆偪丄嵍抂埲奜偺傛偆側娐忬偺傾儈僪椶偼摿偵乽儔僋僞儉乿偲屇偽傟傞偙偲偑偁傞丅乮嵍抂偼丄僔僋儘傾儖僉儖婎傪傕偮捠忢偺傾儈僪乯
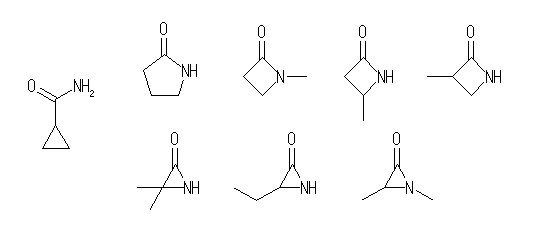
(c) 埲壓偺峔憿傛傝丄擟堄偺傂偲偮傪摎偊傞丅
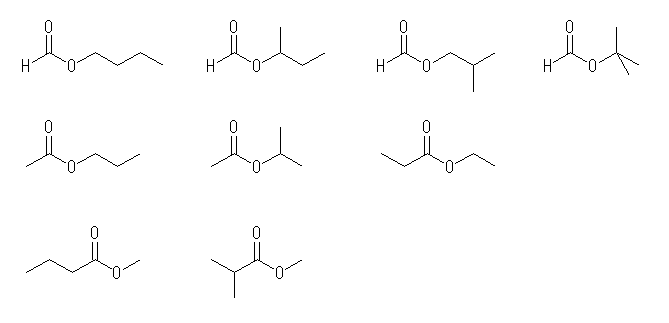
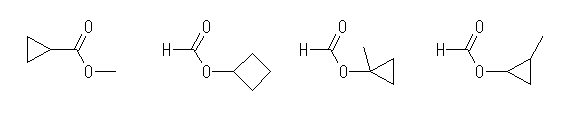
側偍丄壓恾偺傛偆側娐忬偺僄僗僥儖椶偼乽儔僋僩儞乿偲屇偽傟傞偙偲偑偁傞丅
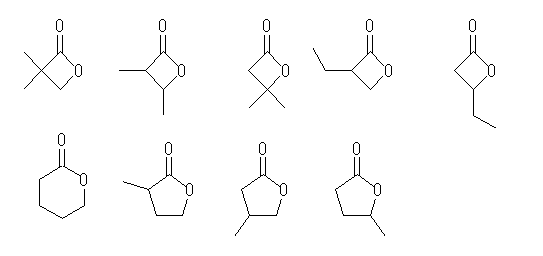
(d) 椺 benzaldehyde
儀儞僛儞娐傗僫僼僞儗儞娐偵傾儖僨僸僪婎 -CHO 偑捈寢偟偨傕偺傪椺偲偟偰帵偣偽傛偄丅乮Ph-CH2-CHO 側偳偺傛偆偵丄暘巕撪偵朏崄娐偑偁偭偨偲偟偰傕傾儖僨僸僪婎偺寢崌埵抲偑傾儖僉儖婎偱偁傞応崌丄僼僃僯儖婎傪傕偮帀朾懓傾儖僨僸僪偲偟偰暘椶偝傟傞丅乯
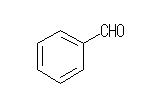
(e) 椺 methyl 2-oxobutanate
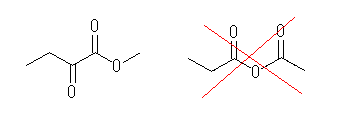
塃偺傛偆側峔憿乮R-CO-O-CO-R'乯偼丄巁柍悈暔偱偁傝丄働僩僄僗僥儖偱偼側偄丅
(f) 椺 2-aminoethanol
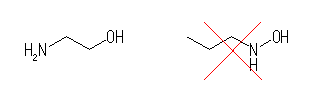
塃偺傛偆側峔憿乮拏慺忋偵悈巁婎偑抲姺偟偨傕偺乯偼丄僸僪儘僉僔儖傾儈儞偱偁傞丅
乮敪揥乯
(a) 扽壔悈慺晹暘偑朞榓側峔憿偺傒傪帩偮傕偺傪峫偊傞傕偺偲偡傞丅
娐峔憿傪帩偨側偄堎惈懱偼丄俁庬椶懚嵼偡傞丅
偙偺慡偰傪嫇偘傞偨傔偵偼丄C5H12 偺崪奿堎惈懱偡傋偰傪峫偊丄擟堄偺儊僠儗儞 乮亅CH2亅乯傪僇儖儃僯儖乮亅C(=O)亅乯偵曄偊傞丅
傑偨偼丄僇儖儃僯儖婎傪拞怱偵偍偒丄偦偺嵍塃偵揔摉側傾儖僉儖婎傪偦偺崌寁偺扽慺悢偑係偲側傞傛偆偵攝偡丅
娐忬峔憿傪帩偮傕偺偼丄乮棫懱攝抲堎惈懱偼彍偒丄傑偨僔僋儘傾儖僉儖婎傪帩偮侾庬椶傪傆偔傔偰乯俈庬椶懚嵼偡傞丅
(b) 扽壔悈慺晹暘偑朞榓側峔憿偺傒傪帩偮傕偺傪峫偊傞傕偺偲偡傞丅
拏慺忋偵傾儖僉儖抲姺婎傪帩偨側偄乮偡側傢偪 亅CONH2 峔憿傪帩偮傕偺乯堎惈懱偼俀庬椶懚嵼偟丄拏慺忋偵傾儖僉儖抲姺婎傪帩偮傕偺偱偼丄乮儊僞儞傾儈僪丄偡側傢偪儂儖儉傾儈僪椶傕娷傔偰乯偝傜偵俇庬椶偑懚嵼偡傞丅
(c) 扽壔悈慺晹暘偑朞榓側峔憿偺傒傪帩偪丄娐偺峔憿傪帩偨側偄傕偺偺傒傪峫偊傞傕偺偲偡傞丅
儊僞儞巁乮偡側傢偪僊巁乯偺桿摫懱傕娷傔傞偲丄慡晹偱俋庬椶偲側傞丅
3.27
偄偢傟傕丄壓偺傛偆偵峫偊偰峔憿傪彂偄偰傒偨偺偪丄暘巕幃偑梌偊傜傟偨傕偺偲摨偠偱偁傞偐偳偆偐丄妋擣偟偰傒傞偙偲丅悈慺偺悢偑俀屄懡偄偺偱偁傟偽偳偙偐偵擇廳寢崌傑偨偼娐偺峔憿傪憹傗偡丄側偳偡傞丅
(a) R-CO-R' 偺梌偊傜傟偨暘巕幃 C4H8O 傛傝丄働僩儞婎乮僇儖儃僯儖婎丄-CO- 乯傪堷偒嶼偡傞偲丄 R-R' 偵懳偟偰 C3H8 偲側傝丄傾儖僇儞偺堦斒幃偲側傞偙偲傛傝丄椉傾儖僉儖婎 R, R' 晹暘偼朞榓偱丄偦偺扽慺悢偺崌寁偼俁偱偁傞偙偲偑敾傞丅偙偺傛偆側忦審傪枮偨偡壔崌暔偼堦捠傝偺傒偱偁傞丅
(b) R-CN 偺梌偊傜傟偨暘巕幃 C5H9N 傛傝丄僔傾僲婎乮 -CN 乯傪堷偒嶼偟偰悈慺傪懌偡偲丄R-H 偵懳偟偰 C4H10 偲側傝丄傾儖僇儞偺堦斒幃偲側傞偙偲傛傝丄傾儖僉儖婎 R 偺晹暘偼朞榓偱偁傞偙偲偑敾傞丅R-H 丄 C4H10 偺崪奿堎惈懱俀庬偺偦傟偧傟偵偮偄偰丄擟堄偺悈慺傪傂偲偮僔傾僲婎偵抲姺偡傞曽朄偱 R-CN 偺偡傋偰偺堎惈懱傪扵偡偙偲偑偱偒傞丅慡偰偱係庬椶偺堎惈懱偑懚嵼偡傞丅
(c) OHC-R-CHO 偺梌偊傜傟偨暘巕幃 C4H6O2 傛傝丄俀偮偺傾儖僨僸僪婎乮儂儖儈儖婎丄-CHO 乯傪堷偒嶼偟丄俀偮偺悈慺傪懌偡偲丄H-R-H 偵懳偟偰C2H6 偲側傝丄傾儖僇儞偺堦斒幃偲側傞偙偲傛傝 R 偺晹暘偼朞榓偱偁傞偙偲偑敾傞丅僄僞儞 C2H6 偺擇偮偺悈慺傪傾儖僨僸僪婎偱抲姺偡傞曽朄偼丄埵抲偺堘偄偵傛傝俀庬椶懚嵼偡傞丅
(d) R-Br 偺梌偊傜傟偨暘巕幃 C6H11Br 傛傝丄廘慺傪悈慺偵抲姺偟偨応崌偺 R-H 偺暘巕幃偼 C6H12 偱偁傝丄傾儖僇儞偺堦斒幃偵斾妑偟偰悈慺偺悢偑俀屄彮側偄丅栤戣偺戣堄傛傝丄偙傟偼傾儖働儞偱偁傞丅偡側傢偪丄扽慺悢俇偺傾儖働儞傪偡傋偰昤偒丄偝傜偵偦偺偦傟偧傟偵偮偄偰丄擟堄偺悈慺傪傂偲偮傪廘慺偵抲姺偡傞曽朄偱 R-Br 偺偡傋偰偺堎惈懱傪扵偡偙偲偑偱偒傞丅
婔壗堎惈懱傪嬫暿偟側偄傕偺偲偟偰偐偧偊偰丄C6H12 偺傾儖働儞偼13庬椶懚嵼偟丄R-Br 偼 56庬椶懚嵼偡傞丅
(e) 俆庬椶偺堎惈懱偑懚嵼偡傞丅庡嵔偺扽慺悢偑俇偺傕偺丄俆偺傕偺丄乧偺弴偵悢偊傞偲傛偄丅
(f) 棫懱攝抲堎惈懱傪悢偊側偄傕偺偲偟丄侾俀庬椶偺堎惈懱偑懚嵼偡傞丅娐忬偺晹暘偺扽慺悢偑俇偺傕偺丄俆偺傕偺丄乧偺弴偵悢偊傞偲傛偄丅
(g) 婔壗堎惈懱傪悢偊側偄傕偺偲偟丄俇庬椶偺堎惈懱偑峫偊傜傟傞丅乮 C=C=C 偺傛偆側峔憿傪傕偮俁庬椶傪娷傓丅乯
(h) 働僩傾儖働儞偱偁傞偐傜丄暘巕撪偵働僩儞婎偲扽慺扽慺擇廳寢崌偑娷傑傟傞丅偙偺擇偮偺姱擻婎偑椬愙偟偰 R-C=C-CO-R' 偲側偭偰偄偰傕峔傢側偄偑丄椬愙偟偰偄傞応崌偼摿偵丄擇廳寢崌偺埵抲傪摿掕偡傞偨傔偵 α,β-晄朞榓働僩儞偲偄偆柤徧偱屇偽傟傞丅R-CO-R' 偺梌偊傜傟偨暘巕幃 C5H8O 傛傝丄働僩儞婎乮僇儖儃僯儖婎丄-CO- 乯傪堷偒嶼偡傞偲丄 R-R' 偵懳偟偰 C4H8 偲側傝丄椉傾儖僉儖婎 R, R' 晹暘偺堦曽偺傒偵擇廳寢崌偑偁傝丄偙傟傜偺扽慺悢偺崌寁偼係偱偁傞偙偲偑敾傞丅傑偢丄懳墳偡傞働僩儞傪彂偒丄擇廳寢崌傪曗偆傛偆偵偟偰峫偊傞丅偡側傢偪丄R, R' 晹暘偺扽慺悢偑俁亄侾偱偁傞応崌丄俀亄俀偱偁傞応崌丄偲暘偗偰峫偊傞偲傛偄丅偡傋偰偱係庬椶偺堎惈懱偺壜擻惈偑峫偊傜傟傞丅
乮夝摎椺乯
壓偵帵偡拞傛傝揔摉側峔憿傪侾偮帵偡丅
(a)
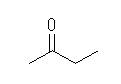
2-butanone
n-butane 傪彂偒丄傂偲偮偺擟堄偺儊僠儗儞傪僇儖儃僯儖 C=O 偵曄姺偡傞偲丄忋恾偵側傞丅枛抂偺扽慺傪僇儖儃僯儖婎偵曄姺偡傞偲傾儖僨僸僪乮R-C(=O)H, 傑偨偼丄R-CHO乯偵側偭偰偟傑偆偺偱丄夝摎偼忋偺侾庬椶偺傒丅
(b)
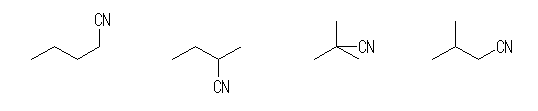
pentanenitrile,
2-methylbutanenitrile,
2,2-dimethylpropanenitrile,
3-methylbutanenitrile
忋恾丄嵍偺俀偮偼 n-butane 傪彂偄偰丄擟堄偺悈慺侾偮傪僔傾僲婎乮-CN乯偵抲偒姺偊偨傕偺丅懳徧惈偺娭學偱俀庬椶偑彂偗傞丅塃偺俀偮偼丄2-methylpropane 傪彂偒丄擟堄偺悈慺侾偮傪僔傾僲婎偵抲偒姺偊偨傕偺丅C4H10 偺崪奿堎惈懱偼俀庬椶側偺偱丄C5H9CN 乮C4H9-CN乯偺峔憿偼丄忋偺係庬椶偺傒丅
(c)
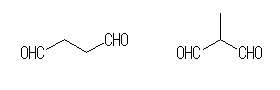
butanedial,
2-methylpropanedial
僄僞儞 C2H6 傪彂偒丄擟堄偺俀偮偺悈慺傪傾儖僨僸僪婎乮儂儖儈儖婎偲傕偄偆丅-CHO乯偵抲偒姺偊偨傕偺偲偟偰峫偊傞偙偲偑偱偒傞丅
傑偨偼丄C4H10 偺崪奿堎惈懱偼俀庬椶傪彂偒丄枛抂偺埵抲偺扽慺俀偮傪傾儖僨僸僪婎偵抲偒姺偊偨傕偺丄偲偟偰峫偊偰傕摨偠寢榑偵側傞丅
(d)
旕忢偵懡偔偺峔憿偑彂偗傞偺偱丄偄偔偮偐椺傪帵偟偨丅
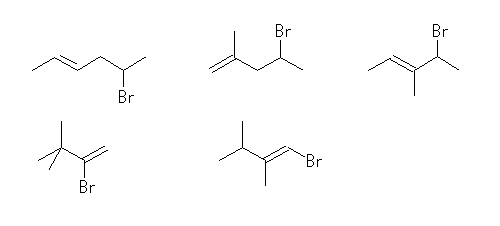
5-bromo-2-hexene,
4-bromo-2-methyl-1-pentene,
5-bromo-3-methyl-2-pentene,
2-bromo-3,3-dimethyl-1-butene,
1-bromo-2,3-dimethyl-1-butene
偡傋偰偺壜擻惈傪嫇偘傞偨傔偵偼丄師偺傛偆偵峫偊傟偽傛偄丅偡側傢偪丄
1) 廘慺抲姺懱偺曣妀偲側傞 C6H12 偺堎惈懱偼丄C6H14 傛傝攈惗偝偣偨侾俁庬椶偁傞丅
2) 偙傟傜偺偦傟偧傟偵偮偄偰丄擟堄偺埵抲偺悈慺傪廘慺偵抲姺偡傞偲忦審偵崌抳偟偨峔憿傪彂偗傞丅
師恾偱偼丄偙偺侾俁庬椶偺峔憿堎惈懱偵偮偄偰丄懳徧偱偼側偄悈慺偺埵抲傪愒偄栴報偱帵偟偨丅偙偺栴報偺悢偩偗丄忦審傪枮偨偟丄偦傟偧傟偑堎側偭偨峔憿傪彂偔偙偲偑偱偒傞丅
側偍丄偙傟傜偺柦柤偵偁偨偭偰偼丄栤偄 3.11 偺敪揥偺崁傪嶲徠偡傞偙偲丅懁嵔偺埵抲偺慜偵懡廳寢崌偺埵抲偱扽慺嵔偺斣崋偑寛掕偡傞偙偲偵拲堄丅
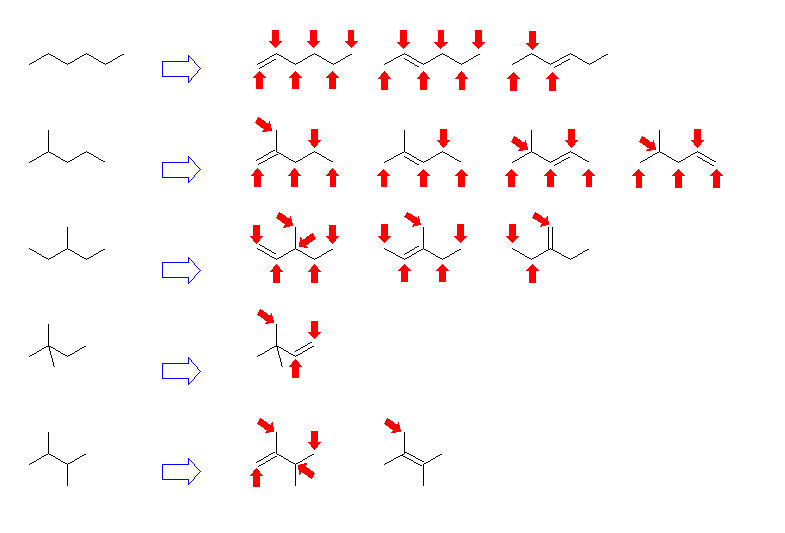
(e)
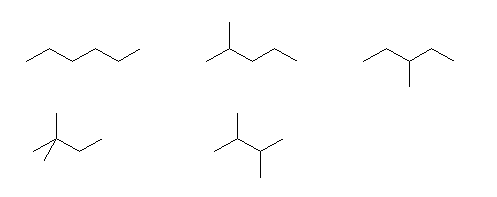
hexane,
2-methylpentane,
3-methylpentane,
2,2-dimethylbutane,
2,3-dimethylbutane
庡嵔偺挿偝偑俇偺傕偺丄俆偺傕偺丄偲偄偆傛偆偵偡傋偰傪恠偔偟側偑傜彂偔偲傛偄丅
(f)
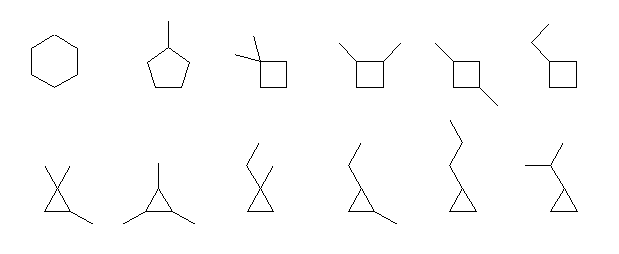
乮忋抜乯
cyclohexane,
methylcyclopentane,
1,1-dimethylcyclobutane,
1,2-dimethylcyclobutane,
1,3-dimethylcyclobutane,
ethylcyclobutane,
乮壓抜乯
1,1,2-trimethylcyclopropane,
1,2,3-trimethylcyclopropane,
1-ethyl-1-methylcyclopropane,
1-ethyl-2-methylcyclopropane,
propylcyclopropane,
(1-methylethyl)cyclopropane
娐偑丄俇堳娐丄俆堳娐丄偲偄偆傛偆偵偡傋偰傪恠偔偟側偑傜彂偔偲傛偄丅
側偍丄1-methylethyl 婎偼 isopropyl 婎偲偟偰柦柤偟偰傕傛偄丅
(g)
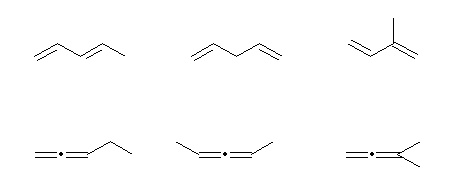
penta-1,3-diene,
penta-1,4-diene,
2-methylbuta-1,3-diene,
penta-1,2-diene,
penta-2,3-diene,
3-methylbuta-1,2-diene
C5H12 偺峔憿堎惈懱乮n-pentane丄 2-methylbutane丄2,2-dimethylpropane 偺俁庬椶乯傪彂偒丄弌棃忋偑傞峔憿偑廳暋偟側偄傛偆偵擇廳寢崌傪俀偮摫擖偡傞偲忋恾偺傛偆偵側傞丅側偍丄2,2-dimethylpropane 偼扽慺偺暲傃傪曄偊偢偵擇廳寢崌傪摫擖偡傞偙偲偼偱偒側偄丅
忋偺抜丄嵍抂偲塃抂偵嫟捠偟偰偄傞晹暘峔憿乮 C=C-C=C 乯偼乽嫟栶擇廳寢崌, conjugated double bond乿偲屇偽傟傞丅
壓偺俁偮偵嫟捠偟偰偄傞晹暘峔憿乮 C=C=C 乯偼丄乽廤愊擇廳寢崌, cumulative double bond乿偲屇偽傟丄偙偺峔憿傪帩偮壔崌暔傪憤徧偟偰乽僋儉儗儞, cumulene乿偲屇傇丅
嵟彫偺僋儉儗儞偱偁傞 propadiene, H2C=C=CH2偺姷梡柤偱偁傞乽傾儗儞, allene乿傪梡偄丄偦偺摨懓楍柤偲偟偰乽僋儉儗儞乿偺戙傢傝偵乽傾儗儞乿偑梡偄傜傟傞偙偲傕偁傞丅
(h)
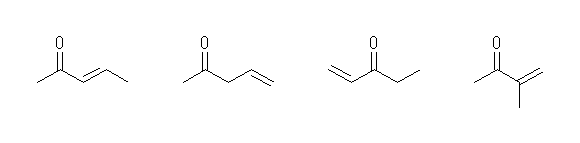
3-penten-2-one,
4-penten-2-one,
1-penten-3-one,
3-methyl-3-buten-2-one
傑偢丄3.26 (a) 偲摨條偵峫偊丄C5H10O 偺暘巕幃傪帩偮偡傋偰偺働僩儞乮2-pentanone, 3-pentanone, 3-methyl-2-pentanone乯偺峔憿傪彂偒丄壜擻側埵抲偵擇廳寢崌傪摫擖偡傞偲丄忋偺峔憿幃偑彂偗傞丅
3.28
偄偢傟傕丄壓偺傛偆偵峫偊偰峔憿傪彂偄偰傒偨偺偪丄暘巕幃偑梌偊傜傟偨傕偺偲摨偠偱偁傞偐偳偆偐丄妋擣偟偰傒傞偙偲丅
(a) R-OH 偺梌偊傜傟偨暘巕幃 C4H10O 傛傝丄悈巁婎傪悈慺偵抲偒姺偊傞偲丄 R-H 偵懳偟偰 C4H10 偲側傝丄傾儖僇儞偺堦斒幃偲側傞丅偡側傢偪偙偺傾儖僐乕儖偼懡廳寢崌摍傪娷傑側偄丅偙偺傾儖僇儞偺崪奿堎惈懱傪偡傋偰扵偟偨偺偪丄偦傟偧傟偵偮偄偰擟堄偺悈慺傪悈巁婎偱抲姺偡傞曽朄偱丄R-OH 偺偡傋偰偺堎惈懱傪扵偡偙偲偑偱偒傞丅梌偊傜傟偨忦審偵懳偟丄係捠傝偺傾儖僐乕儖偑懚嵼偡傞丅
(b) 梌偊傜傟偨暘巕幃 C5H13N 偑 R-NH2 偺峔憿傪帩偮傕偺偲峫偊偰丄傾儈僲婎傪悈慺偵抲偒姺偊傞偲丄R-H 偵懳偟偰 C5H12 偲側傝丄傾儖僇儞偺堦斒幃偲側傞丅偡側傢偪偙偺傾儈儞偼懡廳寢崌摍傪娷傑側偄丅偙傟偼丄N忋偵傾儖僉儖婎偑暋悢偁傞傛偆側乮戞俀媺丄傑偨偼戞俁媺偺乯傾儈儞偱傕摨條偵敾掕偱偒傞丅乮R-NH 傪 R-NHCH3 偵曄姺偡傞偺偼丄宍幃忋丄N-H 寢崌偺娫偵(CH2)傪憓擖偡傞偙偲偱偁傝丄傾儖僇儞偺堦斒幃 CnH(2n+2) 偺 n 傪侾憹壛偝偣傞偩偗偱偁傞丅乯
偲偙傠偱丄偙偺暘巕幃偺傾儈儞傪偡傋偰尒偮偗傞偨傔偵偼埲壓偺俀偮偺峫偊曽偑偁傞丅
傑偢丄戞侾媺傾儈儞乮R-NH2乯丄戞俀媺傾儈儞乮R-NH-R'乯丄戞俁媺傾儈儞乮RR'R"N乯偺弴偵偦傟偧傟偺堎惈懱傪偡傋偰扵偡曽朄偵偮偄偰愢柧偡傞丅
梌偊傜傟偨暘巕幃 C5H13N 偑戞侾媺傾儈儞 R-NH2 偺峔憿傪帩偮傕偺偲峫偊偰丄傾儈僲婎傪悈慺偵抲偒姺偊傞偲丄R-H 偵懳偟偰 C5H12 偲側傞丅偡側傢偪丄扽慺悢俆偺傾儖僇儞偺崪奿堎惈懱傪偡傋偰扵偟偨偺偪丄偦傟偧傟偵偮偄偰擟堄偺悈慺傪傾儈僲婎偱抲姺偡傞曽朄偱丄R-NH2 偺偡傋偰偺堎惈懱傪扵偡偙偲偑偱偒傞乮俉庬椶乯丅師偵戞俀媺傾儈儞偺峔憿傪帩偮傕偺偲偡傞丅俀偮偺傾儖僉儖婎偺扽慺悢偑丄侾亄係丄俀亄俁 偺偦傟偧傟偺応崌偵偮偄偰峫偊傟偽傛偄乮俇庬椶乯丅摨條偵丄戞俁媺傾儈儞偺峔憿傪帩偮傕偺偲偟偨応崌偵偼丄俁偮偺傾儖僉儖婎偺扽慺悢偑侾亄侾亄俁丄侾亄俀亄俀 偺偦傟偧傟偺応崌偵偮偄偰峫偊傟偽傛偄丅
師偺峫偊曽偲偟偰丄扽慺偲拏慺傪娷傔偨尨巕偺暲傃曽偵拲栚偟偰暘偗傞曽朄傪愢柧偡傞丅
忋偲摨條偺峫嶡偵傛傝丄暘巕撪偵懡廳寢崌偑側偄偙偲偑敾偭偨偺偱丄扽慺悢偲拏慺悢傪偁傢偣偰俇偩偐傜丄傑偢丄扽慺悢俇偺傾儖僇儞偺崪奿堎惈懱傪偡傋偰扵偡偙偲偵偡傞丅偙傟傜偺傾儖僇儞偺擟堄偺戞侾媺偺扽慺傪拏慺偵抲偒姺偊傞偲丄扽慺悢俆偺戞侾媺傾儈儞偑摼傜傟傞丅扽慺悢俇偺傾儖僇儞偺擟堄偺戞俀媺偺扽慺傪拏慺偵抲偒姺偊傞偲丄扽慺悢俆偺戞俀媺傾儈儞偑摼傜傟傞丅扽慺悢俇偺傾儖僇儞偺擟堄偺戞俁媺偺扽慺傪拏慺偵抲偒姺偊傞偲丄扽慺悢俆偺戞俁媺傾儈儞偑摼傜傟傞丅戞係媺偺扽慺偼丄拏慺偵偼抲偒姺偊傜傟側偄丅乮拏慺偼宍幃揹壸傪帩偨側偄拞惈尨巕偱偁傞応崌偵偼丄俁杮偟偐寢崌傪帩偨側偄偨傔丅乯
姷傟偰偔傞偲屻幰偺曽偑懍偔摎偊偵扝傝拝偔偐傕偟傟側偄丅偙偺曽朄傪丄(a) 偵揔梡偡傞偵偼丄扽慺悢俆偺傾儖僇儞偺崪奿堎惈懱傪偡傋偰扵偟偨偺偪丄偦偺拞偺擟堄偺戞侾媺扽慺傪巁慺偵抲偒姺偊偨応崌偑扽慺悢係偺傾儖僐乕儖偺偡傋偰偺堎惈懱偱偁傞丅傑偨丄擟堄偺戞俀媺扽慺傪巁慺偵抲偒姺偊偨応崌偼摨偠扽慺悢偺僄乕僥儖偺偡傋偰偺堎惈懱偲側傞丅乮仺 (f) 乯
(c),(d) 傾儖僨僸僪丄働僩儞偼偲傕偵僇儖儃僯儖婎傪帩偮暔幙偱偁傞丅R-CO-R' 偺梌偊傜傟偨暘巕幃 C5H10O 傛傝丄僇儖儃僯儖婎丄-CO-傪堷偒嶼偡傞偲丄 R-R' 偵懳偟偰 C4H10 偲側傝丄傾儖僇儞偺堦斒幃偲側傞偙偲傛傝丄椉傾儖僉儖婎 R, R' 晹暘偼朞榓偱丄偦偺扽慺悢偺崌寁偼係偱偁傞偙偲偑敾傞丅
R 偍傛傃 R' 偵娭偟偰丄偳偪傜傕扽慺悢偑侾埲忋偱偁傞応崌乮R 偲 R' 偺扽慺悢 侾亄俁 傑偨偼 俀亄俀乯偼働僩儞丄偳偪傜偐堦曽偑悈慺偺応崌乮侽亄係乯偼傾儖僨僸僪偱偁傞丅
傑偨丄師偺傛偆偵峫偊偰傕傛偄丅扽慺悢俆偺傾儖僇儞乮偡側傢偪 C5H12 乯偺偡傋偰偺崪奿堎惈懱傪扵偟偩偟丄偦偺戞侾媺偺扽慺傪僇儖儃僯儖婎偺扽慺偵抲姺偡傞乮 R-CH3 仺 R-(C=O)H 乯偲丄傾儖僨僸僪偑惗偠傞丅傑偨戞俀媺偺扽慺偺扽慺傪僇儖儃僯儖婎偺扽慺偵抲姺偡傞乮 R-CH2-R' 仺 R-(C=O)-R' 乯偲丄働僩儞偑惗偠傞丅乮偄偆傑偱傕側偄偑丄戞俁媺丄戞係媺偺扽慺偱偼偙偺庬偺抲偒姺偊偼偱偒側偄丅乯
(e) R-CO2-R' 偺梌偊傜傟偨暘巕幃 C4H8O2 傛傝丄僄僗僥儖寢崌晹暘 -CO2- 傪堷偒嶼偡傞偲丄R-R' 偵懳偟偰 C3H8 偲側傝丄傾儖僇儞偺堦斒幃偲側傞偙偲傛傝丄椉傾儖僉儖婎 R, R' 晹暘偼朞榓偱丄偦偺扽慺悢偺崌寁偼俁偱偁傞偙偲偑敾傞丅偨偩偟丄傾儈儞傗僄乕僥儖丄働僩儞摍偱摨條偺峫嶡傪偟偨偲偒偲偼堎側傝丄R 偲 R' 偼摍壙偱偼側偄丅傑偨丄R 偺扽慺悢偼侽偱傕椙偄偑丄R' 偺扽慺悢偑侽偺帪偼丄僄僗僥儖偱偼側偔僇儖儃儞巁偲側傞偙偲偵拲堄偡傞丅偡側傢偪丄R 偲 R' 偺扽慺悢 侽亄俁 傑偨偼 侾亄俀 傑偨偼 俀亄侾 偺偦傟偧傟偺応崌偑偁傞丅乮僇儖儃儞巁偵偮偄偰傕崌傢偣偰専摙偡傞応崌偼丄俁亄侽 傕娷傔傞丅乯
偙偙偱丄(b) 乣 (d) 偺屻敿晹暘偱夝愢偟偰偒偨傛偆側丄扽慺丄拏慺丄巁慺偺尨巕偺庬椶傪柍帇偟偨帪偺暲傃曽偵拲栚偡傞暘椶偺曽朄傕揔梡偱偒側偄傢偗偱偼側偄丅3.25 (b) 偺乽敪揥乿偵揧偭偰峫偊丄僄僗僥儖傗僇儖儃儞巁偵側傝偆傞傕偺偼偳傟偐傪尒偮偗傟偽傛偄丅
(f) R-O-R' 偺梌偊傜傟偨暘巕幃 C4H10O 傛傝丄僄乕僥儖寢崌巁慺 -O- 傪堷偒嶼偡傞偲丄R-R' 偵懳偟偰 C4H10 偲側傝丄傾儖僇儞偺堦斒幃偲側傞偙偲傛傝丄椉傾儖僉儖婎 R, R' 晹暘偼朞榓偱丄偦偺扽慺悢偺崌寁偼係偱偁傞偙偲偑敾傞丅R 偲 R' 偺扽慺悢 侾亄俁 傑偨偼丄俀亄俀 偵偮偄偰専摙偡傟偽傛偄丅乮 侽亄係 偼傾儖僐乕儖傪梌偊傞丅乯
傑偨偼丄(b)偺僸儞僩偺屻敿傪傒傛丅
乮夝摎椺乯
(a) 埲壓偺係捠傝丅
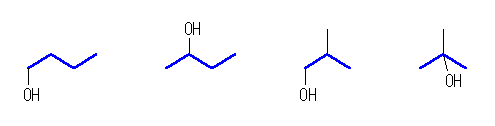
嵍傛傝丄
butan-1-ol,
butan-2-ol,
2-methylpropan-1-ol,
2-methylpropan-2-ol
(b) 埲壓偺侾俈捠傝丅
侾媺偺傾儈儞
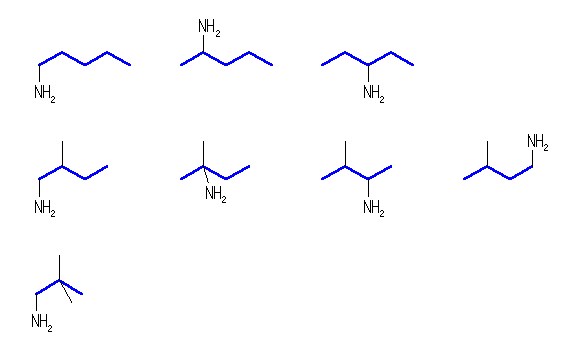
俀媺偺傾儈儞
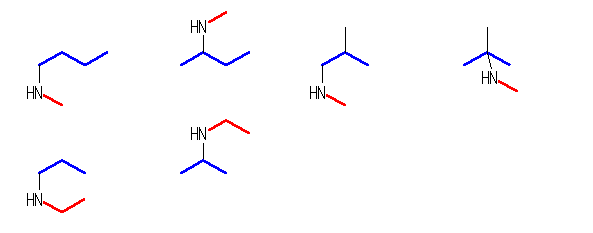
俁媺偺傾儈儞
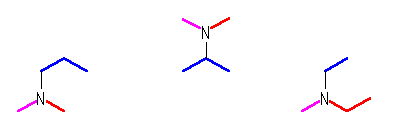
僸儞僩傪嶲徠偵丄埲壓偺傛偆偵扵偟偰傕傛偄丅
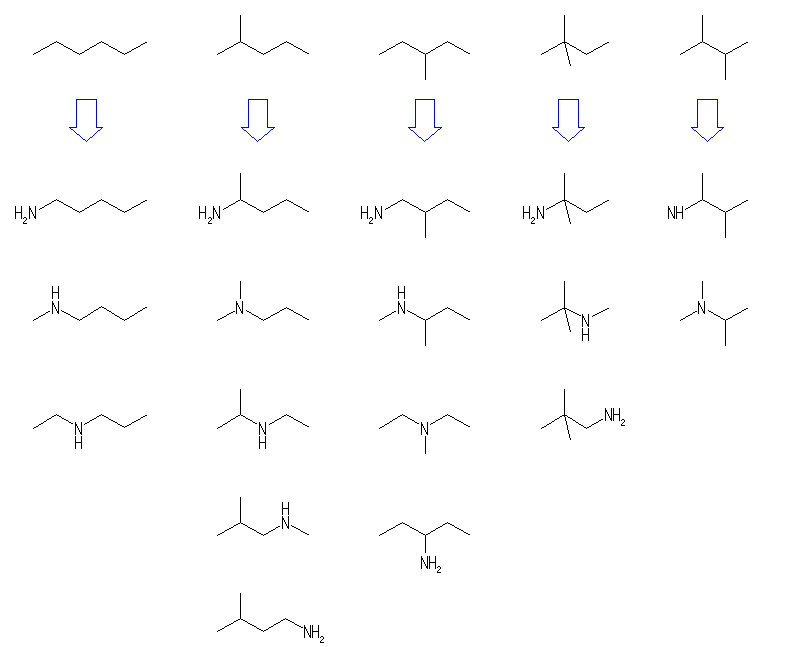
(a),(f) 偙傟傜偺僄乕僥儖偲傾儖僐乕儖偼姱擻婎堎惈懱偱偁傞丅
(b) 偺僸儞僩屻敿偺傛偆偵峫偊傞偲丄師恾偺傛偆偵側傞丅
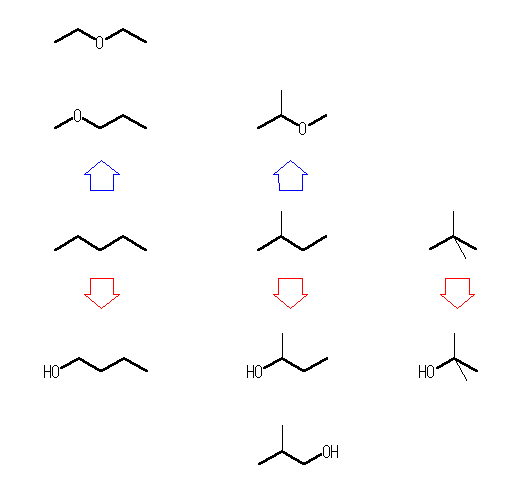
僄乕僥儖乮惵栴報懁乯丂嵍
diethyl ether,
methyl propyl ether,
拞 isopropyl methyl ether
傾儖僐乕儖乮愒栴報懁乯丂
嵍 butan-1-ol,
拞 butan-2-ol,
2-methylpropan-1-ol,
塃 2-methylpropan-2-ol
(c),(d) 偙傟傜偺働僩儞偲傾儖僨僸僪偼姱擻婎堎惈懱偱偁傞丅
僸儞僩屻敿偺傛偆偵峫偊傞偲丄師恾偺傛偆偵側傞丅
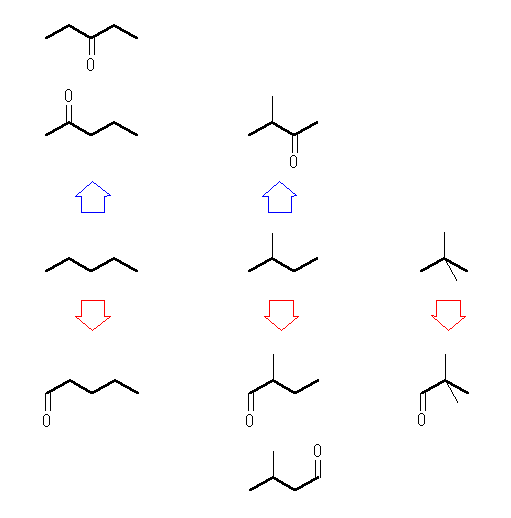
働僩儞乮惵栴報懁乯丂嵍 pentan-3-one,
pentan-2-one,
拞 3-methylbutan-2-one
傾儖僨僸僪乮愒栴報懁乯丂嵍 pentanal,
拞 2-methylbutanal,
3-methylbutanal,
塃 2,2-dimethylpropanal
(e) 埲壓偺係捠傝丅
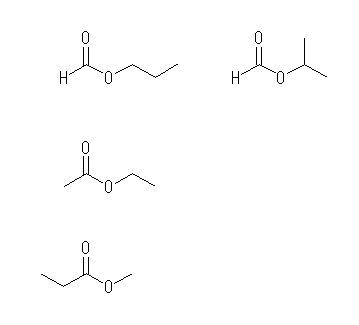
忋抜丂儊僞儞巁乮methanoic acid乯丄姷梡柤丗僊巁乮formic acid乯偺僄僗僥儖丅
嵍偐傜丄propyl formate,
isopropyl formate
拞抜丂僄僞儞巁乮ethanoic acid)丄姷梡柤丗恷巁乮acetic acid乯偺僄僗僥儖丅
ethyl acetate
壓抜丂僾儘僷儞巁乮propanoic acid乯丄姷梡柤丗僾儘僺僆儞巁乮propionic acid乯偺僄僗僥儖丅
methyl propionate
3.29
(a), (b), (c) 偦傟偧傟丄戞侾媺丄戞俁媺丄戞俀媺扽慺偵悈巁婎丄僔傾僲婎丄僗儖僼傽僯儖婎乮儊儖僇僾僩婎丄僠僆乕儖婎乯偑寢崌偟偨暘巕傪昤偔丅偙傟傜偺抲姺婎偼杮幙揑偵侾杮偺寢崌偵懳偟偰抲姺偡傞傕偺偱偁傝丄傾儈儞椶偵偍偗傞拏慺偲偼堎側傞丅偙偺偨傔丄3.31 (b) 偺僸儞僩偵偱偰偒偨傛偆偵丄戞壗媺偺傾儈儞偲偄偆昞尰偺応崌偱偼丄媺偺巊偄偐偨偑庒姳堎側傞偺偱拲堄偡傞偙偲丅
(d) 乽戞侾媺傾儖僐乕儖偱偁傝丄摨帪偵戞俀媺傾儖僐乕儖偱偁傞乿傛偆側暘巕偼丄嵟掅偱傕俀偮埲忋偺悈巁婎傪帩偨側偗傟偽側傜側偄丅
(e) 僀僜僾儘僺儖婎乮暘巬傾儖僉儖婎偺堦偮偺姷梡柤乯偺峔憿偵偮偄偰偼丄嫵壢彂偺87儁乕僕傪嶲徠偡傞偙偲丅3.10 (b) 傕嶲峫偵偣傛丅傕偪傠傫偙偪傜偺栤偄偱偼丄傾儖僇儞偱側偔懠偺姱擻婎傪暪偣帩偭偰偄偰傕椙偄丅偲偼偄偊丄僀僜僾儘僺儖婎偺峔憿偺忋偵峏偵傛偗偄側抲姺婎傪晅偗偨応崌偵偼乽僀僜僾儘僺儖婎乿偱偼側偔側傞偺偱拲堄偡傞偙偲丅
(f) 3.8 側偳傪嶲徠偣傛丅
乮夝摎椺乯
忦審偵崌抳偡傞峔憿偼柍尷偵偁傞偐傜丄埲壓丄偄偔偮偐偺椺偺傒傪帵偟偰偄傞丅
(a) 悈巁婎偑丄戞侾媺扽慺偵寢崌偟偰偄傞傛偆側傕偺丅
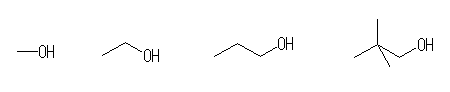
methanol,
ethanol,
propanol,
2,2-dimethyl-1-propanol
(b) 僔傾僲婎偑丄戞俁媺扽慺偵寢崌偟偰偄傞傛偆側傕偺丅
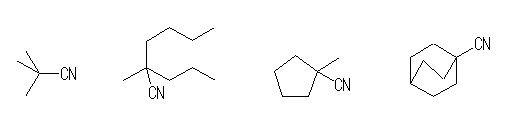
2,2-dimethylpropanenitrile,
2-methyl-2-propylhexanenitrile,
(c) 僗儖僼傽僯儖婎乮儊儖僇僾僩婎丄僠僆乕儖婎丄亅SH乯偑丄戞俀媺扽慺偵寢崌偟偰偄傞傛偆側傕偺丅
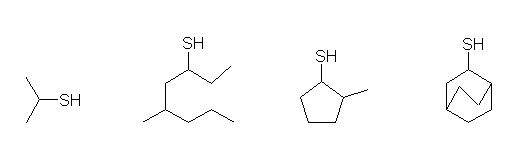
propane-2-thiol,
5-methyloctane-3-thiol,
2-methylcyclopentane-1-thiol,
bicyclo[2.2.2]octane-2-thiol
(d) 俀偮乮埲忋乯偺悈巁婎偑偁傝丄偦傟偧傟戞侾媺偍傛傃戞俀媺扽慺偵寢崌偟偰偄傞傛偆側傕偺丅
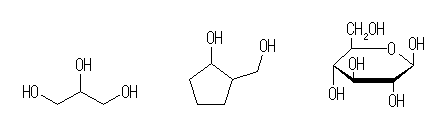
1,2,3-propanetriol (glycerol),
2-hydroxymethyl-1-cyclopentanol,
glucose
(e) 壔崌暔拞偺柤徧拞偵僀僜僾儘僺儖婎偑娷傑傟傞偨傔偵偼丄埲壓偺忦審傪枮偨偡昁梫偑偁傞丅僀僜僾儘僺儖婎乮扽慺悢俁乯偑丄偦傟偲扽慺悢偑摨偠偐丄偦傟傛傝戝偒偄扽慺悢偺僔僋儘傾儖僇儞偵寢崌偟偨傕偺丅傑偨偼丄朏崄娐側偳偵寢崌偟偨傕偺丅傾儈儞偺拏慺忋偵僀僜僾儘僺儖婎偑偁傞応崌傕偁傝偆傞丅
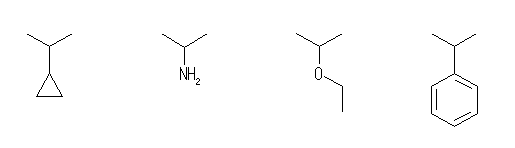
isopropylcyclopropane,
isopropylamine,
ethyl isopropyl ether,
isopropylbenzene
傾儖僇儞偺堦晹偲偟偰僀僜僾儘僺儖婎偺峔憿傪帩偮応崌偼丄庡嵔偺慖傃曽偵傛傝柤徧拞偵僀僜僾儘僺儖婎偑娷傑傟側偄応崌傕惗偠傞偺偱丄柦柤婯懃傪嶲徠偡傞偙偲丅
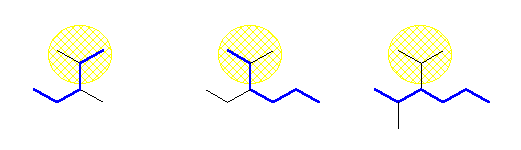
2,3-dimethylpentane,
3-ethyl-2-methylhexane,
3-isopropyl-2-methylhexane
(f) 戞係媺扽慺傪侾偮埲忋娷傓傕偺丅
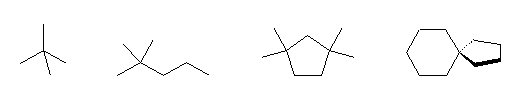
2,2-dimethylpropane,
2,2-dimethylpentane,
3.30
乽儁儞僞儞偺儌僲僽儘儌懱乿傪尩枾偵撉傒丄儁儞僞儞 n-C5H12 偺擟堄偺堦偮偺悈慺傪廘慺偵抲姺偟偨傕偺丄偲偡傞側傜偽丄俁庬椶偑懚嵼偡傞丅 傕偟曣妀傪 n-C5H12 偺崪奿堎惈懱傕娷傓傕偺偲偡傞側傜偽丄峏偵俆庬椶偺堎惈懱偑懚嵼偡傞丅
柦柤偼丄嫵壢彂 pp83-86 偺傾儖僇儞偺柦柤朄偵廬偆丅偨偩偟丄抜奒俁乽抲姺婎傪傒偮偗偰斣崋傪偮偗傞乿丄抜奒係乽柤慜傪侾岅偱彂偔乮偨傔偵傾儖僼傽儀僢僩弴偵暲傋傞乯乿偵偍偄偰丄僴儘僎儞抲姺婎乮婎杮揑偵偼丄愙摢岅偲偟偰柦柤偡傞偡傋偰偺抲姺婎乯偼傾儖僉儖婎偲摨條偵埖偆丅
乮夝摎椺乯
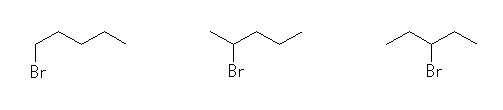
1-bromopentane,
2-bromopentane,
3-bromopentane
偙傟埲奜偺 C5H11Br
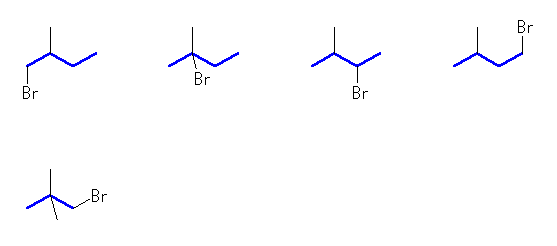
1-bromo-2-methylbutane,
2-bromo-2-methylbutane,
2-bromo-3-methylbutane,
1-bromo-3-methylbutane,
1-bromo-2,2-dimethylpropane
3.31-3.40
3.31
3.30 偲摨條偵峫偊傛丅俁庬椶偑懚嵼偡傞丅
乮夝摎椺乯
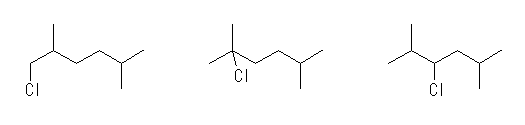
1-chloro-2,5-dimethylhexane,
2-chloro-2,5-dimethylhexane,
3-chloro-2,5-dimethylhexane
4-chloro-2,5-dimethylhexane 偼丄3-chloro-2,5-dimethylhexane 偲摨堦暔偱偁傞偐傜嬫暿偱偒側偄丅乮乽4-chloro-2,5-dimethylhexane乿偲偄偆柦柤偼岆傝丅乯
摨條偵丄5-chloro-2,5-dimethylhexane 偼 2-chloro-2,5-dimethylhexane 偲偡傞偺偑惓偟偄丅傑偨丄6-chloro-2,5-dimethylhexane 偼 1-chloro-2,5-dimethylhexane 偲偡傞偺偑惓偟偄丅偟偨偑偭偰丄忋恾偺俁庬椶偺傒偑栤戣偺忦審傪枮偨偡傕偺偱偁傞丅
3.32
扽慺偺崿惉忬懺傪峫偊傞忋偱偼丄拲栚偟偰偄傞扽慺偵懳偟丄扽慺傗悈慺埲奜偺巁慺傗拏慺偑寢崌偟偰偄傞応崌偱傕摨偠傛偆偵峫偊傞丅傕偟偙偙偱傑偩濨枂偝偑巆偭偰偄傞側傜丄 1.20 側偳傪傕偆堦搙嶲徠偡傞偙偲丅
偙偺栤偄偱梌偊傜傟偰偄傞偺偼丄姱擻婎偱偼側偔丄偁傞姱擻婎傪傕偮壔崌暔偺堦斒柤偱偁傞丅
働僩儞婎乮傕偟偔偼椉懁偵傾儖僉儖婎偺寢崌偟偨僇儖儃僯儖婎乯傪帩偮傕偺偑働僩儞偱偁傝丄僔傾僲婎傪帩偮傕偺偑僯僩儕儖丄偦偟偰丄僇儖儃僉僔婎傪帩偮傕偺偑僇儖儃儞巁偱偁傞丅
乮夝摎椺乯
(a) sp2 (b) sp (c) sp2
3.33
(a) 梌偊傜傟偨暘巕幃丄忦審暥偵崌抳偡傞峔憿堎惈懱偼慡晹偱俆庬椶懚嵼偡傞丅偦偺拞偱乽價傾僙僠儖乿偺柤徧偵憡摉偡傞傕偺偼桞侾偮偱偁傞丅乽價乿偼攞悢愙摢岅偱偁傝丄乽傾僙僠儖 acetyl 乿偼丄恷巁乮 acetic acid 乯偐傜攈惗偟偨偁傞晹暘峔憿偵懳偡傞柤徧偱偁傞丅偙傟傛傝椶悇偣傛丅
(b) 偙偺暘巕幃偲乽懡廳寢崌傪傕偨側偄乿偲偄偆忦審暥傛傝丄奩摉偡傞峔憿偼桞堦偮偵寛傔傞偙偲偑偱偒傞丅乮敪揥乯偺崁傕嶲徠偺偙偲丅
(c) 梌偊傜傟偨暘巕幃偍傛傃忦審暥傛傝丄奩摉偡傞峔憿偼桞堦偮偵寛傔傞偙偲偑偱偒傞丅
乮夝摎椺乯
(a) 娐傗扽慺亅扽慺懡廳寢崌傪帩偨側偄偺偩偐傜丄扽慺亅巁慺擇廳寢崌偑暘巕撪偵俀偮偁傞丅偙偺傛偆側忦審偵崌偆偺偼丄師偺俆庬偺峔憿丅
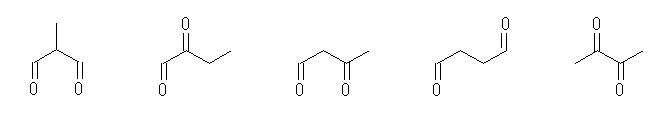
2-methylpropanedial,
2-oxobutanal,
3-oxobutanal,
butanedial,
butane-2,3-dione
偙偺偆偪丄乽價傾僙僠儖, biacetyl乿乮姷梡柤乯偼丄塃抂偺butane-2,3-dione 偱偁傞丅
恷巁乮acetic acid)偐傜桿摫偝傟傞抲姺婎偲偟偰丄傾僙僠儖婎 CH3C(=O)- 偑偁傞偑丄偙傟偑俀偮岦偐偄偁偭偰晅偄偨峔憿傪帩偭偰偄傞偙偲偑柤徧偺桼棃偱偁傞丅
(b) 暘巕幃傛傝晄朞榓搙偼侾丅懡廳寢崌偑側偄偺偩偐傜丄娐峔憿傪侾偮帩偮偙偲偑敾傞丅懡壙偺尦慺偼丄扽慺偲拏慺偱暪偣偰俁偮偩偐傜俁堳娐偱偁傞丅
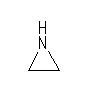
(c) 梌偊傜傟偨暘巕幃傛傝丄晄朞榓搙偼侽丅暘巕撪偵懡廳寢崌傗娐峔憿偼帩偨側偄丅傑偨丄偦傟偧傟偺扽慺偵懳偟悈巁婎偑偁傞偲偄偆偙偲偐傜丄俁偮偺巁慺偼偡傋偰悈巁婎傪峔惉偟丄僄乕僥儖寢崌傕帩偨側偄丅偙偺偨傔丄僾儘僷儞傪曣懱偲偟偨師偺峔憿偱偁傞偙偲偑敾傞丅
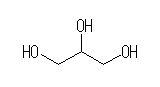
乮敪揥乯
(b) -NH2 偼傾儈僲婎偱丄偙傟傪帩偮壔崌暔偼傾儈儞偱偁傞丅扽慺亅拏慺娫偑擇廳寢崌偲側偭偨=NH 偼僀儈僲婎偱丄偙傟傪帩偮壔崌暔偼僀儈儞偱偁傞丅傑偨丄堎側傞俀偮偺扽慺傪壦嫶偡傞 -NH- 傕丄僀儈僲乮 imino 乯傑偨偼僄僺僀儈僲乮 epimino 乯偱柦柤偟偰傕傛偄丅
3.34
傕偟傑偩偙傟傜偺峔憿幃傪昤偔偙偲偑偱偒側偄側傜丄傾儖僇儞偺柦柤朄傪傕偆堦搙暅廗偟偰傒傞偙偲丅
乮夝摎椺乯
(a) 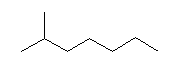
(b) 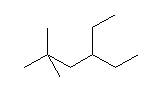
(c) 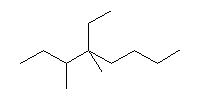
(d) 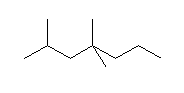
(e) 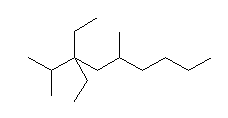
(f) 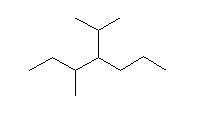
3.35
3.8 乣 3.10 側偳傪嶲徠偺偙偲丅
乮夝摎椺乯
悢椺偺傒傪帵偡丅
(a) 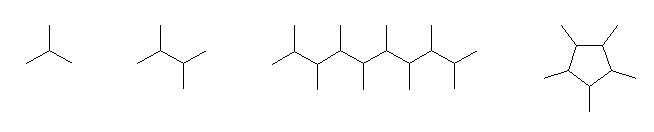
2-methylpropane,
2,3-dimethylbutane,
2,3,4,5,6,7,8,9-octamethyldecane,
1,2,3,4,5-pentamethylcyclopentane
(b)
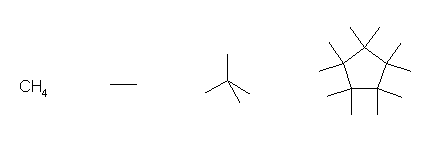
methane,
ethane,
2,2-dimethylpropane,
1,1,2,2,3,3,4,4,5,5-decamethylcyclopentane
(c) 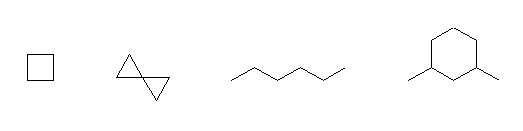
cyclobutane,
spirobicyclopropane,
hexane,
1,3-dimethylcyclohexane
3.36
戞侾媺扽慺偵寢崌偟偨悈慺傪戞侾媺悈慺丄戞俀媺扽慺偵寢崌偟偨悈慺傪戞俀媺悈慺丄戞俁媺扽慺偵寢崌偟偨悈慺傪戞俁媺悈慺偲屇傇丅
乮夝摎椺乯
(a) 戞侾媺悈慺偲偼丄戞侾媺扽慺偵寢崌偟偨悈慺側偺偱丄-CH3 偺偙偲偱偁傞偐傜丄儊僠儖婎側偳丄崪奿偺枛抂扽慺傪俁偮傕偮壔崌暔傪彂偗偽傛偄丅
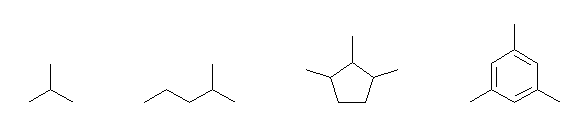
2-methylpropane,
2-methylpentane,
1,2,3-trimethylcyclopentane,
1,3,5-trimethylbenzene
(b) 扽慺偲悈慺偺傒偐傜側傞朞榓壔崌暔偵偮偄偰峫偊傞偲丄戞俀媺扽慺丄戞俁媺扽慺偵偼悈慺偑寢崌偟偰偄傞偙偲偵側傞偐傜丄戞侾媺扽慺丄戞係媺扽慺偺傒偐傜側傞傛偆側峔憿傪峫偊傟偽傛偄丅傑偨偼丄戞俀媺扽慺丄戞俁媺扽慺偺悈慺傪僴儘僎儞側偳揔摉側抲姺婎偱抲偒姺偊偨傕偺偱傕丄忦審傪枮偨偡偙偲偵側傞丅
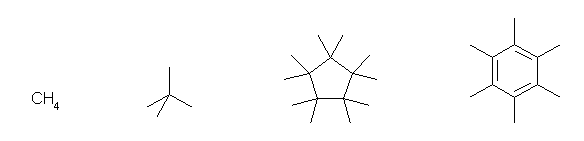
methane,
2,2-dimethylpropane,
1,1,2,2,3,3,4,4,5,5-decamethylcyclopentane
1,2,3,4,5,6-hexamethylbenzene
3.37
堎惈懱摨巑偱偼丄乮懡廳寢崌偺悢 亄 娐偺悢乯偑堦掕偱偁傞丅偟偨偑偭偰丄傾儖僉儖婎偺暘巬偺巇曽偺堘偄偵傛傞崪奿堎惈懱傗丄姱擻婎偺埵抲偺堘偄偵傛傞埵抲堎惈懱傪扵偡丅
(e) 偱偼丄乽摨偠姱擻婎乿傪捠忢捠傝偵儂儖儈儖婎乮傾儖僨僸僪婎乯偲峫偊傞偲丄奩摉偡傞夝偼懚嵼偟側偄丅姱擻婎偲偟偰僇儖儃僯儖婎傪峫偊傞乮偡側傢偪丄傾儖僨僸僪婎偲働僩儞婎傪嬫暿偟側偄乯応崌偺傒夝偑偁傝摼傞丅
乮夝摎椺乯
暋悢偺堎惈懱傪帩偮傕偺偼丄悢椺偺傒帵偟偨丅屳偄偵堎惈懱偱偁傞偨傔偵偼丄扽慺悢傪偼偠傔偲偟偰丄暘巕幃偑摨偠僨傾儖昁梫偑偁傞偺偱拲堄偡傞偙偲丅
(a) 僴儘僎儞傪姱擻婎偲偟偰帩偮僴儘傾儖僇儞偵偮偄偰峫偊傞丅埵抲堎惈懱偲偟偰偼丄師偺俁偮丅
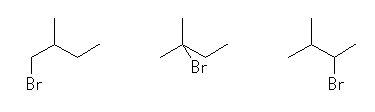
1-bromo-2-methylbutane,
2-bromo-2-methylbutane,
2-bromo-3-methylbutane
偦偺懠偺崪奿堎惈懱偑懡庬偁傝丅
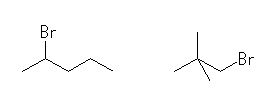
2-bromopentane,
1-bromo-2,2-dimethylpropane
(b) 僄乕僥儖寢崌傪帩偮僔僋儘傾儖僇儞傪峫偊傞丅
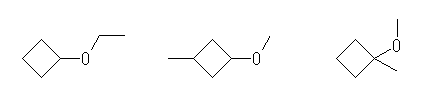
ethoxycyclobutane,
1-methoxy-3-methylcyclobutane,
1-methoxy-1-methylcyclobutane
(c) 僔傾僲婎偺埵抲堎惈懱偼丄師偺侾庬偺傒偑懚嵼偡傞丅
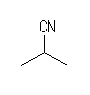
2-methylpropanenitrile
(d) 悈巁婎傪帩偮僔僋儘傾儖僇儞傪峫偊傞丅
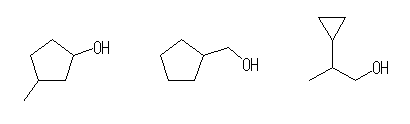
3-methylcyclopentanol,
cyclopentylmethanol,
2-cyclopropyl-1-propanol
(e) 僇儖儃僯儖婎偺埵抲堎惈懱偼師偺捠傝丅偨偩偟丄傾儖僨僸僪婎偲働僩儞婎傪嬫暿偡傞応崌偵偼丄偙傟傜偼摨偠姱擻婎傪帩偮偲偼尵偊側偄丅
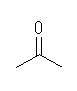
2-propanone (acetone)
(f) 僼僃僯儖婎乮朏崄娐乯傪帩偮僇儖儃儞巁偼丄師偺俁庬偑峫偊傜傟傞丅乮偙傟傜偼屳偄偵儊僠儖婎偺埵抲堎惈懱偱偁傞丅乯
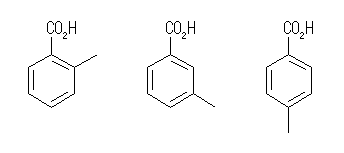
2-methylbenzoic acid (o-toluic acid),
3-methylbenzoic acid,
4-methylbenzoic acid
3.38
傾儖僇儞偺柦柤朄乮嫵壢彂 3.4 愡乯傪嶲徠偡傞偙偲丅
乮夝摎椺乯
(a) 2-methylpentane
(b) 2,2-dimethylbutane
(c) 2,3,3-trimethylhexane
(d) 5-ethyl-2-methylheptane
(e) 3,3,5-trimethyloctane
(f) 2,2,3,3-tetramethylhexane
3.39
傑偢丄C6H14 偺偡傋偰偺乮俆庬椶偺)堎惈懱偺峔憿傪彂偄偰傒傛丅偦偺偺偪丄偦傟偧傟偵惓偟偔柤慜傪偮偗傞偙偲丅
乮夝摎椺乯
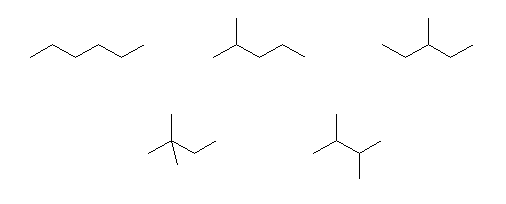
n-hexane,
2-methylpentane,
3-methylpentane,
2,2-dimethylbutane,
2,3-dimethylbutane
3.40
傑偢偼丄梌偊傜傟偨柤慜乮偑惓偟偄傕偺偲偟偰丄偦傟乯偵懳墳偡傞峔憿傪昤偄偰傒傛丅偦偺忋偱丄偦偺峔憿偵惓偟偄柤慜傪偮偗傞傛偆偵偣傛丅
(a), (b), (e) 偼丄庡嵔偺慖傃曽偵娫堘偄偑偁傞丅
(c), (d) 偼丄斣崋偺偮偗曽偵娫堘偄偑偁傞丅
乮夝摎椺乯
梌偊傜傟偨柤慜偵揧偭偨峔憿乮庡嵔傪悈暯偵昤偒丄嵍抂偐傜斣崋傪偲偭偨埵抲偵抲姺婎傪抲偄偨乯偲丄偦偺壔崌暔偺惓偟偄柤徧乮惓偟偄庡嵔偼惵慄偱帵偟偨乯傪婰偡丅
(a) 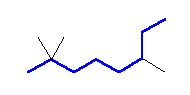
2,2,6-trimethyloctane
(b) 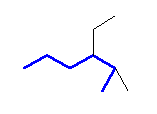
3-ethyl-2-methylhexane
(c) 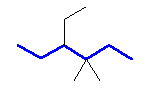
4-ethyl-3,3-dimethylhexane
(d) 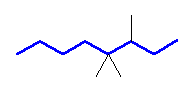
3,4,4-trimethyloctane
(e) 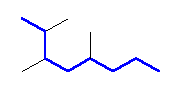
2,3,5-trimethyloctane
3.41-3.50
3.41
僄僠儖婎傗乮3-儊僠儖僽僠儖乯婎側偳偺晅偔埵抲偵拲堄偟丄堄恾偟偰偄偨傕偺偲庡嵔偑戙傢偭偰偟傑傢側偄傛偆偵偡傞偙偲丅
乮夝摎椺乯
悢椺偺傒帵偡丅
(a) 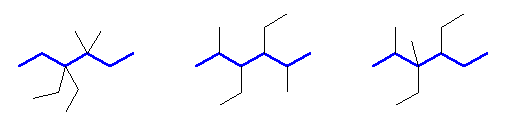
3,3-diethyl-4,4-dimethylhexane,
3,4-diethyl-2,5-dimethylhexane,
3,4-diethyl-2,3-dimethylhexane
僄僠儖婎偼丄俁埵傑偨偼係埵偺偄偢傟偐偱側偄偲丄庡嵔偑僿僉僒儞偱偼側偔側偭偰偟傑偆丅
(d) 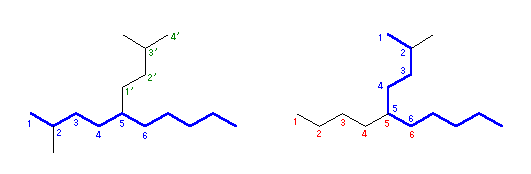
乮嵍乯 2-methyl-5-(3-methylbutyl)decane
塃偺傛偆側峔憿偱偼丄扽慺嵔偑摨偠挿偝偺帪偼暘婒偑懡偔側傞傛偆偵庡嵔傪偲傞偐傜丄5-butyl-2-methyldecane 偲側傞丅
3.42
2-methylbutane 偼丄峔憿幃偱昞偡偲丄師偺捠傝丅峔憿幃拞丄C2-C3 寢崌傪惵慄偱帵偟偨丅
(a),(b) 偹偠傟宍攝嵗偺偆偪丄棫懱揑偵戝偒側抲姺婎偳偆偟乮儊僠儖婎側偳乯偑 傾儞僠宍偵側偭偰偄傞傕偺偑堦斣埨掕丅廳側傝宍攝嵗偺偆偪丄棫懱揑偵戝偒側抲姺婎偳偆偟乮儊僠儖婎側偳乯偑廳側傞傕偺偑堦斣晄埨掕丅
(c) 栤偄偵梌偊傜傟偨悢抣偺懠偵丄嫵壢彂 93 儁乕僕 昞 3.5 傛傝丄悈慺亅悈慺偺廳側傝宍憡屳嶌梡偼 4.0 kJ/mol丄悈慺亅儊僠儖偺廳側傝宍憡屳嶌梡偼 6.0 kJ/mol偺抣傪梡偄傞丅
乮夝摎椺乯
(a) 壓偺恾偺俀庬椶偺偹偠傟宍攝嵗偑峫偊傜傟傞偑丄傛傝埨掕側偺偼嵍丅
(c) 偺傛偆側掕検揑側尒愊傕傝偵傛傝丄偙傟傜擇偮偺攝嵗偺娫偺僄僱儖僊乕嵎偼丄3.8 kJ/mol丅偙傟偼丄乮敪揥乯偱帵偟偨崻嫆偵傛傟偽丄俀偮偺攝嵗偩偗傪峫偊偨偲偟偰丄嵍偺峔憿偺傛傝埨掕側攝嵗偵偁傞暘巕偼丄塃偺偹偠傟宍攝嵗偵偁傞暘巕偺俆攞掱搙懚嵼偡傞偙偲傪帵偡丅
(b) 壓偺恾偺俀庬椶偺廳側傝宍攝嵗偑峫偊傜傟傞偑丄傛傝晄埨掕側偺偼塃丅
堦斣晄埨掕側廳側傝宍攝嵗偲堦斣埨掕側偹偠傟宍攝嵗偺僄僱儖僊乕嵎偼丄17.2 kJ/mol丅偙偺抣偼丄俀偮偺攝嵗偩偗傪峫偊偨偲偟偰丄埨掕側偹偠傟宍攝嵗偵偁傞暘巕偺悢偑丄晄埨掕側廳側傝宍攝嵗偵偁傞暘巕偺栺1000攞掱搙偱偁傞偙偲傪帵偡丅
(c) 埲壓偺傛偆偵側傞丅
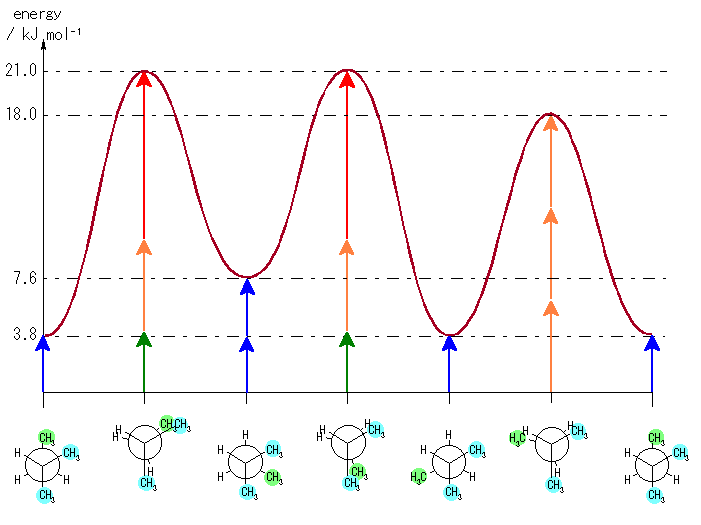
偨偩偟丄埲壓偺傛偆側僄僱儖僊乕偺尒愊傕傝偵傛傞丅
僑乕僔儏憡屳嶌梡丗
丂丂悈慺亅悈慺丂丂 0 kJ/mol
丂丂悈慺亅儊僠儖丂 0 kJ/mol
丂丂儊僠儖亅儊僠儖 3.8 kJ/mol 乮惵栴報乯
廳側傝宍憡屳嶌梡丗
丂丂悈慺亅悈慺丂丂 4.0 kJ/mol 乮椢栴報乯
丂丂悈慺亅儊僠儖丂 6.0 kJ/mol 乮烌栴報乯
丂丂儊僠儖亅儊僠儖 11.0 kJ/mol 乮愒栴報乯
乮敪揥乯
乽暔棟壔妛乿偱廗偆傛偆偵丄暲恑傗夞揮側偳偺侾帺桼搙偁偨傝偵暘攝偝傟傞僄僱儖僊乕偼 RT/2 (J/mol) 偱偁傞丅幒壏乮 T乣300 K 乯偱暘巕偺帩偮僄僱儖僊乕偺偍傛偦偺栚埨偲偟偰丄RT 傪寁嶼偡傞偲丄偍傛偦 2.5 kJ/mol 偲側傞丅
堦曽丄儃儖僣儅儞暘晍偵傛傞偲丄僄僱儖僊乕嵎 ΔE 偺俀偮偺忬懺娫偺愯桳搙偺斾偼 e亅(ΔE / RT)偱梌偊傜傟傞丅乮 e亅(ΔE / RT) 偼丄偟偽偟偽丄exp(亅(ΔE / RT)) 偲偄偆昞婰朄偱彂偐傟傞丅乯
偡側傢偪丄僄僱儖僊乕嵎偑 2.5 kJ/mol 偱偁傞傛偆側擇偮偺忬懺偺娫偱暯峵偑惉棫偟偰偄傞側傜丄忋偺忬懺偵偼壓偺忬懺偵斾傋偰 1/e 攞偟偐暘晍偟側偄偙偲傪帵偡丅偙偺偲偒丄慡懱偵懳偡傞愯桳棪偼
僄僱儖僊乕嵎偑 2.5 kJ/mol偺偲偒丄乮1/(1+e)亖乯27%丅
乮 5.0 kJ/mol 偱偼丄1/e2 攞乮12%乯丄
7.5 kJ/mol 偱偼丄1/e3 攞(4.7%)丄
10.0 kJ/mol 偱偼丄1/e4 攞(1.8%)丄
12.5 kJ/mol 偱偼丄1/e5 攞(0.67%乯丄
15.0 kJ/mol 偱偼丄1/e6 攞(0.25%乯丄
17.5 kJ/mol 偱偼丄1/e7 攞(0.091%乯丄
20.0 kJ/mol 偱偼丄1/e8 攞(0.034%乯丄
22.5 kJ/mol 偱偼丄1/e9 攞(0.012%乯丄
25.0 kJ/mol 偱偼丄1/e10 攞(0.0045%乯偲側傞丅乯
嶲徠 嫵壢彂p90乮壓偐傜係峴栚偐傜壓偐傜俁峴栚乯
偙傟傪丄僄僞儞偺廳側傝宍攝嵗偵偄傞暘巕偺妱崌傪媮傔傞偺偵巊梡偟偰傒傞丅偹偠傟宍攝嵗偲廳側傝宍攝嵗偱偼丄12.0 kJ/mol 偺僄僱儖僊乕嵎偑偁傞偺偱丄偦偺懚嵼搙偺斾偼丄 e(12 / 2.5) : 1 偲側傞偐傜丄慡暘巕拞偺廳側傝宍攝嵗偺悢傪媮傔傞乮偙偺俀偮偟偐攝嵗偑懚嵼偟側偄傕偺偲偟偰乯寁嶼幃偼丄1 / (1 + (e(12 / 2.5))) 偲側傝丄偙傟傪寁嶼偡傞偲丄0.008162 偱丄栺 0.82 % 偲側傞丅乮嫵壢彂偺婰弎偵堦抳偡傞丅乯
埲忋偺媍榑傪尦偵偟偰丄嫵壢彂p94乮拲堄揰乯傪撉傒丄偦偺堄枴傪棟夝偡傞偙偲丅
3.43
乮僸儞僩乯僑乕僔儏憡屳嶌梡丗
丂丂悈慺亅悈慺丂丂 0 kJ/mol
丂丂悈慺亅儊僠儖丂 0 kJ/mol
丂丂儊僠儖亅儊僠儖 3.8 kJ/mol
傪梡偄傞丅
乮夝摎椺乯
2,3-dimethylbytadiene 偺峔憿偼丄埲壓偺捠傝丅
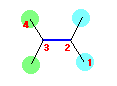
廬偭偰丄埲壓偺俁偮偺偹偠傟宍攝嵗偑壜擻偱偁傞丅
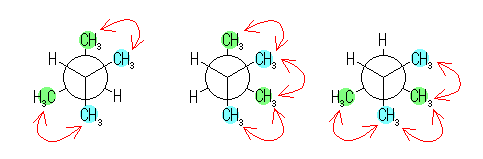
偙偺偆偪丄嵍偺傕偺乮俀偮偺悈慺偑傾儞僠宍偵偁傞傕偺乯偱偼丄儊僠儖亅儊僠儖偺僑乕僔儏憡屳嶌梡偑俀偮偱偁傞偺偵懳偟丄巆傝偺擇偮乮俀偮偺悈慺偑僑乕僔儏宍偵偁傞傕偺乯偱偼丄儊僠儖亅儊僠儖偺僑乕僔儏憡屳嶌梡偑俁偮偁傞丅偟偨偑偭偰丄偙傟傜偺娫偺僄僱儖僊乕嵎偼丄3.8 kJ/mol 偱偁傞丅
側偍丄栤偄 3.42 偲摨條偵掕検揑側僄僱儖僊乕恾傪昤偔偲丄埲壓偺傛偆偵側傞丅
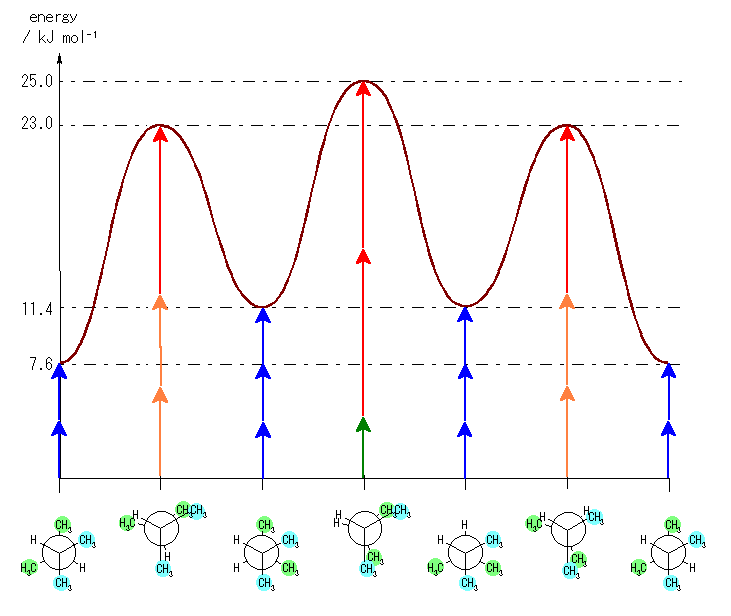
偨偩偟丄埲壓偺傛偆側僄僱儖僊乕偺尒愊傕傝偵傛傞丅
僑乕僔儏憡屳嶌梡丗
丂丂悈慺亅悈慺丂丂 0 kJ/mol
丂丂悈慺亅儊僠儖丂 0 kJ/mol
丂丂儊僠儖亅儊僠儖 3.8 kJ/mol 乮惵栴報乯
廳側傝宍憡屳嶌梡丗
丂丂悈慺亅悈慺丂丂 4.0 kJ/mol 乮椢栴報乯
丂丂悈慺亅儊僠儖丂 6.0 kJ/mol 乮烌栴報乯
丂丂儊僠儖亅儊僠儖 11.0 kJ/mol 乮愒栴報乯
3.44
乽掕惈揑乿偵嶌恾偱偒傟偽椙偄偐傜丄僄僱儖僊乕偺愨懳抣乮廲幉偺抣乯偼媮傔側偔偰傕傛偄丅乮偨偩偟丄偄偄壛尭偱偼偄偗側偄丅摨偠抣偵側傞傋偒偲偙傠偼崅偝傪懙偊傞側偳偵婥傪偮偗傞丅乯
1,2-dibromoethane 偺廘慺傪儊僠儖婎偵抲姺偟偨傕偺偼丄n-butane 偱偁傞偐傜丄1,2-dibromoethane 偺 C-C 寢崌幉偺夞揮偵娭偡傞僄僱儖僊乕偲丄n-butane 偺 C2-C3 寢崌幉偺夞揮偵娭偡傞僄僱儖僊乕乮嫵壢彂 p94 恾 3.9乯偼摨偠傛偆側娭學傪帩偮偼偢偱偁傞丅
側偍丄栤戣 3.46 偺栤戣暥偵梌偊傜傟偨抣偲丄嫵壢彂 p92丄恾 3.8 偺 peopane 偺僄僱儖僊乕傪斾妑偡傞偙偲偵傛傝丄1,2-dibromoethane 偺僄僱儖僊乕傪丄偁傞掱搙丄掕検揑偵尒愊傕傞偙偲偑壜擻偲側傞丅
乮夝摎椺乯
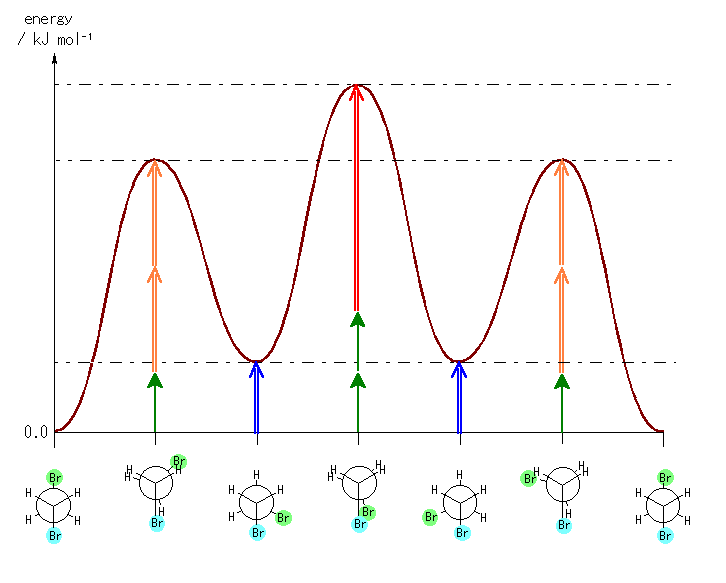
偨偩偟丄埲壓偺傛偆側僄僱儖僊乕偺尒愊傕傝偵傛傞丅
僑乕僔儏憡屳嶌梡丗
丂丂悈慺亅悈慺 0 kJ/mol
丂丂悈慺亅廘慺 0 kJ/mol
丂丂廘慺亅廘慺 乮惵栴報乯
廳側傝宍憡屳嶌梡丗
丂丂悈慺亅悈慺 乮椢栴報乯 4.0 kJ/mol
丂丂悈慺亅廘慺 乮烌栴報乯 7.0 kJ/mol 仼 栤戣 3.46 傛傝
丂丂廘慺亅廘慺 乮愒栴報乯
偙偙偱丄偍傛偦偺戝偒偝偼丄n-butane 偺 C2-C3 寢崌幉偺夞揮偵娭偡傞僄僱儖僊乕乮壓恾乯傪嶲徠偲偟偨丅
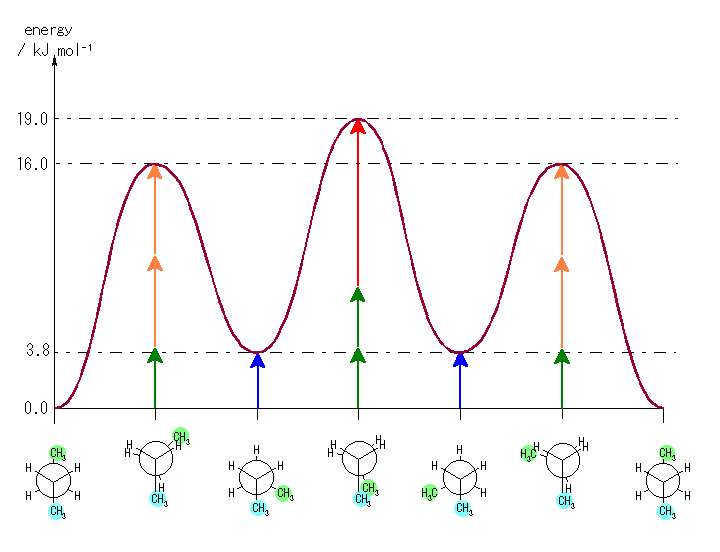
偨偩偟丄埲壓偺傛偆側僄僱儖僊乕偺尒愊傕傝偵傛傞丅
僑乕僔儏憡屳嶌梡丗
丂丂悈慺亅悈慺丂丂 0 kJ/mol
丂丂悈慺亅儊僠儖丂 0 kJ/mol
丂丂儊僠儖亅儊僠儖 3.8 kJ/mol 乮惵栴報乯
廳側傝宍憡屳嶌梡丗
丂丂悈慺亅悈慺丂丂 4.0 kJ/mol 乮椢栴報乯
丂丂悈慺亅儊僠儖丂 6.0 kJ/mol 乮烌栴報乯
丂丂儊僠儖亅儊僠儖 11.0 kJ/mol 乮愒栴報乯
3.45
暘巕偺帩偮憃嬌巕儌乕儊儞僩偼丄奺寢崌偺帩偮暘嬌偺儀僋僩儖榓偱偁傞丅傑偨丄憃嬌巕儌乕儊儞僩偵偮偄偰偼丄嫵壢彂偺俀復俀愡傪嶲徠偡傞偙偲丅側偍丄僋儘儘儊僞儞乮H3C-Cl乯偺憃嬌巕儌乕儊儞僩偼丄幚應抣偲偟偰 1.87 D 偱偁傞乮嫵壢彂 倫39丄昞 2.1乯丅
乮夝摎椺乯
暘巕偺憃嬌巕儌乕儊儞僩偼丄條乆側攝嵗傪偲偭偰偄傞暘巕偑丄偦傟偧傟偺峔憿偵墳偠偰帵偡抣偺暯嬒偲側傞偲峫偊傜傟傞丅
1,2-僕僽儘僄僞儞偑偲傞攝嵗偺偆偪偱丄堦斣埨掕側傕偺偼丄俀偮偺廘慺偑傾儞僠偲側傞棫懱攝嵗偱偁傞丅偙偺傾儞僠宍攝嵗偐傜梊應偝傟傞暘巕偺憃嬌巕儌乕儊儞僩偼僛儘偲側傞偐傜丄傕偟偡傋偰偺暘巕偑偙偺攝嵗傪偲偭偰偄傞偲偡傟偽丄娤應偝傟傞憃嬌巕儌乕儊儞僩傕僛儘偲側傞偼偢偱偁傞丅偲偙傠偑丄幚尡揑偵 μ = 1.0 D 偺憃嬌巕儌乕儊儞僩偑娤應偝傟偰偄傞帠幚傛傝丄憃嬌巕儌乕儊儞僩偑僛儘偱偼側偄攝嵗傪偲傞暘巕偑偁傞偙偲偑傢偐傞丅
嵟戝偺憃嬌巕儌乕儊儞僩傪帩偮棫懱攝嵗偼丄俀偮偺廘慺偑廳側傝宍傪偲傞傕偺偱偁傞偑丄偙傟偼偐側傝晄埨掕側偺偱丄傎偲傫偳懚嵼偟側偄丅乮壓偺夝愅偱帵偡傛偆偵丄廳側傝宆攝嵗偼丄偡傋偰暪偣偰傕0.15亾掱搙偟偐側偄丅乯
俀偮偺廘慺偑僑乕僔儏偲側傞棫懱攝嵗傕丄憃嬌巕儌乕儊儞僩傪傕偮丅偙傟偑桳堄側検乮壓偺夝愅偱帵偡傛偆偵丄偍傛偦20亾嫮丅乯懚嵼偟偰偍傝丄暘巕偺憃嬌巕儌乕儊儞僩偵婑梌偟偰偄傞偲峫偊傜傟傞丅
乮埲壓丄傗傗徻偟偄夝愅偲夝愢丅乯
1,2-dibromoethane 偺偦傟偧傟偺夞揮攝嵗偵懳墳偡傞憃嬌巕儌乕儊儞僩偺曽岦傪栴報偱彂偒崬傫偩丅傑偨丄偙傟傜偺攝嵗偺僄僱儖僊乕偺掕検揑側庢傝埖偄偲丄偙傟偵婎偯偄偨偦傟偧傟偺攝嵗偺婑梌偺掕検揑側媍榑偼丄埲壓偺傛偆偵側傞丅
恾偺壓偺悢抣偼丄儃儖僣儅儞暘晍傛傝梊應偝傟傞憡懳揑側懚嵼搙丅乮Newman 搳塭幃偺壓偺俁峴偼丄忋傛傝丄寁嶼幃丄寁嶼寢壥悢抣丄偍傛傃寁嶼寢壥悢抣傪亾偱昞偟偨傕偺丅乯
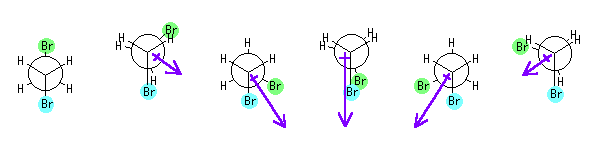
| ||||||||||
| 1 | : | 1/e(18/2.5) | : | 1/e(5/2.5) | : | 1/e(20/2.5) | : | 1/e(5/2.5) | : | 1/e(18/2.5) |
| 1 | : | 0.00075 | : | 0.135 | : | 0.00034 | : | 0.135 | : | 0.00075 |
| 78.6 % | : | 0.06 % | : | 10.6 % | : | 0.03 % | : | 10.6 % | : | 0.06 % |
恾嵍抂丄堦斣埨掕側偹偠傟宍攝嵗偱偼廘慺摨巑偑傾儞僠攝嵗傪偲偭偰偍傝丄扽慺亅廘慺偺暘嬌偼屳偄偵懪偪徚偟崌偆偨傔丄暘巕偼憃嬌巕儌乕儊儞僩傪帩偨側偄丅
嵍傛傝俀斣栚丄俀慻偺廘慺偲悈慺偑廳側傝宍偲側傞攝嵗偱偼丄暘巕偼丄扽慺亅廘慺偺暘嬌偲摨掱搙偺憃嬌巕儌乕儊儞僩傪帩偮丅傑偨丄4.28 偺栤戣傛傝丄悈慺亅廘慺偺廳側傝宍憡屳嶌梡偺戝偒偝偑 7.0 kJ/mol 偲媮傑傞乮悈慺亅儊僠儖偺廳側傝宍憡屳嶌梡偱偼 6.0 kJ/mol 偱偁偭偨偙偲傪峫偊傞偲丄廘慺偺曽偑儊僠儖婎傛傝丄彮偟戝偒偄偲峫偊傜傟傞乯偺偱丄偙傟偵婎偯偗偽丄18 kJ/mol 偺僄僱儖僊乕偱偁傞偙偲偵側傞丅偟偨偑偭偰丄乮忋恾丄堦斣塃偺夞揮堎惈懱 僐儞僼僅儅乕偲偁傢偣偰乯0.18% 掱搙偺婑梌偟偐側偄丅[ 寁嶼幃 : 0.00075*2 / (1 + 0.135*2 + 0.00075*2 + 0.00034) = 0.0018 ] 乯丅
嵍傛傝俁斣栚丄廘慺偲廘慺偑僑乕僔儏偵側傞攝嵗偼丄扽慺亅廘慺偺暘嬌偺 1.7 攞掱搙偺憃嬌巕儌乕儊儞僩傪帩偮丅n-butane 偐傜偺椶悇傛傝丄5 kJ/mol 掱搙偺僄僱儖僊乕偱偁傞偲壖掕偟偰乮忋恾丄塃偐傜俀斣栚偺夞揮堎惈懱 僐儞僼僅儅乕偲偁傢偣偰乯 21% 掱搙偺婑梌偑偁傞偙偲偵側傞丅[ 寁嶼幃 : 0.135 * 2 / (1 + 0.135*2 + 0.00075*2 + 0.00034) = 0.212 ] 丅
廘慺偲廘慺偑廳側傝宍偲側傞攝嵗偱偼丄憃嬌巕儌乕儊儞僩偼嵟戝偲側傝丄扽慺亅廘慺偺暘嬌偺 2 攞掱搙偲側傞丅偙偺攝嵗偼丄n-butane 偐傜偺椶悇傛傝丄彮側偔偲傕20 kJ/mol 掱搙偺晄埨掕側攝嵗偱偁傞偲壖掕偡傞偲丄0.03% 枹枮偺婑梌偟偐側偄偲峫偊傜傟傞丅[ 寁嶼幃 : 0.00034 / (1 + 0.135*2 + 0.00075*2 + 0.00034) = 0.00027 ]乯
3.46
嫵壢彂 p91乣92丄僾儘僷儞偺棫懱攝嵗嶲徠丅悈慺亅悈慺偺廳側傝宍憡屳嶌梡偼丄僄僞儞偺廳側傝宍攝嵗偺僄僱儖僊乕偐傜偺峫嶡偵傛傝丄侾売強偁偨傝丄4.0 kJ/mol 偱偁傞丅乮嫵壢彂p93 昞3.5乯丅
乮夝摎椺乯
(a) 7.0 kJ/mol 乵 寁嶼幃 : 15.0 亅 (4.0 亊 2) = 7.0 乶
(b) 埲壓偺捠傝丅
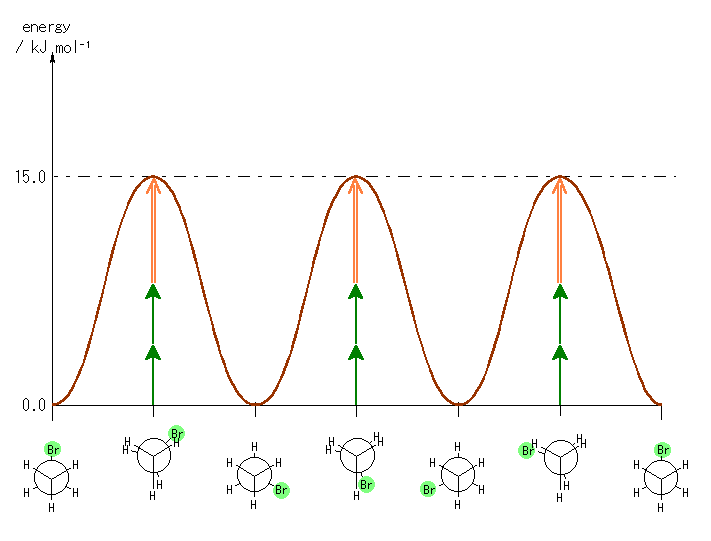
3.47
嫵壢彂 p94丄侾峴栚傛傝
乽偳偺傾儖僇儞偵偍偄偰傕丄嵟傕埨掕側攝嵗偼丄偡傋偰偺俠亅俠寢崌偑偹偠傟宆偱丄戝偒側抲姺婎乮拲栚偟偰偄傞俠亅俠寢崌偐傜偱偰偄傞傾儖僉儖婎乯偑屳偄偵傾儞僠偵攝楍偡傞傕偺偱偁傞丅乿
乮夝摎椺乯
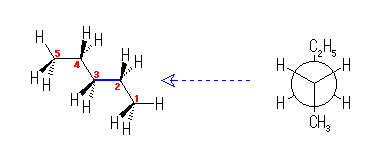
嵍恾偺傛偆偵丄偡傋偰偺扽慺偑捈慄揑偵怢傃偨棫懱攝嵗傪偲傞丅偙偺偲偒丄C2-C3 寢崌幉偵偦偭偨 Newman 搳塭恾乮塃恾乯傪尒傞偲丄戝偒側抲姺婎偱偁傞庤慜偺儊僠儖婎乮C1乯偲岦偙偆懁偺僄僠儖婎乮C4-C5乯偑屳偄偵傾儞僠偵側偭偨偹偠傟宍傪偲偭偰偄傞偙偲偑傢偐傞丅
3.48
栤偄 3.47 偲摨條偵峫偊傞丅C1-C2 寢崌偵偮偄偰尒偨応崌丄戝偒側抲姺婎乮墫慺偲傾儖僉儖婎乯偑屳偄偵傾儞僠偵攝楍偡傞傛偆側攝嵗偑埨掕偱偁傞丅
乮夝摎椺乯
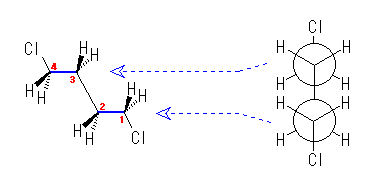
嵍恾偺傛偆偵丄偡傋偰偺扽慺偲俀偮偺墫慺偑捈慄揑偵怢傃偨棫懱攝嵗傪偲傞丅偙偺偲偒丄C1-C2 寢崌幉丄偍傛傃C3-C4 寢崌幉偵偦偭偨 Newman 搳塭恾乮塃恾乯傪尒傞偲丄戝偒側抲姺婎偱偁傞墫慺偲傾儖僉儖婎偑屳偄偵傾儞僠偵側偭偨偹偠傟宍傪偲偭偰偄傞偙偲偑傢偐傞丅
3.49
(a) 僕僇儖儃儞巁 HOCO-R-CO2H 偵懳偟偰梌偊傜傟偨暘巕幃 C4H6O5 傛傝丄俀偮偺僇儖儃僉僔婎乮 -CO2H 乯傪悈慺偵抲偒姺偊傞偲丄乮 C4H6O5 亅 2亊CO2H 亄 2H 傛傝乯 C2H6O 偲側傞丅偙傟偼乮昤偄偰傒傟偽偡偖傢偐傞偟丄3.25 偺乮敪揥乯偲摨偠傛偆偵峫嶡偟偰傕傛偄偑丄偙偺晹暘偵懳偟偰媮傔傜傟偆晄朞榓搙偼侽偱丄乯暘巕撪偵懡廳寢崌傪傑偭偨偔帩偨側偄傾儖僐乕儖傑偨偼僄乕僥儖偱偁傞丅偙傟傜偵偮偄偰擟堄偺俀売強偺悈慺傪僇儖儃僉僔婎偵抲姺偡傞偙偲偱梌偊傜傟偨暘巕幃偺僕僇儖儃儞巁偺峔憿傪偡傋偰昤偔偙偲偑偱偒傞丅
(b) 悈巁婎偺晅偗崻偺扽慺偑俀媺偱偁傞傛偆側傾儖僐乕儖偲偟偰峫偊傞丅偨偩偟丄拲栚偟偰偄傞扽慺偵偮偄偰偄傞傾儖僉儖婎偺傒側傜偢僇儖儃僉僔婎傕悢偊傞偙偲偵偡傞丅
乮夝摎椺乯
(a) 僸儞僩傪嶲徠偺偙偲丅C2H6O 崪奿偼惵偱帵偟偨丅
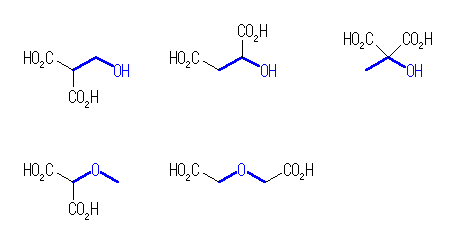
扽巁僄僗僥儖偺峔憿乮
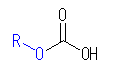 乯傪帩偮埲壓偺俀偮傪嫇偘偰傕傛偄丅
乯傪帩偮埲壓偺俀偮傪嫇偘偰傕傛偄丅
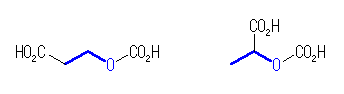
(b) 忋恾偺偆偪丄忋抜丄拞墰偺峔憿丅乮 2-hydroxybutanedioic acid )
3.50
C3H6O3 偲偄偆暘巕幃偼丄乮昤偄偰傒傟偽偡偖傢偐傞偟丄晄朞榓搙偑侾偱偁傞偙偲偐傜傕乯暘巕撪偵丄擇廳寢崌傑偨偼娐偑堦偮偩偗偺峔憿傪帩偮偙偲傪帵偟偰偄傞丅傑偨丄偦偺儌僲僽儘儌懱偑侾庬椶偩偗偱偁傞偲偄偆偙偲偼丄僩儕僆僉僒儞拞偺偡傋偰偺悈慺偑摍壙偱偁傞偙偲傪帵偟偰偄傞丅乮壔妛揑偵偼悈巁婎側偳丄巁慺忋偺悈慺偑廘慺壔偝傟傞偙偲偼峫偊偵偔偄偺偱丄乽扽慺忋偺偡傋偰偺悈慺偑乿摍壙偱偁傞丄偲尵偭偨傎偆偑惓妋偐傕偟傟側偄丅偟偐偟側偑傜偙偙偱偼丄偙偺忦審偼峫偊側偄傕偺偲偟丄乽偡傋偰偺乿悈慺偑摍壙偱偁傞傕偺偩偗傪峫偊丄1,2,3-cyclohexanetriol 偺傛偆側峔憿偼彍偄偰傛偄傕偺偲偡傞丅乯
乮夝摎椺乯
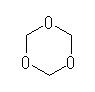
1,3,5-trioxacyclohexane
偩偗偑丄梌偊傜傟偨忦審傪枮偨偡壔崌暔偱偁傞丅
傑偢丄暘巕幃傛傝丄暘巕撪偵偼擇廳寢崌傑偨偼娐偺峔憿偑侾偮偩偗偁傞丅僇儖儃僯儖婎偼帩偨側偄偺偱丄擇廳寢崌偑偁傞偲偡傟偽丄偦傟偼扽慺亅扽慺擇廳寢崌偱偁傞偑丄偙偺傛偆側応崌丄偡傋偰偺悈慺偑摍壙偵側傞傛偆側懳徧惈偺崅偄峔憿傪昤偔偙偲偑偱偒側偄丅
傕偟丄僇儖儃僯儖婎傪帩偭偰傕椙偄偺偱偁傟偽丄師偺傛偆側峔憿偵偍偄偰丄偡傋偰偺悈慺偑摍壙偲側傞丅
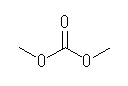
dimethyl carbonate, 扽巁僕儊僠儖
娐偺峔憿傪帩偮傕偺偱丄懳徧惈偺崅偄傕偺偵偼丄1,2,3-cyclohexanetriol 偺傛偆側峔憿傕峫偊傜傟傞偑丄悈巁婎悈慺偲扽慺偺悈慺偑嬫暿偝傟摍壙偱偼側偄丅
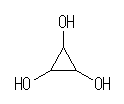
1,2,3-cyclohexanetriol
乮敪揥乯
扽慺尨巕偺巁壔悢偵拲栚偡傞偙偲傕丄偙偺傛偆側栤戣傪夝偔忋偱栶棫偮丅巁壔悢偲偼丄扽慺尨巕偵寢崌偟偰偄傞堿惈尨巕乮巁慺丄拏慺丄僴儘僎儞乯偺悢偱偁傝丄偡側傢偪傾儖僐乕儖傗儌僲僴儘僎儞壔傾儖僉儖偺悈巁婎傗僴儘僎儞偺寢崌偟偨扽慺偵偍偄偰偼侾丄傾儖僨僸僪傗働僩儞偺僇儖儃僯儖婎扽慺偵偍偄偰偼俀丄僇儖儃儞巁傗僄僗僥儖丄巁傾儈僪丄僔傾僲婎側偳偺扽慺偵偍偄偰偼俁偱偁傞丅
儂儖儉傾儖僨僸僪 H2C=O 偺扽慺偵偍偄偰偼丄巁壔悢俀偱偁傞偑丄夝摎椺偵帵偟偨 1,3,5-trioxacyclohexane 偵偮偄偰傕丄偡傋偰偺扽慺偺巁壔悢偑俀偱偁傞丅
偙傟偵懳偟丄扽巁僕儊僠儖偵偍偄偰偼丄僄僗僥儖拞怱偺扽慺偼巁壔悢偑係丄儊僠儖婎偺扽慺偺巁壔悢偼侾偱偁傞丅傑偨丄1,2,3-cyclohexanetriol 偵偍偄偰偼偡傋偰偺扽慺偺巁壔悢偑侾偱偁傞丅
3 H2C=O 仼仺 僩儕僆僉僒儞
偺嶰検壔暯峵偵偍偄偰偼丄扽慺偺巁壔悢偼曄壔偟側偄丅扽慺偺巁壔悢偑曄壔偡傞偨傔偵偼丄堦斒偵巁壔娨尦傪敽偆斀墳偑昁梫偱偁傞丅
3.51-3.54
3.51
傑偢偼峔憿幃傪彂偒丄C2, C3 偺偦傟偧傟偵偳偺傛偆側抲姺婎偑偁傞偺偐傪妋擣偡傞丅師偄偱丄Newman搳塭幃傪彂偒丄廳側傝宆丄偹偠傟宍偺偦傟偧傟偺攝嵗偵偮偄偰丄榗傒僄僱儖僊乕偺戝彫傪峫偊傞偙偲丅
3.42 側偳傕嶲徠偺偙偲丅
乮夝摎椺乯
嫵壢彂 p93丄昞 3.5 傛傝丄埲壓偺悢抣傪梡偄偰丄
偦傟偧傟偺攝嵗偺傕偮榗傒僄僱儖僊乕傪寁嶼偡傞偙偲偑偱偒傞丅
僑乕僔儏憡屳嶌梡丗
丂丂悈慺亅悈慺丂丂 0 kJ/mol
丂丂悈慺亅儊僠儖丂 0 kJ/mol
丂丂儊僠儖亅儊僠儖 3.8 kJ/mol
廳側傝宍憡屳嶌梡丗
丂丂悈慺亅悈慺丂丂 4.0 kJ/mol
丂丂悈慺亅儊僠儖丂 6.0 kJ/mol
丂丂儊僠儖亅儊僠儖 11.0 kJ/mol
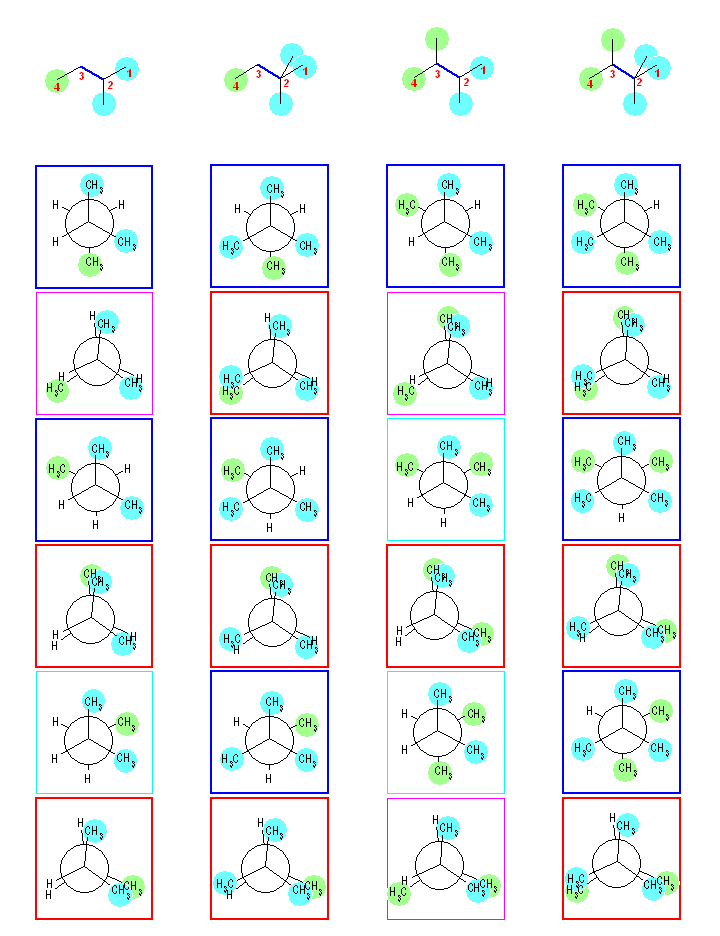
埲壓丄係偮偺壔崌暔偵偮偄偰丄C2-C3 偺寢崌幉偵増偭偨夞揮堎惈懱偵偮偄偰 C2懁偐傜尒偨 Newman搳塭幃傪帵偟偨丅偙偙偱偼丄C2懁扽慺忋偺抲姺婎傪屌掕偟丄C3懁偺扽慺偺抲姺婎傪60搙偢偮塃夢傝偵夞揮偝偣側偑傜攝嵗堎惈懱傪惗惉偟偰偄傞丅
| (a) 2-methylbutane | (b) 2,2-dimethylbutane | (c) 2,3-dimethylbutane | (d) 2,2,3-trimethylbutane |
| |||
| 嵟傕埨掕側偹偠傟宍攝嵗乮惵榞偱帵偟偨傕偺乯 | |||
| 僑乕僔儏 丂乮儊僠儖亅儊僠儖乯亊侾 丂丂3.8 kJ/mol |
僑乕僔儏 丂乮儊僠儖亅儊僠儖乯亊俀 丂丂7.6 kJ/mol |
僑乕僔儏 丂乮儊僠儖亅儊僠儖乯亊俀 丂丂7.6 kJ/mol |
僑乕僔儏 丂乮儊僠儖亅儊僠儖乯亊係 丂丂15.2 kJ/mol |
| 師偵埨掕側偹偠傟宍攝嵗乮悈怓偺榞偱帵偟偨傕偺乯 | |||
| 僑乕僔儏 丂乮儊僠儖亅儊僠儖乯亊俀 丂丂7.6 kJ/mol |
僑乕僔儏 丂乮儊僠儖亅儊僠儖乯亊俁 丂丂11.4 kJ/mol |
||
| 埨掕側曽偺廳側傝宍攝嵗乮搷怓偺榞偱帵偟偨傕偺乯 | |||
| 廳側傝宍 丂乮悈慺亅儊僠儖乯亊俁 丂丂18.0 kJ/mol |
廳側傝宍 丂乮悈慺亅儊僠儖乯亊俀 丂乮儊僠儖亅儊僠儖乯亊侾 丂丂23.0 kJ/mol |
||
| 嵟傕晄埨掕側廳側傝宍攝嵗乮愒榞偱帵偟偨傕偺乯 | |||
| 廳側傝宍 丂乮悈慺亅悈慺乯亊侾 丂乮悈慺亅儊僠儖乯亊侾 丂乮儊僠儖亅儊僠儖乯亊侾 丂丂21.0 kJ/mol |
廳側傝宍 丂乮悈慺亅儊僠儖乯亊俀 丂乮儊僠儖亅儊僠儖乯亊侾 丂丂23.0 kJ/mol |
廳側傝宍 丂乮悈慺亅悈慺乯亊侾 丂乮儊僠儖亅儊僠儖乯亊俀 丂丂26.0 kJ/mol |
廳側傝宍 丂乮悈慺亅儊僠儖乯亊侾 丂乮儊僠儖亅儊僠儖乯亊俀 丂丂28.0 kJ/mol |
偟偨偑偭偰丄嵟傕榗傒偺彫偝偄傕偺偼丄2-methylbutane 偺偹偠傟宍攝嵗偺偆偪忋恾偺惵榞偱帵偟偨傛偆側傕偺丅嵟傕榗傒偺戝偒偄傕偺偼丄2,2,3-trimethylbutane 偺廳側傝宍攝嵗丅
3.52
3.21 側偳偲摨偠傛偆偵峫偊傞偙偲丅
simvastatin 偺俁師尦柾宆
pravastatin 偺俁師尦柾宆
乮夝摎椺乯
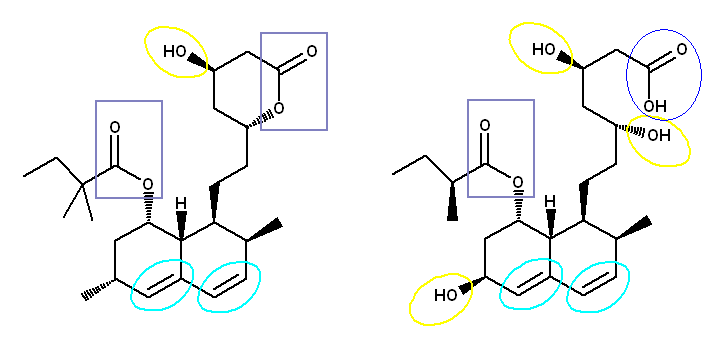
埲壓丄姱擻婎柤乮偦偺姱擻婎傪帩偮壔崌暔偺堦斒柤乯丗忋恾偵偍偄偰偺埵抲丄偺弴偵帵偟偨丅
擇廳寢崌乮僔僋儘傾儖働儞乯丗悈怓
悈巁婎乮傾儖僐乕儖乯丗墿
僇儖儃僉僔婎乮僇儖儃儞巁乯丗惵
僄僗僥儖寢崌乮僄僗僥儖乯丗惵奃偺巐妏
simvastatin 偲 pravastatin 偺峔憿傪丄怓傪曄偊偰傎傏廳側傞傛偆偵帵偟偨丅
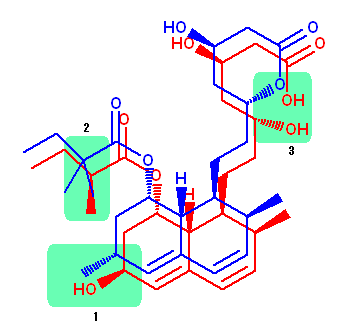
忋恾偐傜傕柧傜偐側傛偆偵丄峔憿忋丄俁売強偺憡堘偑尒傜傟傞丅
1. 僔儞僶僗僞僠儞偱偼儊僠儖婎偑丄僾儔僶僗僞僠儞偱偼悈巁婎偵側偭偰偄傞丅乮傑偨丄棫懱傕媡揮偟偰偄傞丅乯
2. 嵍忋偺僄僗僥儖偺暘婒偑堎側傞丅僔儞僶僗僞僠儞偱偼丄2,2-dimethylbutanoic acid 偺僄僗僥儖偱偁傞偺偵懳偟丄僾儔僶僗僞僠儞偱偼丄2-methylbutanoic acid 偺僄僗僥儖偱偁傞丅
3. 塃忋偺僔儞僶僗僞僠儞偺娐忬僄僗僥儖乮儔僋僩儞乯偑丄僾儔僶僗僞僠儞偱偼傾儖僐乕儖偲僇儖儃儞巁偵壛悈暘夝偝傟偰偄傞丅
3.53
偦傟偧傟偺扽慺偵俀偮偢偮寢崌偟偰偄傞悈慺偑偳偺傛偆側嬻娫攝抲乮棫懱攝嵗乯偵側偭偰偄傞偐偵娭學偑偁傞丅乮係復偱偔傢偟偔妛傇丅乯
乮夝摎椺乯
戝偒偔暘偗偰庡梫場偼俀偮丅侾偮栚偼寢崌妏偑 sp3 崿惉偐傜梊憐偝傟傞妏搙偵嬤偯偔偙偲偑偱偒傞偙偲丅俀偮栚偼丄奺寢崌偑偹偠傟宆攝嵗傪偲傟傞傛偆偵側傞偙偲丅
1) 寢崌妏榗傒偵傛傞愢柧丗丂僔僋儘僿僉僒儞偺峔惉扽慺傪摨堦暯柺撪偵偍偄偨惓榋妏宍偺峔憿偱偁傞偲偡傞偲丄C-C-C 寢崌妏偼120搙偵側偭偰偟傑偄丄sp3 崿惉偐傜梊憐偝傟傞109.5搙傛傝傕戝偒偄丅嫵壢彂偺恾偵梌偊傜傟偨嵍偺峔憿偺傛偆偵丄扽慺尨巕偑暯柺偺忋壓偵摝偘傞偙偲偵傛傝寢崌妏偑彫偝偔側傞偙偲偑偱偒傞丅偦偺偨傔丄摨堦暯柺偵偁傞傛傝傕丄旕暯柺偺愜傟嬋偑偭偨峔憿偺曽偑埨掕偱偁傞丅
2) 偙偺愜傟嬋偑傝偼丄C-C 扨寢崌偺幉偺傑傢傝偺夞揮偵傛偭偰幚尰偝傟傞丅偙偺傛偆側嬻娫揑側尨巕偺攝抲偺偙偲傪丄棫懱攝嵗偲偄偆丅棫懱攝嵗偼丄幒壏晅嬤偱偼暘巕偺傕偮僄僱儖僊乕偵傛傝偍屳偄偵擖傟懼傢傞偙偲偑偱偒傞傕偺偑懡偄丅偙偺偙偲偼丄傾儖僇儞乮偡偱偵戞俁復偱妛傫偩乯偲丄僔僋儘傾儖僇儞乮戞係復偱妛傇乯偵偮偄偰丄嫟捠偱偁傞丅
僔僋儘僿僉僒儞偺丄偙偺恾偵梌偊傜傟偨嵍偺峔憿偼丄乽偄偡宆攝嵗乿偲柤晅偗傜傟偰偍傝丄堦斣廳梫側婑梌傪偟偰偄傞丅
嫵壢彂 4.5 愡丄4.6 愡摍偱埖偆傛偆偵丄僔僋儘僿僉僒儞偺棫懱攝嵗偺拞偱丄偄偡宆攝嵗偱偼丄偡傋偰偺椬傝偁偭偨俀偮偺扽慺尨巕偵偍偄偰丄寢崌偟偨悈慺偑屳偄偵堦斣偼側傟偨峔憿乮偹偠傟宆攝嵗乯偲側偭偰偄傞偨傔偵埨掕偱偁傞丅
3.54
係復丄4.2愡傪嶲徠丅
乮夝摎椺乯
僔僋儘傾儖僇儞偼丄娐傪峔惉偟偰偄傞扽慺摨巑偺娫偺寢崌偵偦偭偨夞揮偵惂尷偑偁傞丅傕偟丄塃庤偺拞巜傪嵍庤偱偮偐傫偱偄傞偲偒丄塃庤偺恊巜偺埵抲偲恖嵎偟巜偺埵抲偲傪擖傟懼偊傞偙偲偑偱偒側偄傛偆偵丄娐傪峔惉偟偰偄傞扽慺偵寢崌偟偨抲姺婎偼丄娐偺柺偵懳偡傞忋壓傪擖傟懼偊傞偙偲偑偱偒側偄丅仸
偦偺偨傔丄師恾偺傛偆偵丄娐偺柺偵懳偟偰俀偮偺儊僠儖婎偑摨偠懁偵偁傞傕偺乮cis-懱乯偲丄媡懁偵偁傞傕偺乮trans-懱乯偲偑偁傝丄屳偄偵嬫暿偝傟傞丅偙傟傪僔僗亅僩儔儞僗堎惈偲偄偆丅
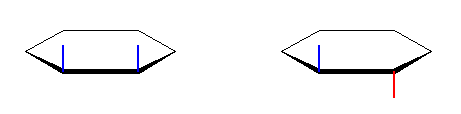
拹仸丗偙傟偼丄寢崌偺愗抐偲嵞寢崌傪敽傢偢偵偼扽慺忋偺係偮偺寢崌偺棫懱娭學傪斀揮偝偣傞偙偲偑偱偒側偄偐傜偱偁傞丅棫懱偺斀揮偵偮偄偰偼丄偨偲偊偽嫵壢彂 11 復偱徻偟偔妛傇丅
側偍丄trans 懱偱偼丄峏偵師偺俀偮偺堎惈懱偑嬫暿偝傟傞丅
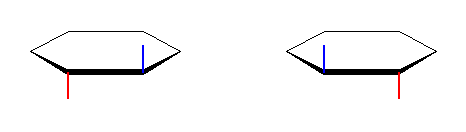
忋恾偵帵偟偨俀偮偺峔憿偼丄嬻娫撪偺暯峴堏摦傗暘巕慡懱偺夞揮偺憖嶌偺傒偱屳偄偵廳偹偁傢偣傞偙偲偑偱偒偢丄塃庤偲嵍庤偺傛偆側娭學偵偁傞丅偙偺傛偆側傕偺偼屳偄偵岝妛堎惈懱乮嬀憸堎惈懱丄懳彾懱乯偱偁傞偲偄偆丅
師偺俁師尦柾宆偵丄偙傟傜擇偮偺峔憿傪帵偟偨丅廳偹偁傢偣傞偙偲偑壜擻偐偳偆偐丄俁師尦柾宆傪摦偐偟偰専摙偟偰傒傛丅
嵍偺 trans-1,2-dimethylcyclohexane 偺俁師尦柾宆
塃偺 trans-1,2-dimethylcyclohexane 偺俁師尦柾宆