18.01-18.10 (01-10)
18.01, 01
以下、いずれの方法でも命名でき、間違いではない。
命名法1)「アルキル基名1」+「空白文字」+「アルキル基名2」+「空白文字」+「エーテル」
アルキル基名1とアルキル基名2が等しいときは、「ジ(またはビス)+アルキル基名」+「空白文字」+「エーテル」となる。日本語表記では区切りの空白文字は不要。アルキル基名が複雑になる場合には、命名法2を用いる方がよい。
命名法2)主に非対称なエーテルの命名に用いる。通常、大きな方の部分を母核に選び、残りのエーテル部を、アルキルオキシ基(alkyloxy group)として命名する。アルキルオキシ基のうち、次の9種は短縮型を用いてよい。さらに、このうちグループAは、誘導体を作って命名してもよい。
| グループ | 構造 | 短縮型の名称 |
|---|---|---|
| A | CH3O- | methoxy |
| CH3CH2O- | ethoxy | |
| CH3CH2CH2O- | propoxy | |
| CH3CH2CH2CH2O- | butoxy | |
| C6H5O- | phenoxy | |
| B | (CH3)2C(H)O- | isopropoxy |
| (CH3)2C(H)CH2O- | isobutoxy | |
| CH3CH2C(H)(CH3)O- | sec-butoxy | |
| (CH3)3CO- | tert-butoxy |
×ペントキシ基 → ○ペンチルオキシ基
上記表にないものは、短縮型が認められない。
(解答例)
a) diisopropyl ether, or 2-isopropoxypropane
b) cyclopentyl propyl ether, or propoxycyclopentane
c) 4-bromophenyl methyl ether, or 14-bromo-41-methoxybenzene
p-bromoanisole でも可。アニソール anisole は methoxybenzene の慣用名。
d) cyclohexene-1-yl methyl ether, or 1-methoxycyclohexene
e) ethyl isobutyl ether, (or ethyl 2-methylpropyl ether), or 1-ethoxy-2-methylpropane
f) allyl vinyl ether, (or ethenyl 2-propenyl ether), or 3-vinyloxy-1-propene
飽和炭化水素からの1価基 alk-yl に相当するところの「不飽和炭化水素からの1価基(多重結合を持つアルキル基)」は、語尾を enyl、ynyl、dienyl、enynyl などとし、必要ならば不飽和結合の位置を示す。このときの番号は遊離原子価炭素(アルキル基のねもと)を1とする。
18.02, 02
「酸触媒によるアルコールからの脱水でのエーテル合成」に限らず、同じタイプの2分子の基質から生成物を得る反応では、非対称な生成物を得るためには、いつも同じようなことが問題となる。
この反応の機構は、教科書 18.2 節に述べられているとおり、プロトン化を受けたアルコール分子に対し、別のアルコールの水酸基の酸素孤立電子対による求核反応により水を脱離して生じる。
(解答例)
A と B とを混合して反応させようとした場合、A は B だけではなく A に対しての反応も起こし、同様に B は A だけでなく B とも反応を起こす。つまり、A-A、A-B、B-A、B-B の4種類が生成することになる。生じる生成物がエーテルであるから、この反応においては A-B と B-A は区別しない。
実験上のテクニックとして、反応する A の周囲にほとんど B しかない状況をつくり出すことができれば、事態は改善される。すなわち、A を大過剰の B の中に少しずつ滴下するなどにより、A が別の A と反応できない状況にしてやれば、非対称な生成物 A-B のみが得られると考えられる。
この反応においては、反応にかかわる活性種はプロトン化を受けたアルコールである。一方のアルコール A のみがプロトン化を受ける状況をつくりだすことが可能であれば、周囲に過剰にある B との反応のみを起こすことができると考えられ、また、少なくとも B-B は生じないはずである。
とはいえ、アルコール水酸基の酸素に配位されたプロトンは、1つのアルコール分子に固定されていると考えるよりも、交換が頻繁におきていると考えられる。つまり、はじめに一方のアルコール A に硫酸を触媒として加えたのちに、これを大量の B の中へ滴下したとしても、系中ではエーテルを生じるより前に、プロトン化を受けた AH+ と BH+ とが平衡になってしまい、非対称なエーテルを生成させる試みはうまくいかないだろうと考えられる。
エタノールと 1-プロパノールとを反応させると、diethyl ether, ethyl propyl ether, dipropyl ether が 1:2:1 で生じると予想される。
18.03, 03
Williamson エーテル合成は、問題 18.2 のような酸触媒によるアルコールの脱水と比較して、非対称なエーテルを合成する上で有利である。これは、A 部分がほかの A とは反応せず、また A や B と反応するような B' も生じないため、反応において A-B のみを与えるからである。
Williamson エーテル合成の反応機構は教科書 18.3 節を参照のこと。
Williamson エーテル合成における反応の限界は、この反応が SN2 で進行するため、求核攻撃をうける側(ハロゲン化アルキル)が1級(または2級)でなければならないことである。ベンゼン環上やビニル位など、求核攻撃をうける側の炭素に二重結合(π 電子)がある場合にも反応は起きない。
以上に注意して、ハロゲン化アルキルに何を用い、アルコキシドに何を用いるかを決定する。
(解答例)
(a) いずれのアルキル基も1級であるから、次のいずれの組み合わせでも合成可能である。
○ CH3CH2CH2O- + CH3Br
○ CH3O- + CH3CH2CH2Br
(b) フェニル基の炭素上では求核置換反応はおきにくい。(→発展)
○ PhO- + CH3Br
× CH3O- + PhBr (未反応)
(c) 1級と2級のアルキル基であるから、1級のハロゲン化アルキルを選ぶ方がよい。
○ (CH3)2CHO- + PhCH2Br
△ PhCH2O- + (CH3)2CHBr (脱離反応が競争する。)
(d) 1級と3級のアルキル基であるから、1級のハロゲン化アルキルを選ばなければならない。
○ (CH3)3CO- + CH3CH2Br
× CH3CH2O- + (CH3)3CBr (脱離により、2-methylpropene を生じる)
PhX → PhX' のような「芳香族求核置換反応」は、次のような限られた系でのみ起きる。以下は例外と考え、フェニル基上での求核置換反応は「通常は起きない」と考えてしまってもよい。
- 芳香環の置換位置のオルト位、およびパラ位にニトロ基などの強い電子吸引性基があり、炭素上の π 電子密度が非常に小さくなっている場合。(SN2 的に進行する。)
- 脱離基が N2 であるジアゾニウム塩(下図 C6H5N2+・X- )のように、脱離基が極めて脱離しやすい場合。(SN1 的に進行し、C6H5+ イオンを経由する。)
- 上記のいずれにも相当しない場合で、非常に強い塩基(NaNH22 など)を用いた場合。(反応は、HX の脱離と、HX' の付加の機構で進行する。HX の脱離で生じる反応中間体は、ベンザイン benzyne と呼ばれる特殊な構造である。)
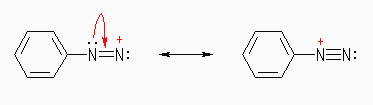 ジアゾニウム塩の構造
ジアゾニウム塩の構造
18.04, 04
問題 18.3 のヒントを参照すること。
求核置換反応については、11章を見直すこと。
(解答例)
(a) bromoethane(1級) > 2-bromopropane(2級) >> bromobenzene (aryl halide は反応しない)
(b) bromoethane > chloroethane >> 1-iodopropene (vinylic なので反応しない)
(b) は、脱離基の脱離しやすさにより、iodoethane > bromoethane > chloroethane の順が決まる。
18.05, 05
オキシ水銀化法の詳細な反応機構については、電子の流れを意識しながら、図の 7.4 を自分で描いてみること。
アルコキシ水銀化法は、オキシ水銀化法に対し、次の2点が異なるのみで、それ以外は同じである。
1) マーキュリニウムイオン(3員環の中間体)に対して求核攻撃するものが、水の代わりにアルコールである。
2) 酢酸水銀の代わりにトリフルオロ酢酸水銀を用いる。
後者は、酢酸イオンによる求核攻撃がおきると、副生成物が生じるので、これを防ぐためである。
1-methylcyclopentene のような基質に反応させる場合、二重結合が左右非対称なのでそのどちらに反応するか(位置特異性)、反応のときに立体はどのようになるか(立体特異性)の両方に気をつけなければならない。
(解答例)
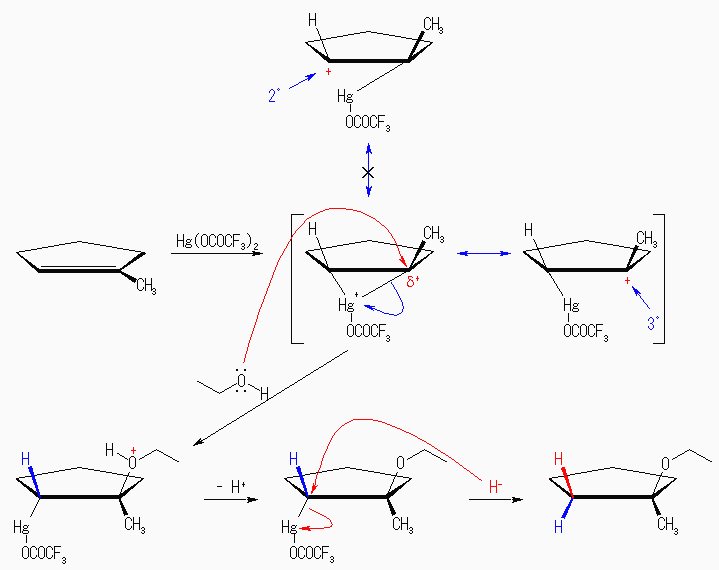
マーキュリニウムイオンは、なるべく多くの置換基のついた炭素(3級炭素)の上に正の部分電化を持ち、この炭素に対する求核攻撃をうける。そのため、マルコフニコフ配向の位置選択性をもち、アルコキシ化が進行する。アルコキシ基は、水銀基とはトランスの立体選択性で付加している。これが NaBH4 由来のヒドリドにより還元的に切断される際に反転を起こす。このスキームに示した生成物では、ヒドリド還元に際しての付加の立体は区別できないが、NaBD4 などを用いた場合には区別できることになる。
18.06, 06
次の反応の限界を考慮にいれて合成法を選択する。
Williamoson 合成では、ハロゲン化アルキルに3級以上のものを用いることができない。2級は不可能ではないが、なるべく1級が好ましい。
アルコキシ水銀化法では、原料のオレフィンに対して、マルコフニコフ配向でしか付加できない。
(解答例)
以下の略解では、必ずしも普遍的ではない省略の仕方をした。アルコキシ水銀化法では、「アルケン + (アルコキシ水銀化法であることを明示的に示すため)Hg(OCOCF3)2 + アルコール」の順で示しているが、必ずしもこれらを一度に混ぜて進行させるとは限らない。また、これにより生じた有機水銀化合物をヒドリド還元してはじめてアルコールが得られる。
(a) butyl cyclohexyl ether (butoxycyclohexane)
○ C6H11O- + n-C4H9Br
△ n-C4H9O- + C6H11Br
○ cyclohexene + Hg(OCOCF3)2 + n-C4H9OH
× 1-butene + Hg(OCOCF3)2 + cyclohexanol (sec-butyl cyclohexyl ether を与える)
(b) benzyl ethyl ether
○ PhCH2O- + CH3CH2Br
○ CH3CH2O- + PhCH2Br
○ ethene + Hg(OCOCF3)2 + PhCH2OH
ethene は特に室温で気体なので、Williamoson 合成の方が扱いやすい。
(c) sec-butyl tert-butyl ether
△ (CH3)3CO- + CH3CH2CHBrCH3
× CH3CH2CH(O-)CH3 + (CH3)3CBr
○ 2-methylpropene + Hg(OCOCF3)2 + CH3CH2CH(OH)CH3
○ 1-butene + Hg(OCOCF3)2 + (CH3)3COH
○ 2-butene + Hg(OCOCF3)2 + (CH3)3COH
(d) tetrahydrofuran (THF)
○ BrCH2CH2CH2CH2O-
× CH2=CHCH2CH2OH + Hg(OCOCF3)2
問題の解とは関係ないが、Williamoson 合成、アルコキシ水銀化法の両者ともが選択可能である場合、環境への考慮をすると水銀を使う方法を避けるのが一般的だと思われる。
18.07, 07
(a) 3級のアルキル基と、1級のアルキル基(メチル基)の結合したエーテルである。
(b) 2級のアルキル基と1級のアルキル基の結合したエーテルである。
(解答例)
(a) 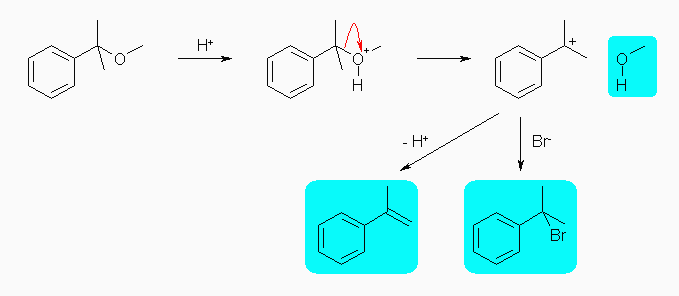
酸性条件下で、エーテル酸素がプロトン化されたあと、メタノールとともに3級のカルボカチオンが生じ、このカルボカチオンからは(E1 機構により) 2-phenylpropene と(SN
1 機構により) 2-bromo-2-phenylpropane とを生じる。
(b) 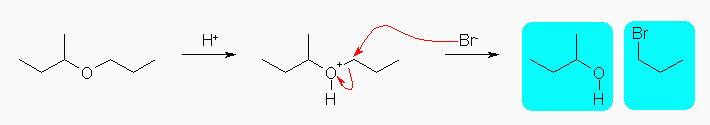
酸性条件下で、エーテル酸素がプロトン化されたあと、Br- により、立体的によりすいている1級の炭素に対して求核攻撃がおこり、 SN
2 機構により 1-bromopropane と 2-butanol を生じる。
18.08, 08
第3級、ベンジル位、アリル位のエーテルは、安定化されたカルボカチオンを生成することができるため、共通のカルボカチオン中間体を経由して、E1 機構、または SN 1 機構で開裂する。(この二つの反応は、競争となり、どちらが優先するかは反応条件などによる。)
(解答例)
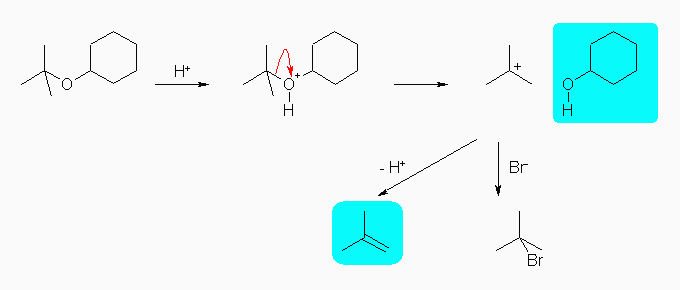
酸性条件下で、エーテル酸素がプロトン化されたあと、シクロヘキサノールとともに3級のカルボカチオンが生じ、このカルボカチオンからは(E1 機構により) 2-methylpropene と(SN
1 機構により) 2-bromo-2-methylpropane を生じる。
18.09, 09
いずれの酸も、H+ の供与体であるという点では共通である。従って、酸によるエーテルの開裂において、エーテル酸素がプロトン化を受けるところまでは同じであると考えられる。第3級、ベンジル位、アリル位のエーテルの場合は、安定なカルボカチオンを生じながら結合が切れる反応が、1分子的に生じる。しかし、それ以外のエーテルの場合は、ハロゲン化物イオンによるエーテル炭素への求核攻撃があってはじめて2分子的な開裂となる。
(解答例)
(ヒントからの続き)ハロゲン化物イオンによるエーテル炭素への求核攻撃により反応するのであるから、これらのイオンの「求核性」が高いほど、反応は効果的に進行する。
水溶液中では、ハロゲン化物イオンの求核性は、I- が一番高く、ついで、Br- で、Cl- は求核性が低い。
教科書 11.5 節で既習の事項であるが、SN2 反応の特性のうち、求核試薬の影響については、以下のような傾向にある。
- 通常、中性の求核種よりも負に帯電した求核種の方が反応性が高い。
- 同じ反応原子を有する求核種同士での比較では、塩基性の高いものほど求核性が高い傾向にある。(その求核種に対する共役酸が弱いものほど求核性が高い、と言っても同じ意味である。)
これは、塩基性と求核性が水素および炭素に対するという違いはあるにしても、いずれもルイス塩基性という共通の性質によるものであるからである。 - (水溶液中の求核反応に関しては、)電気陰性度の低い周期表の下の元素ほど求核性が高い。これは、電気陰性度の高いイオンほど強く水和されてしまう傾向にあり、裸のイオンとして振舞えないためである。
希エタノール溶液中のブロモメタンの SN2 反応の求核種の反応性について、教科書より下表を引用しておく。
| 求核種 | 相対反応性 |
|---|---|
| H2O | 1 |
| CH3CO2- | 500 |
| NH3 | 700 |
| Cl- | 1000 |
| OH- | 16000 |
| CH3O- | 25000 |
| I- | 100000 |
| CN- | 125000 |
| HS- | 125000 |
18.10, 10
Claisen 転位の反応機構を描いた教科書の図 18.1 に対応させて、反応機構を描いてみること。
(解答例)
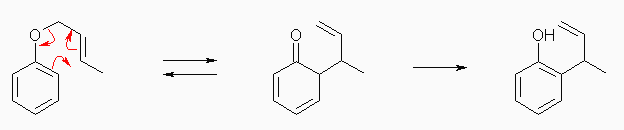
Claisen 転位は、6員環の環状遷移状態を経由するペリ環状反応で進行する。生じたシクロヘキサジエノン中間体は、ケト-エノール互変異性化反応により、アリルフェノールを生じる。したがって、2-butenyl phenyl ether は、Claisen 転位により上図のように反応し、2-(1-methylallyl)phenol を生じる。1-methylallyl 基は、1-methyl-2-propenyl 基として命名してもよい。(アルキル基のねもとが1になるので、二重結合は、C2-C3 間である。)
18.11-18.20 (11-22)
18.11, 11
m-クロロ過安息香酸(mCPBA, PhCO3H)は、過酸(peroxyacid)のひとつである。反応性生物だけではなく、反応機構もおさえておくこと。
この問題では、反応の位置特異性は考える必要がないが、立体選択性についてはきちんと考えること。
(解答例)
アルケンと過酸との反応では、エポキシドが生じる。また、その際には、1段階の機構で、シンの立体化学でアルケンに酸素が付加する。
この反応の反応機構の描き方には、次の2通りがあり、反応の条件(溶媒の極性など)によりどちらで進行するかが決まるが、生成物や反応の立体化学はいずれの描き方でも同じになる。
ひとつめは、教科書 18.7 節にも描かれている反応機構で、過酸の末端に近いほうの酸素(正の部分電荷を持つ)にアルケンの π 電子が求核的に付加する(言い換えるならば、過酸の正の部分電荷を持つ酸素が π 電子に対して求電子的に反応する)ことにより起こる。
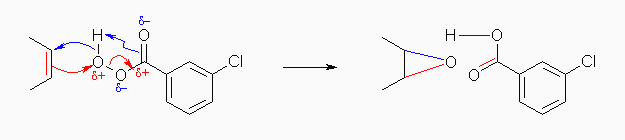
ふたつめは、過酸をまず次式のように解離させてしまう方法である。
RCOOOH ←→ RCO2- + OH+
ここで生じた OH+ は、O+の価電子が5個であることから、酸素原子は1本の共有結合のほか、2対の電子対を持ち、したがって最外殻に6個の電子しか入っていない状態にあり、強いルイス塩基性を示す。この OH+ がアルケンに対して求電子的に付加していくことによりエポキシドを生じる。
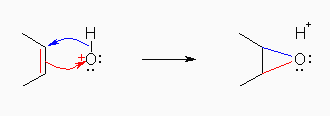
いずれの機構で描いたとしても、「アルケンに対してシンの立体化学で酸素が付加する」点では同じであり、cis- アルケンからはエポキシドの3員環に対して2つの置換基が cis- 配置になったものが、trans- アルケンからはエポキシドの3員環に対して2つの置換基が trans- 配置になったものが生じる。
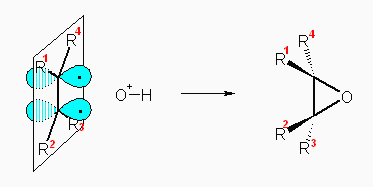
したがって、cis-2-butene と過酸の反応により、cis-2,3-epoxybutane を生じる。
18.12, 12
上の問題 8.11 と同様に考えること。
(解答例)
過酸によるエポキシドの合成では、「アルケンに対してシンの立体化学で酸素が付加する」から、cis- アルケンからはエポキシドの3員環に対して2つの置換基が cis- 配置になったものが、trans- アルケンからはエポキシドの3員環に対して2つの置換基が trans- 配置になったものが生じる。

したがって、trans-2-butene と過酸の反応により、trans-2,3-epoxybutane を生じる。
18.13, 13
(a), (b) いずれのエポキシドも、エポキシド炭素の一方が3級であることに注意し、立体の位置特異性により生成物を予測する。この問題で与えられているエポキシドの場合は、対称性から、生成物の立体化学にはさほど注意しなくてもよい。
(解答例)
酸触媒でのエポキシドの開環反応では、非環状エーテルの酸による開裂とはことなり、SN1 的な性質を持った求核置換反応で進行するから、(カルボカチオンがより安定な)3級炭素上で(立体反転を伴うという意味ではSN2 的な)の置換が起きる。したがって、以下のものが主生成物となる。
(a) 2-chloro-1-cyclohexyl-2-methyl-1-propanol
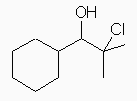
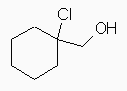
(b) (1-chlorocyclohexyl)methanol
18.14
(a) と (b) は、水酸基の立体配置が異なるだけの幾何異性体である。
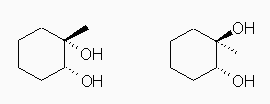
(a) (1S,2R)-1-methylcyclohexane-1,2-diol, (b) (1R,2R)-1-methylcyclohexane-1,2-diol
これらを合成しわけるには、同じ出発物質からはじめて、異なるルートを経由する。
(解答例)
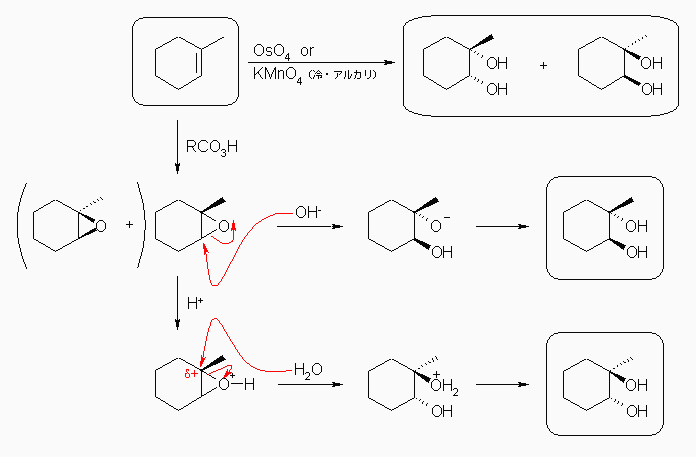
1-methylcyclohexene を共通の出発物質とし、四酸化オスミウム、または冷アルカリ性条件下で過マンガン酸カリウムなどにより処理すると、cis-1,2-ジオールを得る。ただし、この条件では、一般に光学異性体を作り分けることはできないから、(1S,2R) 体と、(1R,2S) 体の混合物となるはずである。
1-methylcyclohexene を過酸で処理することにより、エポキシドを得る。これを水酸化物イオンで求核攻撃し、開環させるか、または、酸性条件下、水による求核攻撃により開環させることにより、trans-1,2-ジオールを得る。上スキームでは、エポキシドに対し、酸性、塩基性での開環反応について立体が異なることを示したが、過酸の処理によりエポキシドを得る際に光学異性体の一方のみを得ているのではない限り、いずれも (1S,2S) 体と、(1R,2R) 体の混合物となる。
18.14
cis-5,6-epoxydecane の構造は次のとおり。
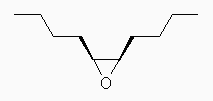
この酸性加水分解では、エポキシ酸素にプロトン化を受けたあと、水が求核剤としてはたらく。
(解答例)
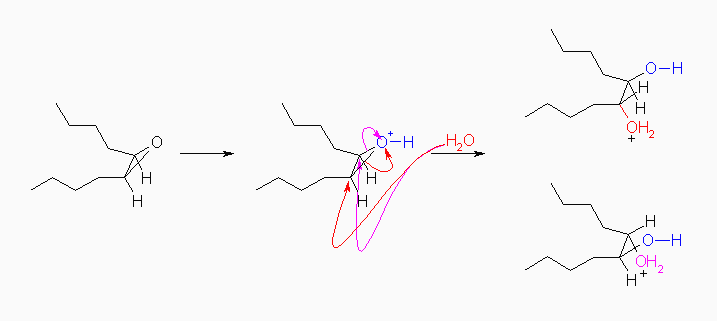
正常な背面からの SN2 反応により、C-O+結合が切れて、一方の炭素上でワルデン反転を起こすので、cis-5,6-decanediol のラセミ混合物、すなわち、(5R,6R)- および、(5S,6S)-5,6-decanediol の等量混合物が得られる。
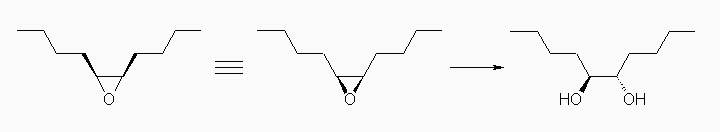
のように生成物の構造を書いてもよい。
18.15
trans-5,6-epoxydecane の構造は次のとおり。
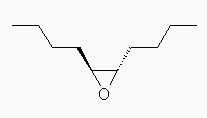
この酸性加水分解では、エポキシ酸素にプロトン化を受けたあと、水が求核剤としてはたらく。
(解答例)
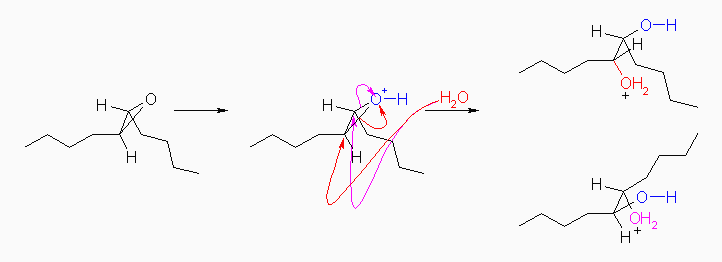
正常な背面からの SN2 反応により、C-O+結合が切れて、一方の炭素上でワルデン反転を起こすので、trans-5,6-decanediol (または、meso-5,6-decanediol )が得られる。((5R,6S)-体および、(5S,6R)-体は同一であることに注意。)
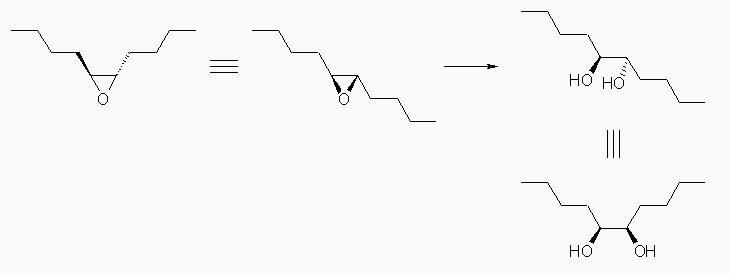
のように生成物の構造を書いてもよい。
18.15, 16
天然に一番大量に存在する酸素は、16O であり、18O はその同位体である。ともに同じ酸素原子なので、ほとんど同じ化学反応性を示すが、生成物中で区別される別の原子として考える。したがって、エポキシド中にもともとあった酸素原子と、水由来で導入された酸素原子を区別するためにこのような同位体標識を行っていると考えられる。
同じ出発原料からはじめても、(a) アルカリ性条件下と (b) 酸性条件下では、反応の位置選択性が異なることを思い出すこと。
明示されていないが、(a) の条件では、NaOH より生じる水酸化物イオン OH- は、水の解離平衡( H2O ←→ H+ + OH- )を通して、溶媒として周囲に大量にある H218O により交換され、大部分は18OH-であるものとして反応させてよい。
(解答例)
いずれも、同様に 2-methyl-1,2-butanediol を与えるが、エポキシドへの求核攻撃の位置選択性がアルカリ性、酸性で逆になることより、同位体標識された 18O を含む水酸基の位置が異なるアルコールが得られる。
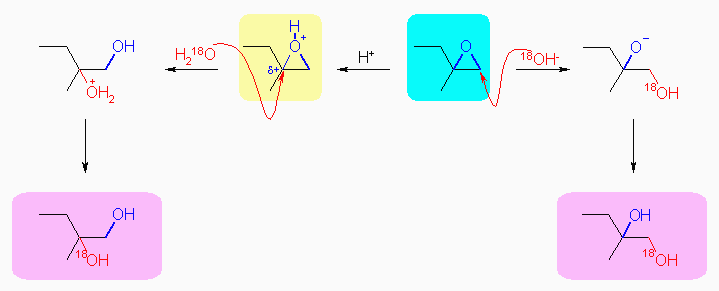
すなわち、中性からアルカリ性では、SN2 反応でエポキシドの開環が進行するから、立体的によりすいている方の炭素に求核攻撃がおこる(水色)。酸性では、エポキシド酸素がプロトン化を受けているため、環ひずみの大きな3員環は C-O+ 結合が長くのびてカルボカチオン的な性格を持っており、したがって(カルボカチオンがより安定化されるような)3級の炭素上に求核攻撃を受け(黄色)、SN1 的な性格を兼ねそなえた SN2 反応でエポキシドの開環が進行する。
酸素の同位体存在度は、16O で 99.76% である。18O は0.20%、17O は0.04%。
同位体標識された原子を O* のように、アスタリスクをつけて表すことがある。(不斉炭素も同様な表示をした。)なお、教科書下巻の巻末付録の「答え」では、 O・ のように表されている酸素が、同位体標識された 18O である。
18.16, 17
空孔の大きさを比較するだけなら、構造式を書いてみるだけでもよい。
x-クラウン-y 式の命名法では、全体で x 員環、うちの y 個は酸素となっている。
(解答例)
それぞれ、空孔の大きさを模式的に色付きの円で表している。
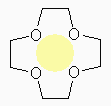
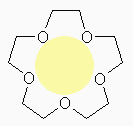
15-crown-5, 12-crown-4
クラウンエーテルは、その酸素のルイス塩基性により、金属イオンに複数の酸素が同時に配位することで金属イオンとの錯体を安定化する。そのため、クラウンエーテルの構造を書く際には、酸素原子を空孔の内側の部分に書くことが多い。
18.17, 19
no hints
(解答例)
(a) 2-butanethiol
(b) 2,2,6-trimethylheptane-4-thiol
(c) 2-cyclopentaene-1-thiol
(d) ethyl isopropyl sulfide
(e) 1,2-bis(methylthio)benzene
(c) で ~thiol と命名するときは、thiol 基が1位なので、二重結合はシクロペンタン環の2、3位の炭素間である。
18.18, 20
チオール類の合成法の指針として、ハロゲン化アルキルからチオールを合成することができる。すなわち、これらの出発物質よりどのようにして 1-bromo-2-butene を合成するかという問題に帰着することができる。
チオールの合成は、ハロゲン化アルキルからのアルコールの合成と同等の考え方でよいのだが、1つ気をつける点がある。アルコールの合成においては、水酸化物イオン( OH- )による求核置換反応が有効であった。同様に、水硫化物イオン( SH- )も、非常に有効な求核剤としてはたらくが、生成したチオールも(硫黄の酸素よりも強い求核性のため)求核剤としてはたらいてしまう。このため、チオールでとまらずにスルフィドを与えてしまうおそれがある。これを避けるためには、チオ尿素を使った反応が有効である。(教科書 18.11 節参照)
1,3-butadiene を出発原料とする場合、これが「共役ジエン」であることを思い出すこと(教科書 14章)。
(解答例)
反応条件は、典型的なものを示した。
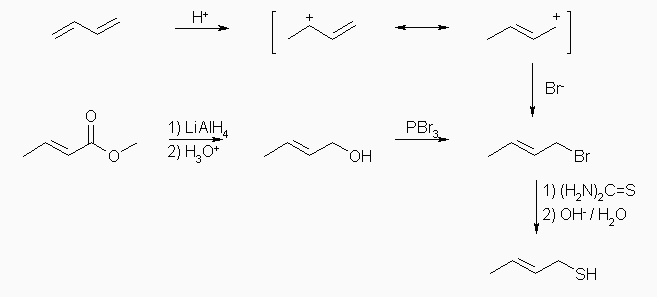
1,3-butadiene への HBr 付加は、40℃より高温で行い 1,4-付加体を優先して得る。(発展および、教科書 14 章参照。)
methyl 2-butenoate のヒドリド還元は、エステルなので一般的に LiAlH4 を用いる。(共役エノンの構造を有するから、たとえケトンやアルデヒドだったとしても、NaBH4 ではなく LiAlH4 を用いる。)
アルコールからのハロゲン化は、水酸基を脱離基に変えているだけだから、Tos-Cl (p-toluenesulfoyl chloride)を用いて、単にスルホン酸エステルにするだけでも用は足りる。(R-Br の代わりに R-O-Tos を用いてもよい。)
1,3-butadiene への HBr の付加反応は、アリル型カチオンを経由するため、2つの生成物の混合物を与える。そのひとつは、1,2-付加体(3-bromo-1-butene)で、もうひとつは、1,4-付加体(1-bromo-2-butene)である。(教科書 14.3 節)
この反応は、低温では速度支配となり 1,2-付加体を優先して与えるが、高温では熱力学支配となり 1,4-付加体を優先して与える。(教科書 14.4 節)
18.19, 18
与えられた分子式 C4H8O と積分曲線から考えて、それぞれのピークに対応する水素原子数は、低磁場(化学シフト値の大きい方)から順に、1H, 1H, 1H, 2H, 3H であると予想できる。
3~4ppm の範囲にピークがないことから、鎖状のエーテルや、エステルの構造は無いものと予想できる。図 18.5 の1,2-epoxypropane の 1H-NMR スペクトルと見比べてみると、同様にオキシラン環を持つ化合物であると予想できる。
いちばん高磁場側のピークは、積分比として 3H 分あり、トリプレット(3重線)となっていることから、CH2 に隣接した CH3 である可能性が高い。
(解答例)
1,2-epoxybutane の 1H-NMR スペクトルである。(構造式省略)
18.21
「沸点が高い」「水と混ざりやすい」は、いずれも分子が高い極性を持つことを示している。
なぜ dimethyl sulfide と dimethyl sulfoxide では、分子の極性が大きく異なるのかを、分子の構造より説明すればよい。(→ 教科書 2章参照のこと。)
(解答例)
教科書2章の電気陰性度を記した図表(図2.2)を見ると、硫黄の電気陰性度は炭素と同じで 2.5 であることがわかる。酸素では、3.5。
したがって、dimethyl sulfide は、propane と類似の電荷の分布を持つと考えられ、極性はあまり大きくないと考えられる。これに対し、dimethyl sulfoxide は、acetone (2-propanone) と類似の電荷分布を持つと考えられ、S-O 結合の方向に大きく分極していると予想できる。
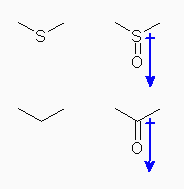
(acetone は水と自由に混ざり、室温で液体であるが、propane は水と混ざらず、また室温では気体である。)
18.20, 22
(a) シクロヘキサン環上の置換基の立体配置(シス/トランス)を考慮に入れて命名すること。命名法については、問題 18.01 のヒントを参照すること。
(b) エーテル酸素は、2つの炭素を含む3員環内にあるから、エポキシドとして命名することになる。教科書 18.7 節を参照して命名すること。
(解答例)
(a) cis-1-ethoxy-3-methylcyclohexane
ethyl 3-methylcyclohexyl ether
シクロヘキサンを母核として命名する場合、エチルオキシ基は短縮型のエトキシ基が置換基名となる。メチル基とエトキシ基の位置番号は、どちらを1に、どちらを3にしても同じだから、アルファベット順で先のエトキシ基が1となる。なお、エタンを母核にした命名の場合だと 3-methylcyclohexyloxyethane となるが、特別な理由がない限り小さい方の部分を母核に選ぶことは無い。メチルシクロヘキシル基の位置番号では、遊離炭素(アルキル基ねもと)を1とする。
(b) E-2-(2-bromophenyl)-2,3-epoxybutane
2-(2-bromophenyl)-2,3-dimethyloxirane
前者の名前は、次のようなオレフィン E-2-(2-bromophenyl)-2-butene の誘導体として、命名されている。

また、後者は oxirane オキシラン(酸素を含む3員環、エポキシエタンの慣用名)を母核とし、これに置換基名をつけている。立体も区別して表示したい場合には、次のようになる。
(2R,3R)-2-(2-Bromophenyl)-2,3-dimethyloxirane
18.21-18.30 (23-30)
18.21, 23
酸によるエポキシドの開環反応に関しては、教科書 18.8 節(特に前半)を参照して解答すること。
なお、与えられたエポキシドの立体は、次のとおりである。
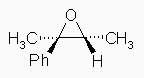
(解答例)
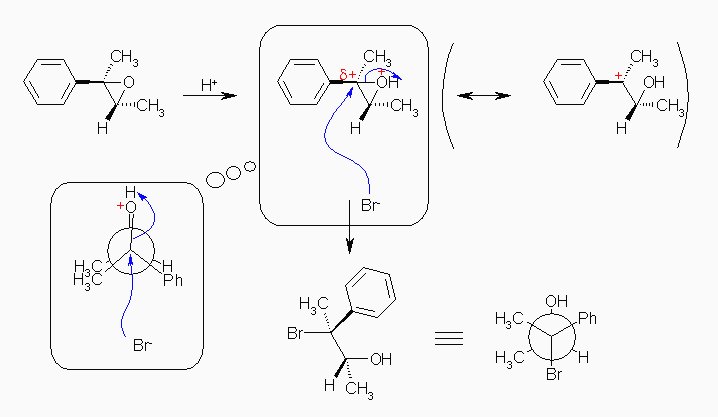
酸性条件下、プロトン化をうけたエポキシドは、3員環がおおきな環歪みをもっていて開環しやすいため、カルボカチオン的な性質をあわせもったイオンとなる。すなわち、上図のように、より安定なカルボカチオンと同様に3級炭素上に正の部分電荷を強く持ち、この部分で求核攻撃を受ける。その結果、立体特異性としては SN2 的でありながら(すなわち、ラセミ化せず、炭素上でワルデン反転を伴う)、位置特異性としては SN1 的な性質(より混み合った炭素で置換がおきる)をあわせもった求核置換反応が進行し、結果として、(2R,3S)-3-bromo-3-phenylbutan-2-ol を生じる。
18.22
エポキシドの中性~塩基性での開環反応なので、教科書 18.8 節(特に後半)を参照して解答すること。グリニヤル試薬 CH3MgBr による処理は、形式的には、CH3- による求核攻撃と考えてよい。
なお、与えられたエポキシドの立体は、次のとおりである。
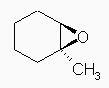
(解答例)
酸性条件とは異なり、より置換の少ない(立体的に空いている)炭素に対しての求核攻撃がおき、SN2 機構で反応が進行する。
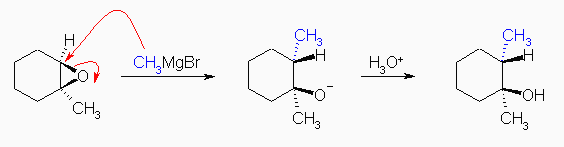
生成物は、(1S,2S)-1,2-dimethylcyclohexanol である。
18.23
アルケンをアルカリ水溶液中、Br2 で処理すると、アルケンに対する臭素化の時と同じ三員環の中間体、ブロモニウムイオンが生じる。これに、水酸化物イオンが求核攻撃すると、ブロモヒドリンとなり、更にアルカリ性条件下なので、ブロモヒドリンよりプロトンが脱離し、分子内での求核攻撃によりエポキシドとなる。
このエポキシドは、もう一度水酸化物イオンにより求核攻撃を受けると、トランスの 1,2-ジオールを与える。この反応は、OsO4 との反応、もしくは冷アルカリ性での MnO4- との反応(いずれもシスの 1,2-ジオールを与える)と対比させて覚えること。
過酸での処理は、教科書 18.7 節にあるように、一段階でエポキシドを与えると考えてよい。
いずれの方法でエポキシドを得る場合も、二重結合であった場所が3員環となる点では共通しているから、ここで異なるエポキシドが得られるとすれば、立体配置のみが問題となる。2つの架橋炭素を結ぶ-C(CH3)2- の橋のジメチル置換基が、二重結合に対して覆いかぶさるようになっていることに注目する。また、エポキシドを得る2つの方法が、臭素と酸素の違いはあるがはじめに3員環の中間体を経由している点にも注目して考える。
(解答例)
7,7-dimethylbicyclo[2.2.1]hept-2-ene において、7位のメチル基が 2,3 位の炭素間の二重結合に対して屋根のように覆っている構造をしているため、二重結合の π 電子に対する求電子的な反応は、あいているほうの面からしか起きないと考えられる。
従って、二重結合に臭素が付加して生じるブロモニウムイオン(3員環の中間体イオン)も、過酸を作用させて生じるエポキシド(3員環)も、同じように分子の下面に突き出すような構造になると予想される。
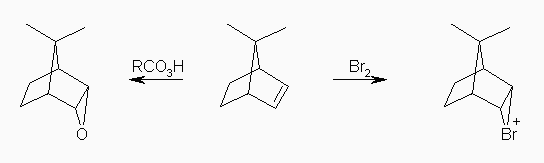
なお、臭素の付加では、π 電子により分極した臭素分子(Brδ+-Brδ-)から、Br+ が付加しているのに対し、極性溶媒中での過酸の処理では、形式的に「 RCO3H ←→ RCO3- + OH+ 」の平衡により生じた OH+ が付加するものと考えてもよい。( OH+ のルイス構造を描いてみること。酸素は、オクテットを満たしておらず、強い求電子種としてはたらくことがわかるはずである。)
ブロモニウムイオンは、水の酸素の孤立電子対より求核攻撃を受け、プロトンを脱離するとブロモヒドリンを与える。水酸基の水素を塩基で引き抜くことにより生じるアルコラート( R-O- )は、分子内で求核置換を行い、エポキシドを与える。
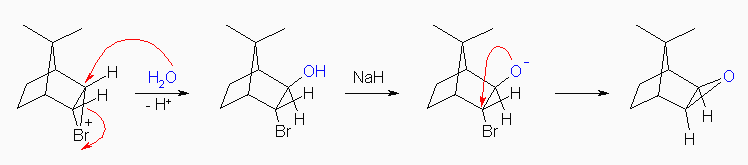
18.24
アルケンをアルカリ水溶液中、Br2 で処理すると、アルケンに対する臭素化の時と同じ三員環の中間体、ブロモニウムイオンが生じる。これに、水酸化物イオンが求核攻撃すると、ブロモヒドリンとなり、更にアルカリ性条件下なので、ブロモヒドリンよりプロトンが脱離し、分子内での求核攻撃によりエポキシドとなる。
このエポキシドは、もう一度水酸化物イオンにより求核攻撃を受けると、トランスの 1,2-ジオールを与える。この反応は、OsO4 との反応、もしくは冷アルカリ性での MnO4- との反応(いずれもシスの 1,2-ジオールを与える)と対比させて覚えること。
過酸での処理は、教科書 18.7 節にあるように、一段階でエポキシドを与えると考えてよい。
いずれの方法でエポキシドを得る場合も、二重結合であった場所が3員環となる点では共通しているから、ここで異なるエポキシドが得られるとすれば、立体配置のみが問題となる。2つの架橋炭素を結ぶ-C(CH3)2- の橋のジメチル置換基が、二重結合に対して覆いかぶさるようになっていることに注目する。また、エポキシドを得る2つの方法が、臭素と酸素の違いはあるがはじめに3員環の中間体を経由している点にも注目して考える。
(解答例)
1,7,7-trimethylbicyclo[2.2.1]hept-2-ene (慣用名 bornene ボルネン)において、7位のメチル基が 2,3 位の炭素間の二重結合に対して屋根のように覆っている構造をしているため、二重結合の π 電子に対する求電子的な反応は、あいているほうの面からしか起きないと考えられる。
従って、二重結合に臭素が付加して生じるブロモニウムイオン(3員環の中間体イオン)も、過酸を作用させて生じるエポキシド(3員環)も、同じように分子の下面に突き出すような構造になると予想される。
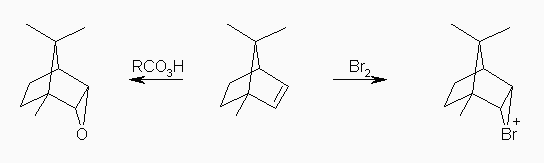
なお、臭素の付加では、π 電子により分極した臭素分子(Brδ+-Brδ-)から、Br+ が付加しているのに対し、極性溶媒中での過酸の処理では、形式的に「 RCO3H ←→ RCO3- + OH+ 」の平衡により生じた OH+ が付加するものと考えてもよい。( OH+ のルイス構造を描いてみること。酸素は、オクテットを満たしておらず、強い求電子種としてはたらくことがわかるはずである。)
ブロモニウムイオンは、水の酸素の孤立電子対より求核攻撃を受け、プロトンを脱離するとブロモヒドリンを与える。水酸基の水素を塩基で引き抜くことにより生じるアルコラート( R-O- )は、分子内で求核置換を行い、エポキシドを与える。
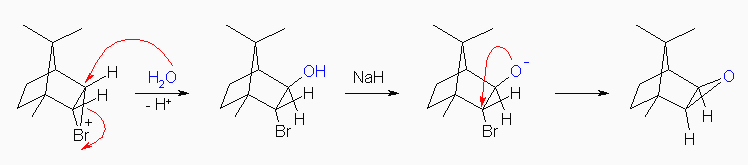
18.24, 25
アリル基の構造については、教科書 18.6 節の反応の例の中にでてくる化合物を参照すること。
(解答例)
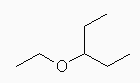
(a) ethyl 1-ethylpropyl ether, 3-ethoxypentane
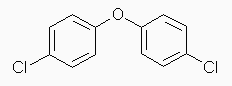
(b) di(4-chlorophenyl) ether
(c) 3,4-dimethoxybenzoic acid
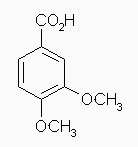
(d) cyclopentyloxycyclohexane, cyclohexyl cyclopentyl ether
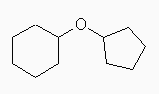
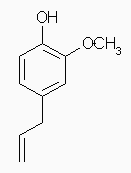
(e) 4-allyl-2-methoxyphenol
18.25, 26
含硫黄系の (a), (f),(g), (i) については、教科書 18.10 節を参照して命名する。
(c) はエポキシドとして、教科書 18.7 節を参照して命名する。また、(d) は環状エーテルを基本として命名する。ヒントは問題 18.6。
上記以外は、基本的には教科書 18.1 節にしたがって命名できる。問題 18.01 のヒントも参照すること。
(解答例)
(a) cyclohexyl isopropyl sulfide, isopropylthiocyclohexane
後者の命名では、アルキルオキシ基( RO- 基 )に相当する RS- 基をアルキルチオ基としている。
(b) 1,2-dimethoxybenzene
1,2- の代わりに o- を用いることも可。(o,o- ではない。)
(c) 1,2-epoxycyclopentane
(d) 2-methyltetrahydrofuran
(e) cyclopropyl isopropyl ether, isopropoxycyclopropane
後者のイソプロピルオキシ基は、短縮型 イソプロポキシ基として命名している。
(f) 2-nitrobenzenethiol
phenol に対して酸素が硫黄で置き換わったものは、benzenethiol となる。
(g) 2-isopropylthio-3,4-dimethylhexane
スルフィドとして命名するには、isopropyl 1,2,3-trimethylpentyl sulfide となる。この場合だと、3,4-dimethylhex-2-yl 基ではなく、1,2,3-trimethylpentyl 基とすることに注意。(アルキル基のねもとの遊離炭素を1位とするため。)
(h) 2,2-dimethoxypropane
(i) 1,1-dimethylthiocyclohexane
18.26, 27
次の順で、主に反応の位置選択性に注意して考える。
1) エーテルの中でも、エポキシドは環の歪みをもち、特殊な場合として考える。(エポキシドは、酸性でなくても求核攻撃により環開裂を起こす。また、中性~アルカリ性のときと、酸性のときでは位置選択性が異なる。
2) 第3級、アリル位、ベンジル位のエーテルであり、アルコールの脱離により安定なカルボカチオンが生じるかどうか。(その場合は、CF3CO2H や、HCl などの求核力の小さな酸でも酸開裂をおこす。)
3) それ以外のとき、エーテルの左右のアルキル基の求核攻撃の受けやすさは、SN2 反応の受けやすさと同じで、立体的にすいている方が優先される。ただし、ビニル位やベンゼン環上など、π 電子を持つ炭素上では置換が起こらないことにも注意する。
なお、酸性では、まずエーテル酸素のプロトン化により、-OR が -O+(H)R となることで脱離しやすくなると同時に、エーテル酸素隣接の炭素上の正の部分電荷が大きくなり、より求核攻撃を受けやすくなると考えられる。詳細は、反応機構(教科書 18.5 節)を参照のこと。したがって、HI を酸として用いた場合の求核種は、I- イオンである。
(解答例)
(a) cyclohexanol + iodoethane
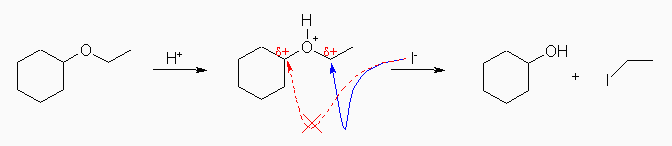
ヨウ化物イオン I- は、2級ではなく1級の炭素に求核攻撃する。
(b) phenol + 2-methylpropene (= isobutene)
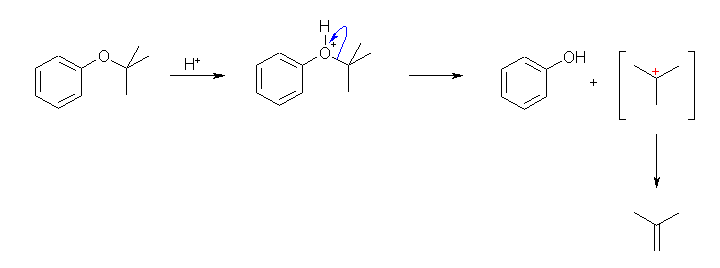
3級のエーテルなので求核性の無い酸でも開裂が起こる。プロトン化を受けたあと、3級のカルボカチオンと脱離した中性のアルコール(この場合はフェノール)になる。3級のカルボカチオンに対して、たとえば、ヨウ化物イオン I- による求核攻撃があれば 2-iodo-2-methylpropane などを生じる(SN1 反応)が、強酸であるトリフルオロ酢酸の共役塩基 CF3CO2- は求核性が弱いのでカルボカチオンからはプロトン脱離が起こる(E1 反応)。
(c) ethanal (= acetoaldehyde) + iodoethane
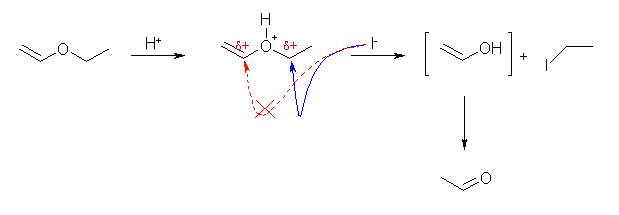
ビニル位の炭素は、π 電子を持つので、ヨウ化物イオン I- による求核攻撃を受けない。したがって、ビニルアルコールとヨードエタンが生じるが、ビニルアルコールはすぐに互変異性化(アルキンの水和:教科書 8.5 節を参照のこと)して、アセトアルデヒドを生じる。
(d) 2,2-dimethyl-1-propanol + iodoethane
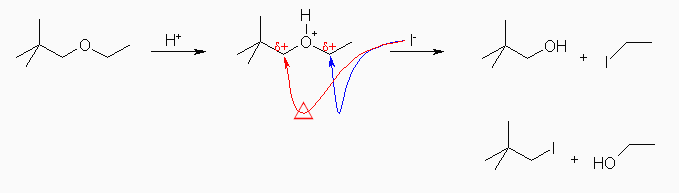
両方とも1級のアルキル基ではあるが、2,2-dimethylpropyl 基のエーテル酸素に隣接した炭素は、ethyl 基の場合にくらべて立体的に比較的混んでいるので、主として ethyl 基上にヨウ化物イオン I- による求核攻撃が起こる。
18.27, 28
(a)、(b)、(d) 通常、エーテルの合成のためには、大きく分けて、Williamson エーテル合成法を使う場合と、アルコキシ水銀化法のように二重結合にアルコールを付加させる場合の2通りが考えられる。それぞれの反応の適用範囲と限界について、整理しておくとよい。
(c) エポキシドの合成法にも、いくつかあるが、生成物および反応の立体化学を考えて出発物質を選ぶこと。
(e)、(f) は、いずれも同じ出発物質として、cyclohexene から合成できる。(e) の場合は2つのメトキシ基がトランスの位置関係にあること、(f) の場合は重水素 -D とメトキシ基がシスの位置関係にあることに注意して、反応を選択する。
(解答例)
(a)
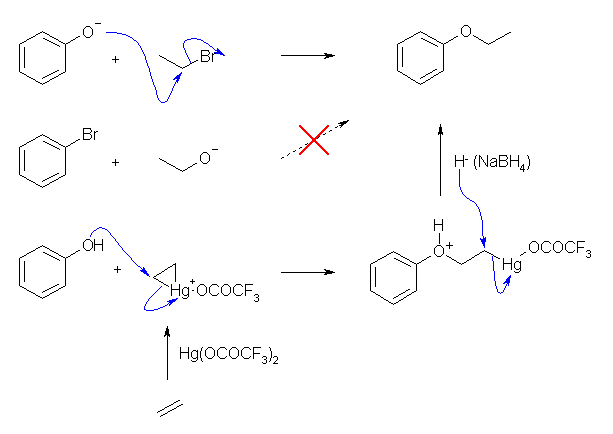
Williamson エーテル合成を用いる場合、ハロゲン化アルキルには、1級のハロアルカンを用いる。そのため、bromoethane や iodoethane などと、フェノキシドイオンとの反応となる。ハロゲン化ベンゼンは、sp2 炭素が π 電子を持っているため、ベンゼン環上では求核置換反応がおきない(*)ため、目的とするエーテルは合成できない。
アルコキシ水銀化法でも、このエーテルは合成することができる。マーキュリニウムイオンの3員環炭素のうち、どちらにフェノールからの求核攻撃が起きても、同じ生成物となる。
(b)
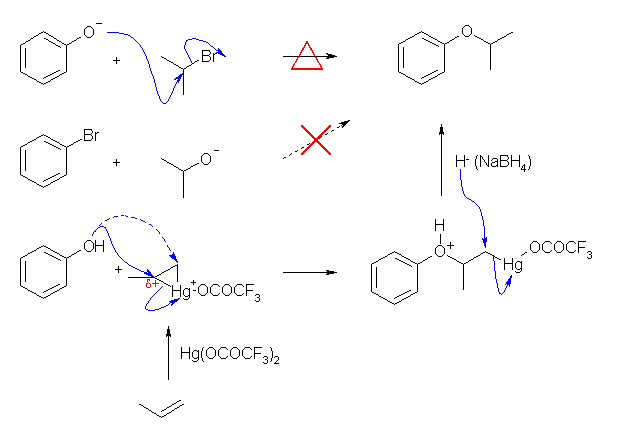
Williamson エーテル合成を用いる場合、ベンゼン環上では求核置換反応がおきない(*)ため、フェノキシドイオンと2級のハロアルカンを用いることになる。SN2 反応なので、(a) のように1級のハロアルカンを用いた場合と比較すると、反応しにくくなっている。
アルコキシ水銀化法でも、このエーテルは合成することができる。この反応の位置特異性は、マーキュリニウムイオンの3員環の炭素のうち、(カルボカチオンの安定性で説明されるように)より多くのアルキル基で置換された方により大きな正の部分電荷があるため、マルコフニコフ配向に従う。
(c)
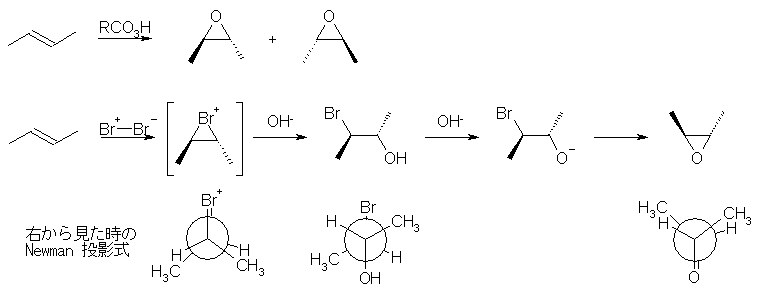
エポキシドの形成反応は、過酸を用いた場合一段階の機構で進行するので、シン付加となる。そのため、trans-体のアルケンを出発物質とすると、trans-体のエポキシドが得られる。
ただし、通常の均一系の条件では、光学異性体である (2R,3R)-2,3-epoxybutane (図、左)と (2S,3S)-2,3-epoxybutane (図、右)は、作り分けることはできない。光学異性体の両方を示すことはしないがが、以下とも事情は同じである。
また、cis-体のアルケンを出発物質とすると、cis-体のエポキシドが得られる。左右の置換基が同じである場合は、cis-体のエポキシドは meso-体なので光学異性体を持たない。
ハロヒドリンを経由してエポキシドを合成する場合も、trans-体のアルケンを出発物質としたとき、ブロモニウムイオンはエポキシドと同様の立体で生成し、水酸化物イオンによる背面攻撃をうけてブロモヒドリンを生じるから、臭素と水酸基がアンチの立体で付加しているとみなせる。更に塩基により生じたアルコキシドによる分子内の求核置換でも、臭素の背面攻撃により起きるので、、トータルとして過酸による処理の時と同じように、シン付加でエポキシドが生じているとみなせる。
(d)
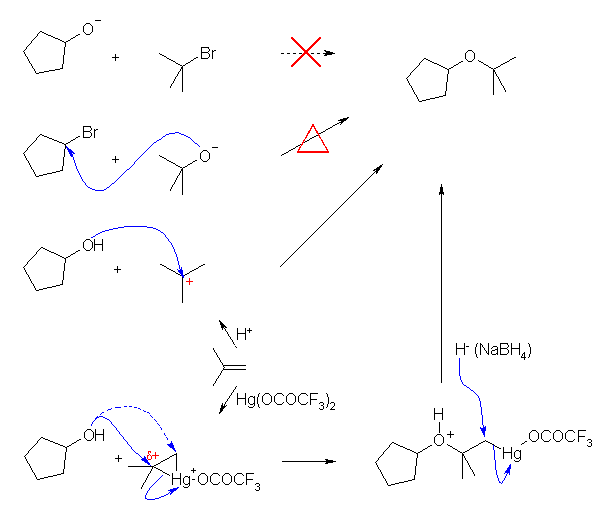
Williamson エーテル合成を用いる場合、3級炭素上では SN2 反応がおきない(競争する脱離反応により、2-methylpropene (= isobutene ) を与える)ので、tert-ブトキシドイオンと2級の環状ハロアルカンを用いることになる。SN2 反応なので、(a) のように1級のハロアルカンを用いた場合と比較すると、反応しにくい。( cyclopentene を与えるような脱離反応が競争する。)
このエーテルはアルコキシ水銀化法で合成することができる。この反応の位置特異性は、マーキュリニウムイオンの3員環の炭素のうち、(カルボカチオンの安定性で説明されるように)より多くのアルキル基で置換された方により大きな正の部分電荷があるため、マルコフニコフ配向に従う。
また、3級のカルボカチオンは安定であるため、HCl や CF3CO2H などの求核性の小さな酸の存在下、2-methylpropene (= isobutene ) から生じたカルボカチオンに対し、cyclopentanol を作用させることでも合成可能である。(この反応は、アルケンに対する水和反応と類似の形式である。)
オキシ水銀化法による水和が、酸による水和と比べて優れている点は、カルボカチオンを経由しない(代わりにマーキュリニウムイオンを経由する)ので、カルボカチオンに典型的な反応であるところの転位反応をおこさないことである。(どちらもマルコフニコフ配向に従い、生成物は同じである。)上図中で生じているカルボカチオンは3級で安定であり、転位により別の構造のカルボカチオンに変化してしまう可能性も低いので、わざわざアルコキシ水銀化法を用いる必要はない。
(e), (f)
シクロヘキセンを出発物質としたいくつかの反応スキームを描いておいた。それぞれ、どのような位置特異性、立体特異性で進行しているのかを確認しておくこと。反応に際し、シクロヘキサン環の炭素上で SN2 反応が起こり、炭素の立体の反転する反応は、図中、赤色の矢印で示し、それ以外の場所で SN2 反応が起こるためにシクロヘキサン環上の炭素の立体が保持される反応は、図中、青色の矢印で示した。
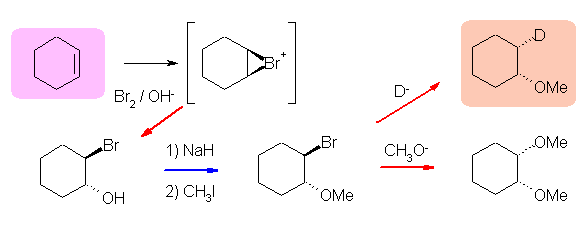
アルカリ性条件下、臭素と反応させるとブロモヒドリンが生じる。水酸基をアルコラートにしたのち、ヨードメタンと反応させることで(アルコラートによる求核攻撃がヨードメタン上で起き、ヨウ化物イオンが脱離する)メチルエーテルが生じる。続いて、シクロヘキサン環上に残ったハロゲンに対し、各種、求核試薬により SN2 反応させることでシンの立体で付加した生成物として得られる。ここで、 D- を与えるような試薬とは、LiAlD4 のようなものである。
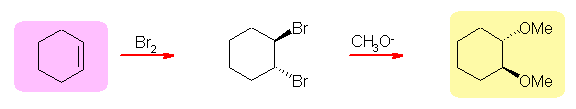
アルケンの臭素化は(上のハロヒドリン経由のスキームでも示したような)ブロモニウムイオンを経由して、アンチ付加をするため、トランス体を与える。このハロゲン化アルキルに対してメトキシドイオンが SN2 反応すれば、トランス体で 1,2-ジメトキシシクロヘキサンが得られる。しかし、実際には、ハロゲン化アルキルが環状、かつ2級であるから、容易には進行せず、臭素化されたことで、その炭素上の水素の酸性度があがっていることもあり、メトキシドイオンが求核試薬ではなく塩基として働き、脱離反応が競争して 1-bromocyclohexene などを与える可能性がある。
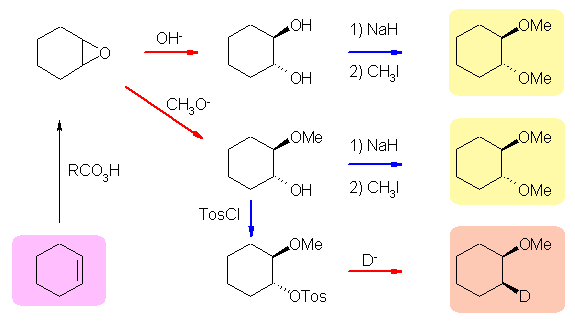
cyclohexene より、過酸との処理により、1,2-epoxycyclohexane を合成できる。(ハロヒドリン経由でも同じように合成できる。)エポキシドは、水酸化物イオンとの処理により、トランスの 1,2-ジオールを与えるので、これらのアルコールをメチル化することで、目的とする trans-1,2-dimethoxycyclohexane を得ることができる。なお、この反応は、上の trans-1,2-dibromocyclohexane に対する求核反応に比べて、ハロゲン化アルキルが1級であり、穏やかな条件で反応させることができる。
また、エポキシドは、水酸基の代わりにメトキシドを求核試薬として用いると、一方の水酸基のみがエーテル化されたものを得ることができる。ここでは、続いて残った水酸基をメチル化しているが、非対称な化合物(一方がメトキシ、もう一方がフェノキシであるようなもの:ただし、一方がフェノキシの場合はヨウ化フェニルは反応しないから、はじめにフェノキシドイオンによる求核反応をしなければならない)を得たい場合にも、このルートを使うことが可能である。
アルコールのメチル化は、アルコラートとした後ヨードメタンなどで処理することで、水酸基の根元の立体を保持して進行する。
水酸基をトシル化すると(塩化トシルを用いたとき、アルコール酸素がトシル基の硫黄上で求核反応するため)水酸基の根元の炭素の立体を保持したまま、水酸基 -OH を脱離基 -OTos に変換することができる。(塩化チオニルによる塩素化も、SNi 機構で進行するので、立体を保持したまま脱離基に変換できる。ただし、pyridine 存在下では、塩化チオニルとの反応も、SN2 機構で進行するため、立体が反転する。)次に求核試薬を作用させ、シクロヘキサン環上で SN2 反応をおこせば、シス-トランスの反転した生成物が得られる。
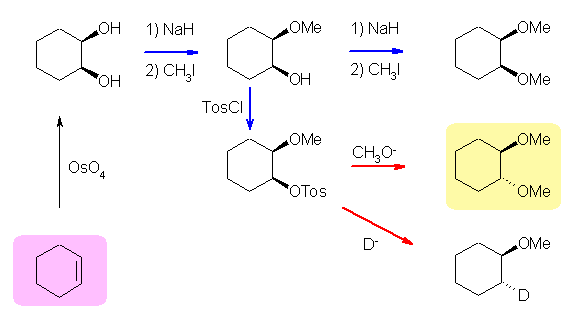
エポキシドが、水酸化物イオンとの処理により、トランスの 1,2-ジオールを与えたのに対応して、アルケンは四酸化オスミウムや、冷アルカリ性条件下の過マンガン酸カリウムとの処理により、シスの立体配置で 1,2-ジオールを与える。これをそのままエーテル化すると、cis-1,2-dimethoxycyclohexane を得ることになるから、エーテル化を途中で止めて(と言っても、2つの水酸基の反応性にはほとんど差が無いと考えられ、選択的にモノエーテル化することは難しいので、混合物をなんらかの方法で分離することになるはずである)から、残った一方の水酸基はトシル化し、SN2 反応で立体を反転させてやれば、trans-体となるはずである。
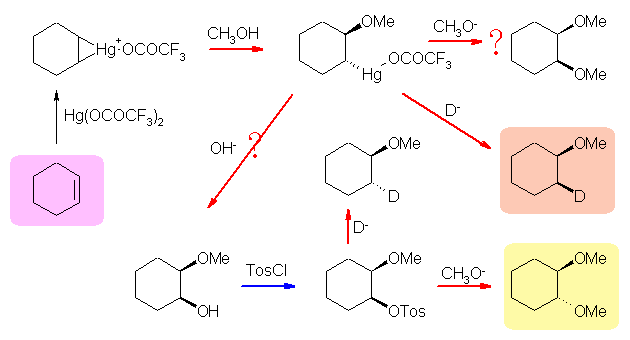
トリフルオロ酢酸水銀を用いると、3員環のマーキュリニウムイオンを中間体として生じるから、これをアルコールで処理すると(エポキシドやブロモニウムイオンのときと同じ立体で反応は進行し、)求核的な開環反応によりトランスの立体配置をもつ有機水銀付加生成物を与える。アルコキシ水銀化法では、ヒドリドによる求核置換反応により、この炭素-水銀結合を切るが、ヒドリド以外の求核試薬でも同様の SN2 反応できるなら、炭素-水銀を、水素以外で置き換えることができると期待される。(上スキーム中、?で示した反応。ただし、ここまでの教科書に、これらの ? の反応が進行するという記述はない。)
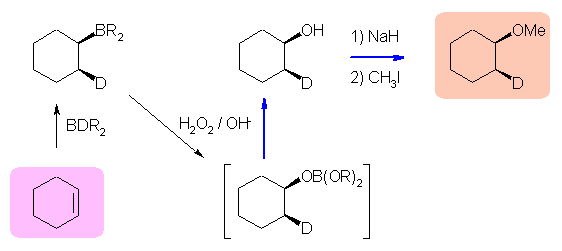
アルコキシ水銀化法と、ヒドロホウ素化反応は、逆の位置選択性を持つから、いつもこれらをペアで考えなければならない。ここでは、(f) の目的生成物中に、重水素 D が含まれているから、上スキーム中でヒドロホウ素化剤として、BHR2 の代わりに BDR2 を用いている。具体的な試薬としては、たとえば重水素化ジボラン BD3 や、重水素化 9-BBN などを用いることができる。
ヒドロホウ素化反応では、(接触水素添加や、四酸化オスミウムなどと同様に)シンの立体配置で付加が起きる。次いで、アルカリ性の過酸化水素で処理することにより、その立体配置を保ったまま炭素-ホウ素結合がアルコールに変換される(次図、* 印炭素)。この反応は、HOO- が、ルイス酸であるホウ素(13族元素で、3配位の化合物を作って、中性で荷電子が6個である。)に求核的に付加し、次いでアルキル基がホウ素に隣接した酸素上に転位、水酸基が脱離する反応により、ホウ酸のエステルを生じる。アルカリ性でこれを加水分解することにより、ホウ酸(の塩)とアルコールを生じる。
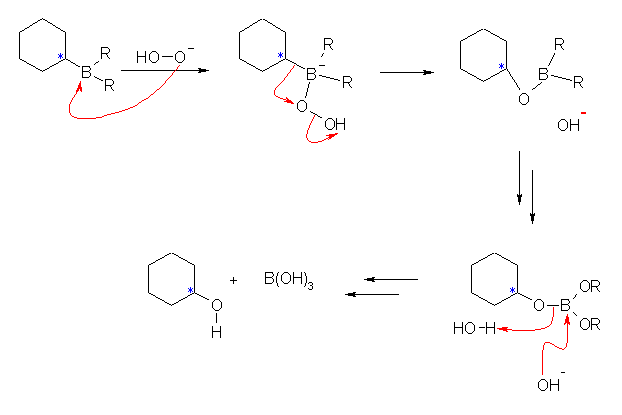
この問題のように立体配置が問題になる場合には、SN1 反応を用いることはできない。たとえば、重水素化された臭化水素 DBr を用いても、はじめにカルボカチオンを生じてしまう条件では、カルボカチオンの中心炭素は SP2 混成で平面3配位形であるから、ジアステレオマーの混合物が得られてしまう。
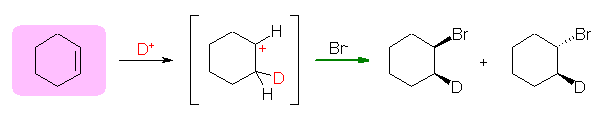
(*) ベンゼン環上での求核置換反応の例外は、以下のとおり。
1) ベンゼン環上に、複数のニトロ基が置換されるなど、 π 電子密度が下がっている場合。
2) 脱離基が N2 であるなど、特別に脱離しやすい系である場合。
3) 上 1), 2) に該当しないが、特に強い塩基を用いた場合。(benzyne 機構で進行する。)
18.28, 29
出発物質として指定されている 1-phenylethanol の構造、および目的生成物の構造を示し、その構造の差から、どの部分でどんな反応が起きているのかを考えること。
それぞれの目的生成物の名称を、英語でも示しておく。
(a) methyl 1-phenylethyl ether (b) phenylepoxyethane (2-phenyloxirane) (c) tert-butyl 1-phenylethyl ether (d) 1-phenylethanthiol
(解答例)
反応条件と、スキームを示す。
(a) 1) NaH, 2) CH3I
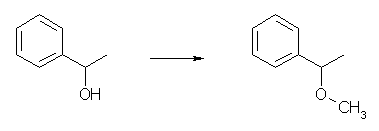
Williamson エーテル合成
(b) 1) POCl3-pyridine, 2) RCO3H
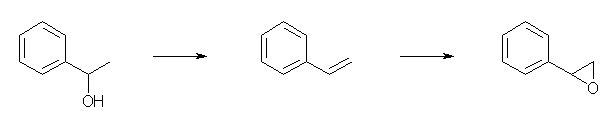
ピリジン存在下のオキシ塩化リンによる処理は、アルコールの脱水反応。教科書 17.7節を参照のこと。反応機構は、図 17.6 にある。
(c) 2-methylpropene, HCl(cat.)
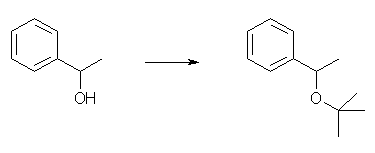
tert-bytyl bromide との Williamson エーテル合成は起きない。したがって 2-methylpropene への付加で合成する。アルコキシ水銀化法の条件( 1) 2-methylpropene, Hg(COCF3)2, 2) NaBH4 )でも合成可能である。
(a),(c) 1-phenylethanol を脱水により phenylethene (= stylene) としたのち、各種アルコールをアルコキシ水銀化法などにより付加させることでも、目的とする化合物が得られる。
(d) 1) PBr3, 2) (H2N)2C=S, 3) OH- / H2O
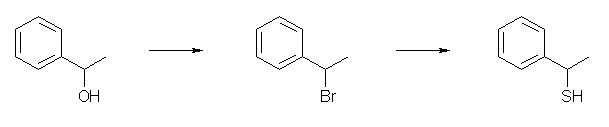
ハロゲン化アルキルとしたのち、チオウレアで処理する。水硫化物イオン SH- での処理では、一度生じた RSH が、別のハロゲン化アルキルと反応して、スルフィド RSR を副生してしまうため、あまり好ましくない。
18.29
(b)~(d) は、教科書 18.10 節を参照すること。
(解答例)
ここでは生成物の名称のみ与えるが、解答作成時には必ず生成物の構造を併記すること。
(a) phenol + 1-bromo-2-methylpropane
プロトン化の後の求核反応は1級アルキル基側のみで起こり、π 電子を持つフェニル基上では起きないから、bromobenzene は生じない。
(b) 4-methylpentane-1-thiol
(c) dicyclopentyl disulfide
(d) ethyl 3-cyclohexenyl sulfoxide
18.30, 30
(a) 二重結合にアルコールが付加している。→ アルコキシ水銀化法
(b) メトキシ基が臭素に置換されているが、炭素の立体が反転している。SN2 反応を1回経由している。
(c) 二重結合の位置が隣接ジオールになっているが、その立体化学はトランスである(アン付加の形である)。→ 四酸化オスミウムや(冷・アルカリ性)過マンガン酸カリウムなどによる処理ではない。
(d)、(e) 三重結合の位置にエーテルが導入されている。三重結合は、対応する二重結合に変換してやることができることを思い出すこと。ただし、エーテル基の導入位置が異なることから、異なる位置選択性を持つ反応を使い分けることになる。
(解答例)
(a) 1) Hg(COCF3)2, 2) isopropanol (= propan-2-ol), 3) NaBH4
(b) 1) HI / H2, 2) PBr3
はじめのエーテル開裂では、プロトン化後の求核攻撃はメチル基側で起きるため、シクロヘキサン環炭素の立体は保持である。PBr3 による反応は、SN2 で進行するためこの炭素の立体は反転する。
(c) 1) RCO3H, 2) OH- / H2O
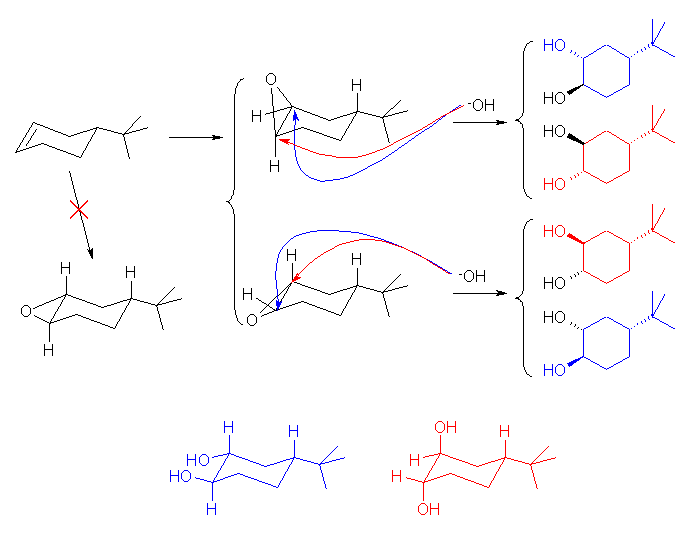
はじめのエポキシ化ではシンの立体化学で付加し、2種のジアステレオマーの混合物となると予想される。次いで、求核的な開環反応によりトランスの立体配置をもつ 1,2-ジオールを生じるが、この際エポキシ環の両炭素はアルキル基による置換の度合いが同じであるから、位置選択性に差がほとんどないと仮定すると、上図に赤で示したものと青で示したものの2種類のジアステレオマーの混合物が得られる。

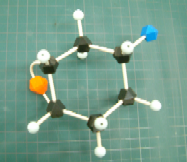
上スキームで生じる、4-tert-butyl-1,2-epoxycyclohexane の2種のジアステレオマーのうち、下方のものの構造を分子模型で組み、写真を載せた。青で示されているのが tert-ブチル基と思って欲しい。オレンジ色に見えるのがエポキシ酸素とする。左は側面から見た図、右はアキシャル方向から見た図である。なお、tert-ブチル基は、1,3-ジアキシャル相互作用が大きいので、ほとんどすべての分子においてエカトリアル位にある配座をとる。
上スキームの赤矢印で示した求核攻撃は、アキシャル水素が邪魔になって起きにくいと予想される。(2位の炭素原子のエポキシ酸素のちょうど裏面というのは、シクロヘキサン環の内側、5位の炭素の方向であり、環の構造が邪魔して攻撃が起きにくい。)これに対し、青で示した求核攻撃は、2位の炭素原子のエポキシ酸素のちょうど裏面がアキシャル方向で、この方向は比較的空いているので求核攻撃が起きやすいと予想される。…のだが、与えられた答え(1位と4位がシスであるようなもの、すなわち上図では赤の構造)と逆の立体配置のものが多く生じるという予想になってしまった。(-_-; 「2つの水酸基がトランスの関係になる」ということだけは押さえておいてください。tert-ブチル基を持つシクロヘキサン環や、trans-デカリンのように環反転の無いシクロヘキサン環系での求核反応の立体化学については、引き続き調べておきます。
(d) 1) H2 / Lindlar catalyst, 2) BH3, 3) H2O2 / OH-, 4) NaH, 5) CH3I
はじめに 1-hexene としたのち、ヒドロホウ素化により 1-hexanol を得る。これをエーテル化すればよい。
(e) 1) H2 / Lindlar catalyst, 2) Hg(OCOCF3)2, 3) CH3OH, 4) NaBH4
はじめに 1-hexene としたのち、オキシ水銀化法により 2-hexanol を得たのち、これをエーテル化してもよい。
18.31-18.40 (31-38)
18.31, 31
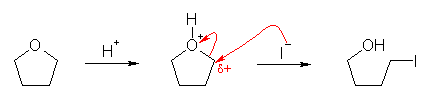
エーテル酸素のプロトン化の後、隣接した炭素上に I- が求核攻撃し、SN2 で進行する。
(解答例)
HO-CH2CH2CH2CH2-I, ( 4-iodo-1-butanol )
18.32, 32
目的生成物を与えるために必要なパーツは何かを考え、そのパーツをベンゼンから合成することを考える。benzyl 基は、PhCH2- の構造を持つ。benzyl phenyl ether では、Williamson のエーテル合成法を用いることが可能であるが、反応に用いることが可能なハロゲン化物は一方のみである。
(解答例)
最終段階は、次の反応となる。
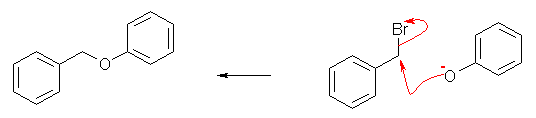
この原料となる、フェノールおよび臭化ベンジル(benzyl bromide)は、以下の合成ルートで得られる。
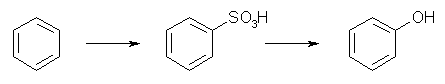
濃硫酸中でスルホン化、水酸化ナトリウムの溶融反応によりフェノールとする。教科書 17.10 節参照。
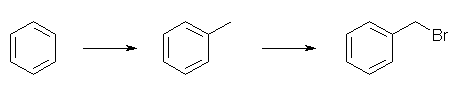
Friedel-Crafts のアルキル化(CH3Cl, AlCl3)によりトルエン(PhCH3, toluene)としたのち、ベンジル位のハロゲン化(NBS, BPO)を行う。教科書 16.3 節、16.10 節参照。
ただし、Friedel-Crafts のアルキル化では、反応生成物の方が、弱い電子供与性基であるアルキル基を余計に持つ分だけ π 電子の密度が上がり、芳香族求電子置換反応に対する活性があがるから、一般的にモノ置換体であるトルエンでは反応がとまらず、2置換体であるキシレンやトリメチルベンゼンなどの混合物が得られる。これを避けるためには、次のようなルートを取ると良い。
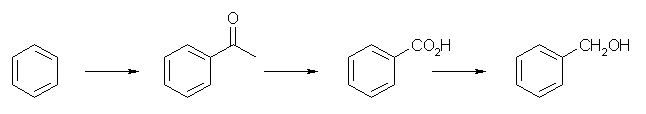
Friedel-Crafts のアシル化では、新たに導入されるアシル基( RCO- )が電子吸引性基であるから、生成物は出発物質であるベンゼンに比べて芳香族求電子置換反応に対する活性が下がる。このため、Friedel-Crafts のアシル化はモノ置換で止まる。
ベンゼンに acetyl chloride ( CH3CO-Cl )を、AlCl3 存在下反応させ、アセトフェノン( PhCOCH3 )とする。側差を酸化して安息香酸(benzoic acid)に変換する条件はいくつかある(教科書 16.10 節参照)が、メチルケトンに特有の反応として、比較的穏やかな反応条件( I2, NaOH aq )で進行するハロホルム反応(教科書 22.8 節参照)を用いることもできる。安息香酸は(通常、エステル化の段階を経てから LiAlH4 を作用させて)還元することにより、ベンジルアルコールが得られる。これを PBr3 と処理することで臭化ベンジルとすることができるほか、ベンジルアルコールをエステル化(トシル化、あるいはアセチル化)により水酸基を脱離基(TosO- や AcO- は、酸 TosOH (トルエンスルホン酸)、AcOH(酢酸)の共役塩基なので、水酸化物イオン(水の共役塩基)にくらべて脱離しやすい)に変えてもよい。
18.33, 33
出発物質の構造式を書いてみよ。一方のアルコールは1級で、もう一方のアルコールは3級である。硫酸で処理するときに、アルコール酸素がプロトン化を受ける。これにより脱水するのは、いずれかを考えよ。
硫酸は、(その共役塩基が)あまり求核性を持たない酸として考えてよい。
(解答例)
以下に示したすべての課程は、可逆である。ただし、次のスキーム中では出発物質に対応する番号を示しているが、カルボカチオンやテトラヒドロフラン環を形成している場合の命名上の番号付けは下図とは異なる。
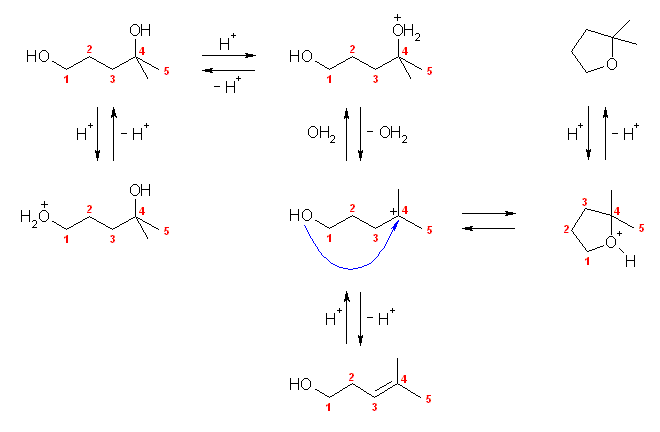
4-methylpentane-1,4-diol は、2つの水酸基を持つ。1級のアルコール(1位の水酸基)はプロトン化されても、求核試薬がなければ SN2 反応せず、また脱離もしない(対応するカルボカチオンが1級で安定ではないため)。したがって、プロトン化したアルコールはプロトンを失ってもとの形に戻る反応しか示さない。その一方、3級のアルコール(4位の水酸基)はプロトン化されると、求核試薬がなくても自発的に水を脱離し、3級で安定なカルボカチオンを生じる。続いて、カルボカチオンに対して、分子内の水酸基による求核攻撃が起きると、プロトン化された環状エーテルを生じる。3級のエーテルなので、酸開裂もまた求核種なしに起こり、可逆である。
全体として、分子内の SN1 機構で 2,2-dimethyltetrahydrofurane を生じるといえる。上のような機構で起きるため、酸素は3級のアルコール(4位の水酸基)より脱離する。
18.34, 14
cis-5,6-epoxydecane の構造は次のとおり。

この酸性加水分解では、エポキシ酸素にプロトン化を受けたあと、水が求核剤としてはたらく。
(解答例)

正常な背面からの SN2 反応により、C-O+結合が切れて、一方の炭素上でワルデン反転を起こすので、cis-5,6-decanediol のラセミ混合物、すなわち、(5R,6R)- および、(5S,6S)-5,6-decanediol の等量混合物が得られる。

のように生成物の構造を書いてもよい。
18.35, 15
trans-5,6-epoxydecane の構造は次のとおり。

この酸性加水分解では、エポキシ酸素にプロトン化を受けたあと、水が求核剤としてはたらく。
(解答例)

正常な背面からの SN2 反応により、C-O+結合が切れて、一方の炭素上でワルデン反転を起こすので、trans-5,6-decanediol (または、meso-5,6-decanediol )が得られる。((5R,6S)-体および、(5S,6R)-体は同一であることに注意。)

のように生成物の構造を書いてもよい。
18.36, 34
アニソール anisole は、phenyl methyl ether の慣用名。DMF ジメチルホルムアミド は、(CH3)2NCHO の示性式をもつ非プロトン性の高極性溶媒で、イオン性化合物、共有結合性化合物を問わず、多くの無機・有機化合物を溶解する。水とは異なりアニオンを強くは溶媒和しないので、そのアニオンの求核力が強くなり、SN2 反応が速くなることが知られている。
Li-I から生じる I- が求核剤として働く。起きる反応は、SN2 で進行する。脱離基は、酸によるエーテルの開裂の場合とは異なり、フェノキシドイオンである。
(解答例)
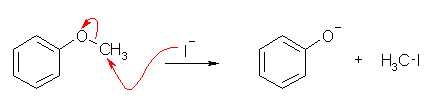
DMF ジメチルホルムアミド中では、エーテルがプロトン化を受けていないまま、水溶液中よりも強い求核性を示す I- によって求核攻撃を受け、隣接炭素上で SN2 反応が進行する。
ヒントおよび発展を参照しておくこと。
SN2 反応であるからメチル基上では起こるが、ベンゼン環上では進行しない。
Li+ イオンは、H+ と同様にルイス酸であるが、この反応では、反応に関与しないものとして考えても上記反応は説明できる。
エーテルの酸開裂において、プロトン化を受けたエーテルの隣接炭素への求核攻撃により脱離するものは、中性のアルコール分子(R-OH)であるが、同じルイス酸である Li+ に配位したエーテル酸素の隣接炭素に求核攻撃があっても、脱離するものは塩(R-O-・Li+)となるので、形式的には R-O- が抜けるものとして考えてもあまり変わらない。また、このような脱離がおきるのはイオンが十分に安定化されるような高い極性をもつ溶媒のときのみであるが、同時にこのような溶媒中では、Li+ イオン自体も溶媒和されると考えられるので、ルイス酸としてエーテル酸素に結合していないかもしれない。
本当に Li+ イオンが反応に関与しているかいないかを知るためには、DMF中で、LiI、NaI、KI など、種々の塩によるアニソールの開裂反応を調べ、陽イオンの効果があるかないかを調べる必要がある。
18.37, 35
この反応は、アルコキシ水銀化法でも達成できる。これは、アルケンへの水の付加が、単なる酸性条件下で水を付加させる場合も、オキシ水銀化法でも、どちらでも達成可能であったことと類似である。
酸触媒から供給される H+ は、(正の電荷をもつから)求電子的に振る舞い、アルケンの、π 電子をもつ炭素に付加していく。その結果、カルボカチオンを生じる。特にこのカルボカチオンの安定性によりきまってくる反応の位置特異性を、「マルコフニコフ配向性」と呼んだ。
問い 18.27(d), 18.33 の解答例および解説も参照すること。
(解答例)
以下に示したすべての課程は、可逆である。
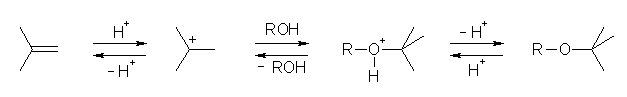
HCl や CF3CO2H などの求核性の小さな酸の存在下、2-methylpropene (= isobutene ) のプロトン化により、安定な3級のカルボカチオンを生じる。このカルボカチオンにアルコールを作用させると tert-ブチルエーテルを合成可能である。(この反応は、アルケンに対する酸性条件下の水和反応と類似の形式である。)
18.38, 36
第5版では、Meerwein 試薬の構造式が間違っている。「テトラフルオロホウ酸トリエチルオキソニウム」が試薬名であるから、Et2O+BF4- は間違い。正しくは Et3O+BF4-。
Meerwein 試薬によるアルコールの O-エチル化反応は、Meerwein 試薬のエチル基炭素上で起きている SN2 反応である。
SN2 反応が起きやすいための条件等については、教科書 11.5 節等を参照すること。求核種の反応性(中性のアルコールは中性の水と同様に、さほど、大きな求核性はないとおもわれる。)、求核攻撃を受ける炭素の立体(Meerwein 試薬のどの炭素に求核攻撃がおきているか。)、脱離基の脱離しやすさ、等について考えること。
(解答例)
アルコラートとヨウ化アルキルの反応( Williamson エーテル合成)
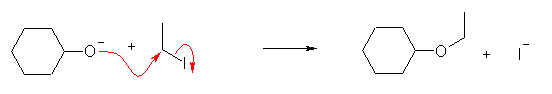
中性のアルコールと Meerwein 試薬の反応
生じたプロトン化エーテルは、プロトンを失い、シクロヘキシル エチル エーテルを与える。
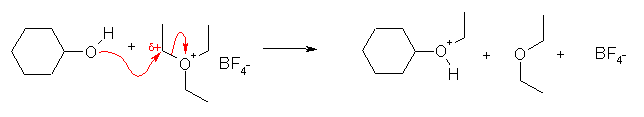
求核試薬の求核性は、アルコラート >> 中性のアルコールである。このため、1級、または2級のヨウ化アルキルは中性のアルコールとは反応しない。Meerwein 試薬は、より求核性の劣る中性のアルコールとも反応する。
求核攻撃の受けやすさには、立体的な要因と電子的な要因がある。立体的には、ヨウ化エチルも、Meerwein 試薬もほとんど同じであると考えられる。電子的な要因として、ヨウ化エチルは電気陰性度の高いハロゲン(ヨウ素)によって炭素上にやや正の部分電荷が生じているのに対し、Meerwein 試薬では形式電荷+の酸素により、隣接した炭素上に正の部分電荷が生じていると考えられる。これは、プロトン化を受けたエーテルが求核攻撃を受けやすくなっているのと同じである。
求核攻撃を受けたあとの脱離について考えると、ヨウ化アルキルからは、ヨウ化物イオン( I- )が脱離するのに対し、Meerwein 試薬からは中性のジエチルエーテルが脱離する。どちらも十分に強い脱離基であると考えられる。これは、プロトン化を受けたエーテルが求核攻撃により中性のアルコールを脱離したり、プロトン化を受けたアルコールが求核攻撃により中性の水を脱離したりするのと同じように起こりやすい過程である。

ここで、1級または2級のエーテルでは、求核性のない酸を用いた場合、酸性にしてもエーテルの開裂が起きないことを思い出さなければならない。(もちろん、アルコール中で酸性にしても、エーテルはアルキル基の交換を起こさない。)すなわち、プロトン化されたエーテルでも水分子による求核置換を受けない。Meerwein 試薬とプロトン化ジエチルエーテルのエチル基炭素の立体および電子的な要因、および、中性のアルコールと中性の水が持つの持つ求核性が、それぞれほぼ同じであると仮定して考えると、Meerwein 試薬でのみ反応がおきるのは、脱離基の脱離能が効いていると考える必要がある。すなわち、中性のアルコールより、中性のジエチルエーテルの方がさらに脱離性が高いと予想できる。
18.39, 37
原料の 1,2-benzenediol と構造を比較すると、反応は2つの段階が必要である。
酸素原子を2つ含むサフロール safrole の5員環は、環状のエーテルの構造であると理解することが可能である。したがって、エーテル合成の条件を応用できる。
ベンゼン環上にアリル基を結合させる段階は、Friedel-Crafts 反応(芳香族求電子置換反応、教科書 16.3 節参照)が利用できる。Friedel-Crafts アルキル化反応では、一般に、炭素数3以上の直鎖アルキル基を導入することはできなかった。これはなぜか。そして、アリル基の場合はどうであるのか。
(解答例)
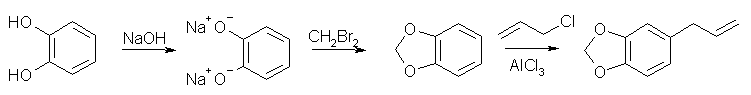
1,2-benzenediol は水酸基がフェノールと同程度の酸性を示すと考えると、水酸化ナトリウムで十分に塩にすることができる。このフェノキシドを求核試薬として、ハロゲン化アルキルには CH2Br2 を用いると、環状のエーテルを形成する( benzo[1,3]dioxole )。
次いで、ハロゲン化アリルと触媒量の塩化アルミを作用させると、Friedel-Crafts のアルキル化反応により、アリル基が導入される。
Friedel-Crafts のアルキル化反応では、はじめにハロゲン化アルキルからカルボカチオンを生じるから、たとえば 1-chloropropane のように1級のハロゲン化アルキルを用いても、生じたカルボカチオンは水素が転位して2級のカルボカチオンとなって、これがベンゼン環上に芳香族求電子反応して isopropylbenzene (= cumene )を生じるが、
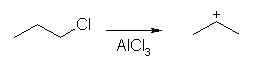
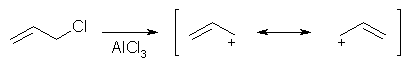
塩化アリルから生じるアリルカチオンは、その共鳴構造からも明らかなように 1,3 位の両炭素上に正電荷が分布し、したがってアリル基が導入される。
18.40, 38
LiAlH4 による反応は、ヒドリド還元である。すなわち、H- による求核反応であると理解できる。
問い 18.22 の解答も参考とすること。
(解答例)
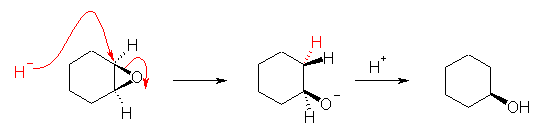
ヒドリド H- の求核攻撃により、歪みの大きなエポキシ環が開環する。
18.41-18.50 (39-48)
18.41, 39
重水素化リチウムアルミニウム、LiAlD4 による反応は、D- による求核反応であると理解できる。問い 18.40 では、ヒドリドの求核攻撃により新たに導入された水素を、分子内にあったほかの水素と明確に区別しなくても生成物の構造を考えることができたが、この問題では、反応の立体化学に気をつける必要がある。
とはいえ、別にあらたなことがあるわけではなく、エポキシドに対する求核攻撃という共通項で括って理解してよい。たとえば、エポキシドに対して、水酸化物イオン OH-を付加させて 1,2-ジオールを得る反応と同様に考えてよい。
(解答例)
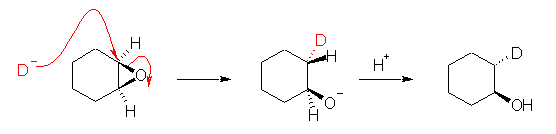
D- の求核攻撃により、歪みの大きなエポキシ環が開環する。生成物の -D と -OH の立体配置は、トランスとなる。
18.42, 40
cis-3-tert-butyl-1,2-epoxycyclohexane は、tert-butyl 基と、エポキシドの3員環が、シクロヘキサンに対して同じ方向(アキシャル、エカトリアルではなく、環の上下)に出ている立体配置を持つ。tert-butyl 基は、アキシャル位にくることができないほど嵩高いからエカトリアル位にあり、したがってエポキシドの3員環も、次の構造式のような配座をとる。
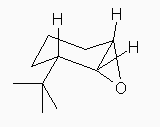
反応の位置選択性: このエポキシドは、3員環の炭素はいずれも2級であるから(3級ではないので)炭素上の部分電荷にもさほど差がなく、また、炭素の上の置換基から来る立体要因でもどちらが求核攻撃を受けやすいかにはあまり差が無いとおもわれる。仮に反応の位置選択性が生じるなら、tert-butyl 基より遠い方の炭素への求核攻撃が若干優先するかもしれない。
反応の立体特異性: 問題文にもあたえられているように、酸触媒存在下での求核攻撃による環の開裂では、ジアキシャルの trans-1,2-ジオールを与える。これは、ちょうど逆反応にあたる脱離反応においてアンチ脱離が優先的に起きたことと対応している。
(解答例)
cis-3-tert-butyl-1,2-epoxycyclohexane の構造を分子模型で組んでみた。青色は tert-butyl 基だと思ってください。
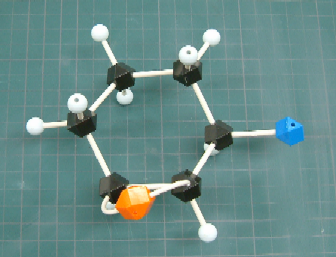
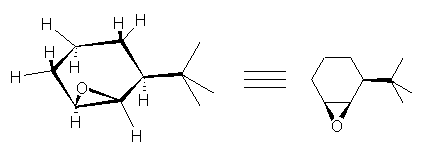
さて、このエポキシドにプロトン化したのち、水分子による求核攻撃が起こり、環が開く。この機構は、次のスキームのように描くことができる。
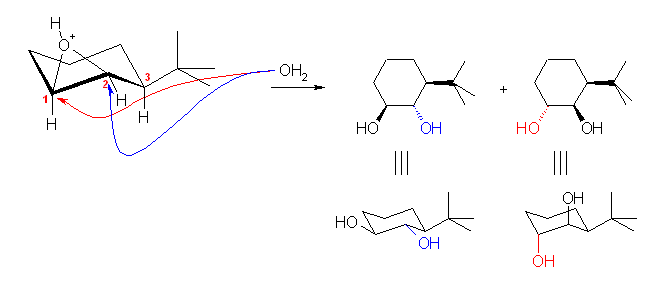
問題文にも与えられているように、「酸触媒加水分解では、ジアキシャル-1,2-ジオールを与える」とするならば、実際に起きている反応は赤の矢印での課程であることになる。
← すみません、以下のなぜなのかの説明は正しいかどうかわかりません。そのそも他の教科書で「酸触媒加水分解では、ジアキシャル-1,2-ジオールを与える」という同じ記述を見つけていません(探し方が悪いだけかもしれませんが)ので。通常は、環の反転でジエカトリアルとジアキシャルが入れ替わってしまうので、環の反転の無い系でしか問題とされないような内容ですので、深く追求はしないでおきましょう。でも、「トランス-1,2-ジオールを与える」ことは間違いないです。また、エポキシ環が開く瞬間は、2つの水酸基酸素がアンチの立体配置をとるのは、SN2 なので当たり前です。ただ、tert-butyl 基との関係でどのような配座のエポキシドが求核攻撃をうけているのかをまじめに考えてあげないと答えは出ないです。そもそも、いす型配座は、すべての炭素がねじれ形をとれるために安定でした。しかし、エポキシ酸素の結合した1位および2位の炭素はねじれ形をとれません。必ず重なり形でなければなりません。この時点でシクロヘキサン環はいす型ではなくなります。しかしながら、酸性条件下ではエポキシ酸素がプロトン化を受けているために、より脱離がおきやすくなっています。(酸性条件下では、位置選択性に対しても、カルボカチオンの安定性が影響を与えるような、SN1 的な性格が混ざってきていることをすでに学びました。)つまり、酸性条件下では、反応の遷移状態が反応生成物に近い構造であると仮定できます。ここから、「エポキシ環の開環がおこるような加水分解において、tert-butyl 基がエカトリアル位にあるようなシクロヘキサンのいす型配座に近い形で、なおかつ水酸基酸素がアンチになるような遷移状態を経る」のだとすると、ジアキシャル-1,2-ジオールを与えることの説明になると思われます。
18.43, 41
Grignard 試薬 CH3MgBr による反応は、形式的には、CH3- による求核反応であると理解してよい。反応系中には、当然のことながらプロトンは存在しない。(もし、プロトンそのものや、プロトン供与性の置換基があれば、CH3- + H+ の反応によりメタンを生じてしまい、Grignard 試薬は反応に関与できない。)
オキセタン oxetane は、通常のエーテルやエポキシドと同様、酸素に隣接した炭素上に(酸素の電気陰性度により誘起されて)正の部分電荷があり、求核攻撃を受ける。
エーテルの酸素に隣接した炭素に求核攻撃がおきたとき、非環状のエーテルではエーテル酸素がプロトン化を受けていると中性のアルコールが脱離できるので求核置換が生じるが、エーテル酸素がプロトン化を受けていない場合では脱離基がアルコキシドとなり、脱離しない。しかし、3員環のエポキシドではエーテル酸素がプロトン化をうけていなくても、環の歪みから(通常は脱離能の低い)アルコキシドの脱離が生じる。
(解答例)
エーテルの酸素に隣接した炭素に求核攻撃がおきたとき、非環状のエーテルではエーテル酸素がプロトン化を受けていると中性のアルコールが脱離できるので求核置換が生じるが、エーテル酸素がプロトン化を受けていない場合では脱離基がアルコキシドなので、脱離しない。
3員環のエポキシドではエーテル酸素がプロトン化をうけていなくても、環の歪みから(通常は脱離能の低い)アルコキシドの脱離が生じる。
4員環のオキセタンでは、環の歪みは3員環にくらべると小さいため、アルコキシドの脱離は3員環のエポキシドに比べると遅くなる。
epoxy (← epi + oxy ; epi は「上に」とか「追加」などの意の接頭辞)とは、もともと -O- という架橋部分に対する名称である。そのため、オキシラン環に対しては、1,2-epoxyalkane のように命名していた(1位と2位の炭素を -O- 架橋で連結した構造)。したがって、その延長として命名するならば、置換オキセタン は substituted 1,3-epoxypropane のように命名できる。
18.44, 42
ハロヒドリンよりエポキシドが生じる反応は、分子内の水酸基由来のアルコキシドが、隣接したハロゲン結合炭素を背面より求核攻撃し、分子内 SN2 機構により進行する。アルコキシド酸素が、隣接したハロゲンの結合した炭素の背面より正しい向きで求核攻撃するためには、どのような立体的な位置関係が必要かを図を描いて確認すること。これらの反応は、エポキシドに対しての求核攻撃により開環する反応の逆反応として考えてよい。
2-クロロシクロヘキサノールの2種の立体配置異性体のうち、一方は上述のようなエポキシド形成反応をするが、もう一方の立体配置異性体では、アルコキシドが分子内の SN2 反応に適した空間配置にないために、この反応と競争して別の反応により、問題文に与えられたシクロヘキサノンを生じると考えられる。
分子間の SN2 反応(すなわち、OH- による求核置換)では、ハロゲンが水酸基に置換されるだけであるから、シクロヘキサノンにはならない。
(すなわち、OH- がクロロシクロヘキサノールのアルコール水素を引き抜くのも塩基としての反応であったわけだが、)求核種は多かれ少なかれ、必ず同時に塩基性をもつ。(逆もしかり。すなわち、塩基は多かれ少なかれ、必ず同時に求核性を示す。)また、ハロゲン化アルキルは強塩基存在下で(求核置換と競争しながら)脱離反応をひき起こし、この反応の立体化学は、アンチ脱離であったことも思い出すこと。
(解答例)
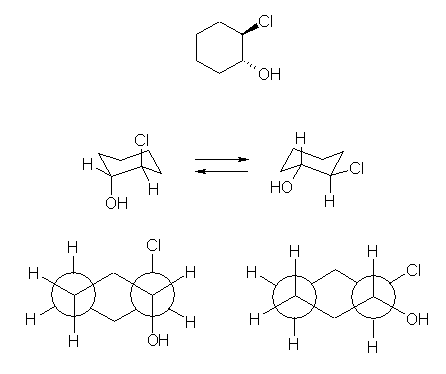
trans--2-chlorocyclohexanol は、上のような立体配置を持っており、環の反転により2つの置換基、-Cl と -OH がアンチの位置関係をとることができる。
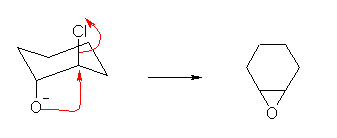
そのため、NaOH で処理することにより生じたアルコラートが、分子内の求核置換により 1,2-epoxycyclohexane を与える。
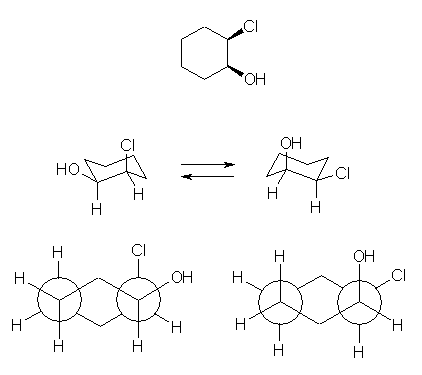
これに対し、ciss--2-chlorocyclohexanol は、上のような立体配置を持っており、環の反転を行っても2つの置換基、-Cl と -OH は常にゴーシュの位置関係にある。
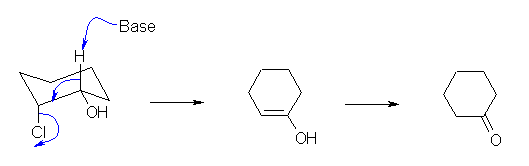
そのため、分子内の求核置換反応は遅いが、代わりに水酸基の付け根で若干酸性度の上がった水素が、クロロ基とアンチの位置関係にくるので、上の機構のようなアンチ脱離が生じ、cyclohexenol を与えるが、これはすぐに互変異性化により cyclohexanone を与える。
18.45, 43
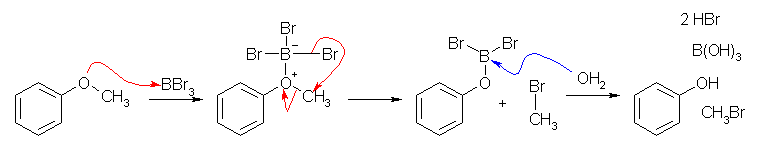
本質的には、HI によるエーテルの酸開裂反応と同じに理解できる。すなわち、H+ はルイス酸としてエーテル酸素(の孤立電子対)に結合していくものと考えててよい。BBr3 との反応では、ホウ素がプロトンの代わりにエーテル酸素に結合する。ついで、求核種であるハロゲン化物イオンがエーテル酸素に隣接した炭素を求核攻撃する。
(解答例)
上、ヒントにほとんど答えをそのまま書いてしまっている。次図のとおり。
18.46, 44
1モルのメトキシ基があると、1モルのヨードメタン CH3I を生じ、したがってヨウ化銀 AgI を1モル生じさせる計算となる。
(解答例)
バニリン vanillin 1.06 g は、その分子量 152 で割ると、6.97 mmol である。
ヨウ化銀 1.60 g は、その式量 234.8 で割って、6.81 mmol である。
1モルのメトキシ基は1モルのヨウ化銀を生じるのであるから、バニリン1分子中にメトキシ基が(6.81/6.97 にいちばん近い整数として)1つある計算となる。
バニリンは以下の構造を持つ。
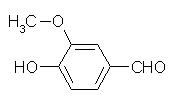
今日では、分子の構造決定に IR (赤外吸収)や、NMR (核磁気共鳴)などの分光学的な手法が使われる場合が多いので、Zeisel 法などのような化学反応を利用する方法は実験室でも頻繁に使われるわけではない。しかしながら、これらの反応の原理を理解しておくことは大切である。
エーテルの酸開裂で生じるヨードメタン CH3I は、常温で無色透明の液体で、沸点は43℃だから容易に気化させることができる。他のエーテルからは分子量の大きい(よって、沸点も高い)ハロゲン化アルキルしか生じないので、メトキシ基のみを定量できるのだろう。
18.47, 45
不飽和度 : 分子式 C19H38O より、不飽和度が1であることがわかる。すなわち、分子内には二重結合( C=C、または C=O )または環構造を1つだけ持つ。酸素原子を1つ含むので、(鎖状および環状の)エーテル、アルコール、ケトン、アルデヒドの可能性がある。
1H-NMR : アルデヒドであれば 9~10 ppm 付近にピークを示すはずであるので、違う。エーテルやアルコールの酸素に隣接した炭素上に水素があれば、3~3.5 ppm付近にピークを示す。ただし、3級アルコールなどのように酸素に隣接した炭素に水素が無い場合は、これに対応するピークが無いはずだから、3~3.5 ppm付近にピークが無いからと言ってエーテルやアルコールではないとはいえない。炭素炭素二重結合があり、そこに水素が結合していれば、5~7 ppm 付近にピークを示すはずである。(さきほどと同様、相当するピークが無いからと言って、C=C が無いとは言えない。)この分子の場合は、図 18.5 (1,2-epoxypropane の 1H-NMR スペクトル)と見比べることにより、2.8 ppm のピークはエポキシドの構造に対応していることの検討がつく。
エポキシドは、酸処理により 1,2-ジオールを与える(エーテル酸素のプロトン化と、引き続いておこる水による求核攻撃での環開裂による)。また、1,2-ジオールを酸性条件下などで過マンガン酸カリウム KMnO4 での処理をすると、炭素-炭素二重結合を処理したときと同様にカルボン酸およびケトンを生じる。(オゾンと反応させ、亜鉛-酢酸で処理することによりアルデヒドとケトンを生じた(オゾン酸化)ことと対応して覚えること。)
(解答例)
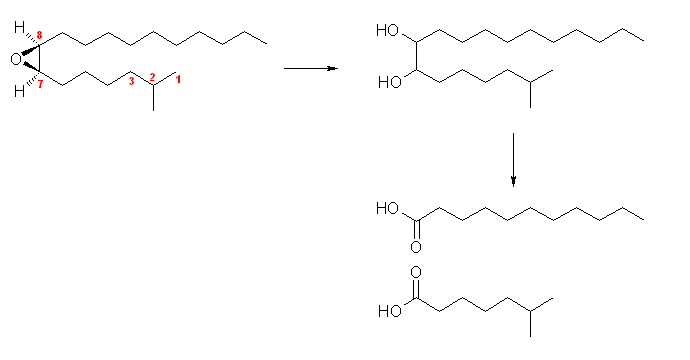
disparlure, C19H38O は、(7R,8S) の立体化学を持つ。酸処理により vic-ジオールとなり、KMnO4 による処理で undecanoic acid と 6-methylheptanoic acid を与える。
18.48, 46
問い 18.47 で disparlure の正しい構造が判ったものとして解くことになる。炭素数 10 以下の化合物から出発しなければいけないから、目的生成物を少なくとも2つの部分から組み立てることになる。
disparlure は分子内にエポキシドの構造を持つが、エポキシドはどのように合成できるかを考えると、前駆体としてオキシラン環(含酸素の3員環)に対応する部分が二重結合であるようなオレフィンから合成することになるだろう。
オレフィンは、アルコールからの脱水、アルキンの接触水素添加や液体アンモニア中のアルカリ金属による還元、Wittig 反応によって、などの方法で合成できる。アルコールはカルボニルに対して Grignard 試薬を付加させることで単純に合成できるが、そのアルコールよりの脱水において位置選択的な反応をおこすことは可能であるかを考えること。
ついで、正しい位置に二重結合を導入することができた場合、それぞれの幾何異性体、すなわち、(E)-体と (Z)-体からエポキシドに誘導する際、どのような条件(過酸により1段階でエポキシ化、またはハロヒドリンを経由、など)のときにどのような立体でエポキシドが生じるかを整理しておくこと。
(解答例)
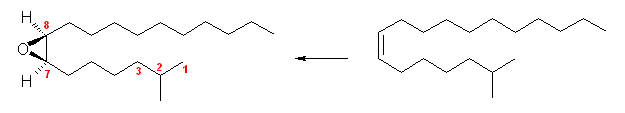
disparlure の前駆体となるオレフィンは、(Z)-2-methyloctadec-7-ene である。これを過酸で処理することにより、(7R,8S)-体および(7S,8R)-体の光学異性体の混合物(ラセミ体)となる。
Wittig 反応によってアルケンを合成(教科書 19.12節参照)した場合、(E)-体が主として得られるので、今回の目的にはそぐわない。そこで、アルキンを Lindlar 触媒存在下、接触水素化(教科書 8.6節参照)により選択的に (Z)-のアルケンを合成することを考える。
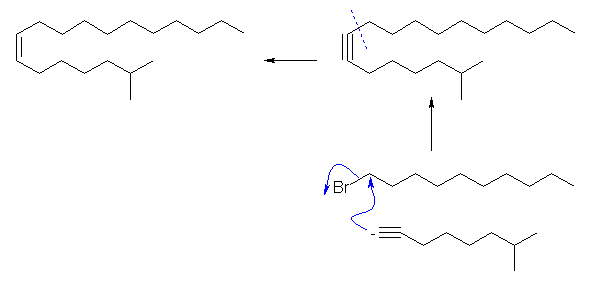
そのようなアルキンは、2-methyloctadec-7-yne で、これを炭素数10以下のパーツより合成するためには、アセチリドアニオンのアルキル化反応(教科書 8.9節参照)を用いることができる。
18.49, 47
「通常の」酸水溶液による環の開裂では、エポキシ酸素へのプロトン化、水による求核攻撃を経て 1,2-ジオールが生成するものと考えられる。 ←この際の反応機構(いわゆる、SN1 的な性質を併せ持った SN2 機構)と生成物の構造についても整理しておくこと。
1,1-diphenyl-1,2-epoxyethane の場合は、一方の炭素が3級であるばかりでなく、その位置がベンジル位でもあり、特にその位置のカルボカチオンが安定であることに注意する。そのため、3級アルコールや非環状の3級のエーテルで、酸性溶液中で SN1 的にカルボカチオンを生じるのと同様に、カルボカチオンを生じる可能性がある。そのように考えて 1,1-diphenylethanal (ジフェニルアセトアルデヒド)を与えるような反応機構を考えてみること。
カルボカチオンは、骨格や置換基などが転位することがあることを思い出すこと。
(解答例)
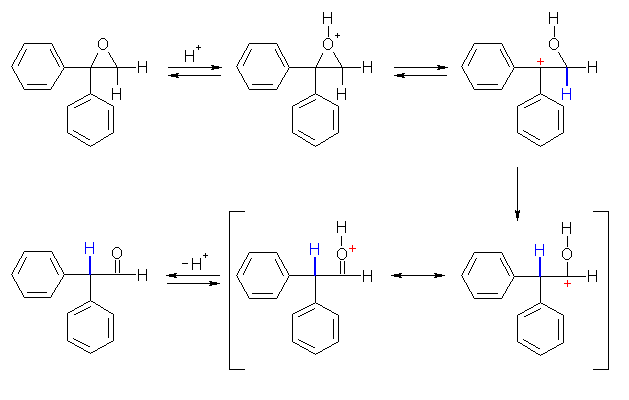
エポキシドの酸性加水分解では、プロトン化をうけたエポキシドは SN1 的な性格を持ちながらも、SN2 機構で環を開く。1,1-diphenyl-1,2-epoxyethane は、3級のエポキシドであるばかりでなくその位置がベンジル位でもあるため、SN1 的に(分子内の R-OH を脱離しながら)環を開き、より安定なカルボカチオンを与える。ここで、ヒドリドシフトが起きて生じる水酸基ねもとのカルボカチオンは、プロトン化をうけたカルボニル基の共鳴構造として描くことができるので、プロトンを失うことによりアルデヒドを与える。
18.50, 48
教科書の構造式の右の化合物名「o-ヒドロキシアセトアルデヒド」は、明らかに間違い。問題文中の「o-ヒドロキシフェニルアセトアルデヒド」は正しい。
前問(18.49 (第5版では、18.47))をヒントにして類似の方法で合成することが可能である。最終目的物に変換可能な前駆体の構造は何であるか。
更に、その前駆体を合成するためにはどのような官能基が必要であるか、というように逆合成の方法で考えること。フェノールの環に炭素2個の置換基を導入するところは、芳香族求電子置換反応を利用する。
(解答例)
前問と同じ反応、
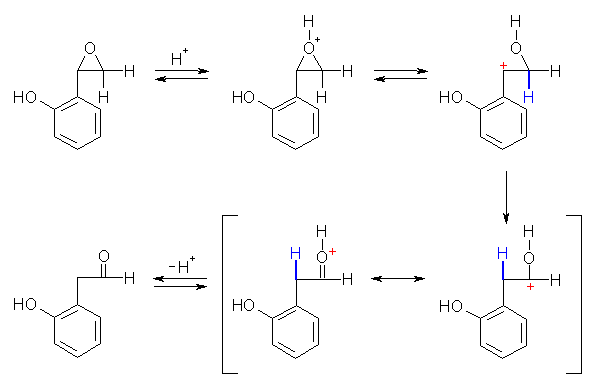
を合成に利用するため、上スキーム中の出発物質となっているエポキシドの前駆体として、まず o-vinylphenol を合成する。(過酸の処理によりエポキシドにすることができる。)
下に、一例のみを示すが、他にもいくつかのルートが考えられる。
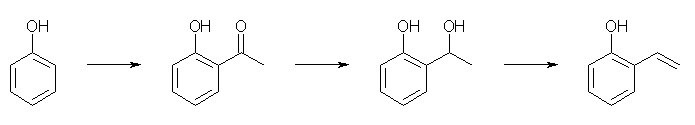
反応試薬の例は、以下のとおり。
CH3COCl, AlCl3 (Friedel-Crafts アシル化反応), NaBH4 (ケトンの還元), POCl3-pyridine (脱水)
18.51-18.58 (49-56)
18.51, 49
(a) に関しては、改めてヒントが必要であるようであれば、教科書9章などに立ち返って復習しておくこと。立体化学を描くためにはオキシラン環(含酸素の3員環)を平面内に書き、そこについた置換基をくさび型の結合で表す方法などを使う。
(b)~(d) 酸水溶液での処理であるから、まずエポキシ酸素にプロトン化し、水が正の部分電荷を持つ炭素に対して求核攻撃していく機構で進行する。位置特異性、立体特異性について整理すること。
(解答例)
(a) (2R,3R)-2,3-epoxy-3-methylpentane
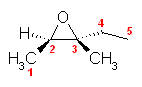
(b) 反応は次式のとおり。主生成物は、(2R,3S)-3-methylpentane-2,3-diol
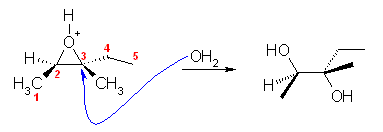
反応の位置は、主としてよりアルキル基の多いほうの3位の炭素。(SN1 的性格)
立体は反転する。(SN2 反応)
(c) 生成物は、対称面をもたず、キラルである。
(d) 3位の炭素への求核攻撃のみが起きた場合には、(2R,3S)-3-methylpentane-2,3-diol
のみが生じ、光学活性である。もし位置選択性が低く、2位の炭素への求核攻撃も同時に起きるようであれば、(2S,3R)- 体(光学異性体)が混入してくるはずである。位置選択性がまったくなければ、光学異性体の等量混合物となり、光学活性ではなくなる。
18.52, 50
a~c あたりは、教科書 17 章あたりを、d,e あたりは教科書、18章の「反応のまとめ」などを見直すこと。
(解答例)
(a) CH3MgBr, (b) H2SO4 または POCl3-pyridine (c) NaH, then CH3I, (d) RCO3H, (e) OH-
18.55, 53
問題 18.54(第5版では、18.52)(1H-NMR スペクトルの問題)で構造を推定しているのだが、ここでは、anethole, C10H12O の構造を以下に与えておく。
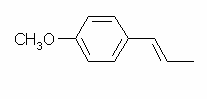
ベンゼンが出発物質に指定されているので、ベンゼン環上に methoxy基と 1-propenyl 基を導入することになる。ベンゼンからフェノールへの変換は教科書 16.2 節および 17.10 節を参照すること。教科書 17.10 節(p 648 (第5版では、p652))より引用「このような過酷な条件に耐える官能基は少ないので、この反応はアルキル置換したフェノールの合成に限定される。」にあるように、はじめに benzene を anisole (= methoxybenzene )に変換し、次いで p-位に最終的に 1-propenyl 基に変換される何かを導入するとよい。
(解答例)
反応のルートの一例のみを示す。反応条件等についても各自確認しておくこと。
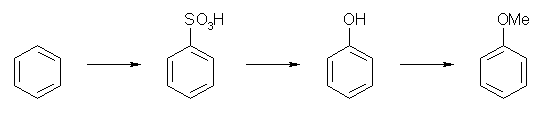
スルホン化、ついでアルカリ溶融。williamson エーテル合成。
ついで、p-位に、1-propenyl 基を導入する。
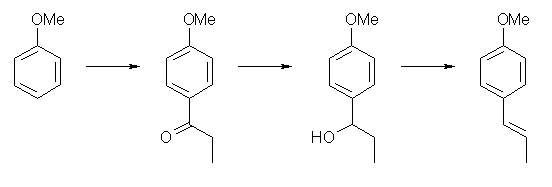
CH3CH2COCl, AlCl3(Friedel-Crafts アシル化), NaBH4(ケトンの還元), POCl3-pyridine(脱水)
他のルートもありうる。たとえば、
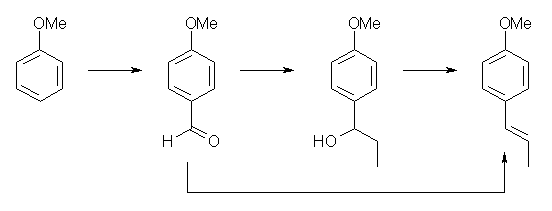
ホルミル化( DMF, POCl3, then OH- : Vilsmeier 反応)により anisaldehyde としたのち、グリニヤル試薬と反応させると、ひとつ上のスキーム中と同じアルコールとなる。また、anisaldehyde は Wittig 反応によっても anethole を与える。
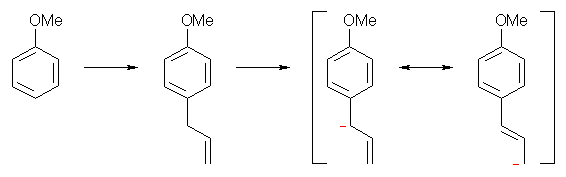
アルケンを強塩基と処理すると、上図のようにカルボアニオンを経由して、二重結合位置の移動 migration of double bonds が生じる。より安定なアルケンを生じる方向に反応は進むので、18.39 safrole の合成のときと同様にしてアリル基を導入したのち、KNH2 で処理してやると、ベンゼン環と共役したより安定なアルケンである 1-propenyl 基へと転位する。(このような二重結合の位置の移動は、プロトン酸や、ルイス酸を触媒とした場合も進行する。)
18.57, 55
アルコールの酸性条件下でのハロゲン化アルキルへの変換や、エーテルの酸開裂などと類似の反応機構で進行する。何が求核種で、何が脱離基であるかを整理すること。
(解答例)
概略をスキームで示す。
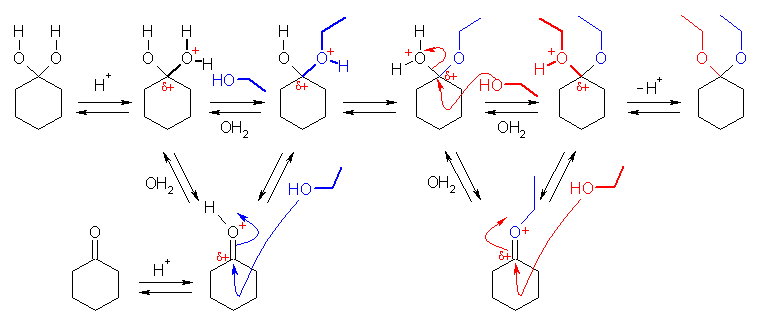
18.58, 56
「驚くべきことに」と問題文にあるが、別に驚くようなことは起こっていないので安心すること。(笑
NaBH4 での処理は、「ヒドリド還元」であり、すなわち H- がカルボニル炭素に求核付加する反応である。通常、カルボニルへのヒドリド付加体をアルコールにするためには、酸(H+)での処理が必要であった。
エポキシドの合成手段の1つに、ハロヒドリンを経由する方法があったことを思い出すこと。
(解答例)
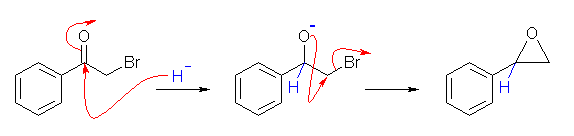
カルボニルへのヒドリドの求核付加により生じたアルコラート(ハロヒドリンより生じたアルコラートと同じ形である)が、分子内で隣接炭素に求核攻撃し、エポキシドを生じる。
(18.53、54、56 は、現在準備中です。)