22.01-22.10
22.01, 01
(g) アセトフェノン は、第5版のみの問題
選択肢の中に、α 水素が2種類あるものがあるので注意すること。
(解答例)
(a) 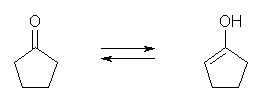
(b) 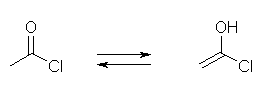
(c) 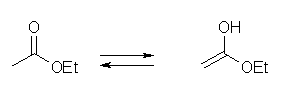
(d) 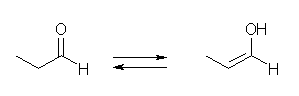
(e) 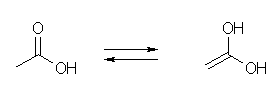
(f) 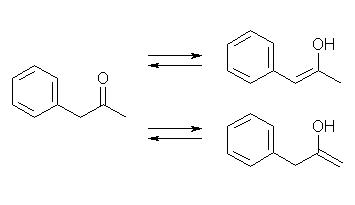
(g) 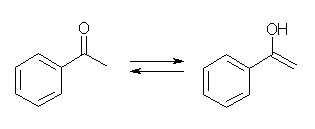
(d) のエノール体には、二重結合の幾何異性体(シス-トランス異性体)がある。
(e) のフェニルアセトンは、カルボニルの α 水素が2種類ある。そのため考えられるエノール型は2種類書くことができるが、図の上の構造の方が安定。(フェニル基と共役した二重結合になっているので。)
22.02, 02
カルボニルの α 水素は相対的に他の位置の水素より、酸性度が高い。(共役塩基がエノラートの共鳴構造で安定であるから。)
(解答例)
カルボニルの α 水素を数えればよい。位置については、構造式等で示すこと。この解答例では省略。
(a) 4つ
(b) 3つ
(c) 3つ
(d) 2つ
(e) 3つ + 1つ(カルボキシ基の水素)
(f) 5つ
(g) 3つ
22.03, 03
α 水素は2種類ある。
(解答例)
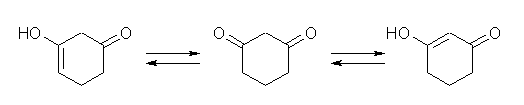
上のような2つのエノール体が考えられる。二重結合がもう一方のカルボニルと共役した構造である、右のエノール体の方が安定である。
(注意!)「問題の解き方」の解説では、左右のカルボニルを区別して4つのエノール体があるような表現になっているが、これはおかしい。この化合物の場合、エノール体は2種類しかない。また、下巻の解答例では「モノエノール体の構造をすべて」書いていないので、これもまた問題の指示からはずれている。
22.04, 04
ケト=エノール互変異性化の反応機構(教科書、図22.1)や、教科書、p866 の記述を参照すること。酸性触媒によるケトンの α ハロゲン化と共通の中間体を経由すると考えれる。
(解答例)
ケト=エノール互変異性化は可逆に進行する。酸性触媒では、カルボニル基をプロトン化する酸は、オキソニウムイオン(またはプロトン)、余分なプロトンを引き抜く塩基は周囲の水分子である。
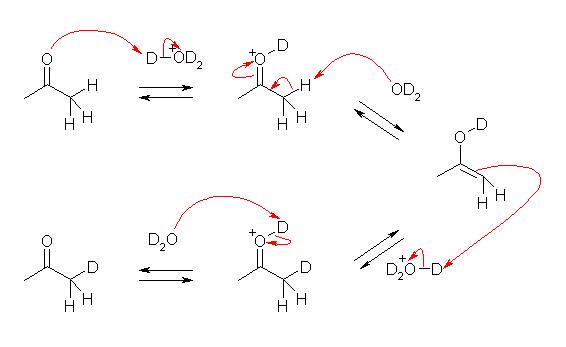
22.05, 05
不飽和度が1増える反応である。(二重結合が1つ増えている。)そのため、アルコールまたはハロゲン化アルキルからの脱離反応を利用することができる。また、カルボニル基の α 位は、選択的にハロゲン化することができることを思い出すこと。
(解答例)
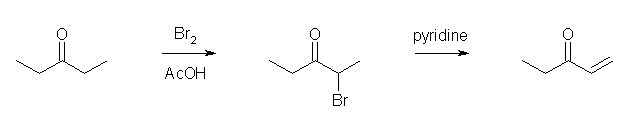
α 位の臭素化は、必ず酸性条件で行う必要がある。もし塩基性条件で行うと、モノブロモ化で止めることができない。(臭素を導入することでエノラートがより安定になるため、無置換のものよりもモノブロモ化されたものの方が基質として、塩基性の臭素化反応を受けやすいため。)
α 位の臭素化が塩基性で進行する場合は、中間体がエノラートである。そのため、左右非対称なケトンの場合、酸性度の高い水素が先に置換される。
22.06, 06
教科書 p868 の、Hell-Vollhard-Zelinskii 反応の機構を参照すること。
(解答例)
カルボン酸を酸ハロゲン化物(酸臭素化物)とし、エノール体を経由して α 位を臭素化したのち、酸ハロゲン化物を加水分解する代わりにメタノールによる加溶媒分解でメチルエステルを与えることができる。
従って、反応条件は、PBr3, Br2 qnd then MeOH となる。(反応機構の図は省略するが、加溶媒分解について不安があれば、カルボニル求核置換反応(21章)を参照すること。)
22.07, 07
α 位の水素はアルカン等の水素よりも酸性である。
問い 22.8 と関連して、ニトリルのシアノ基もカルボニル基と同様の効果を持つ。
(g) cyclohexa-1,3-dione は、5版のみの問題
(解答例)
赤字の水素が、その分子中で最も酸性。
(a) CH3CH2CHO
(b) (CH3)3CCOCH3
(c) CH3CO2H
(d) C6H5CONH2
(e) CH3CH2CH2CN
(f) CH3CON(CH3)2
(g) 2つのカルボニル基に挟まれた、2位のメチレン上の水素。
22.08, 08
カルボニル化合物の共役塩基(エノラート)の共鳴構造を参考にすること。
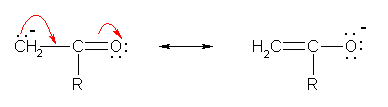
(解答例)
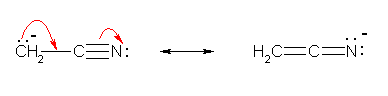
上図のような共鳴が書けるから、シアノ基の α 位の水素は、カルボニル基の α 位の水素と同じ程度に酸性度があると考えられる。
22.09, 09
反応の進行に伴って塩基が消費されるような場合、(中性ではなく)塩基があることによりはじめて反応が起きるが、「触媒ではない」ということになる。問いの本文での言い換え「ハロゲン化に完全に当量の塩基が必要である」ということの理由を説明できれば、問いに答えたことになる。つまり、反応の機構をきちんと説明すること。
(解答例)
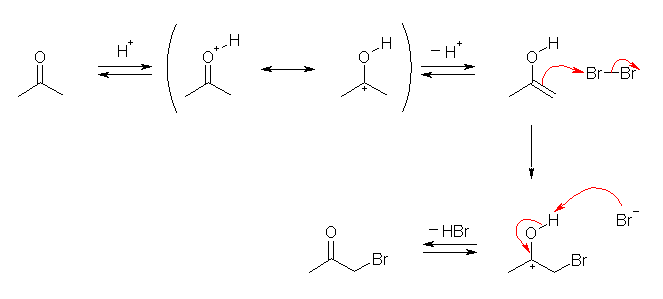
エノールを生成する過程は、上図のように、プロトンの付加と脱離(再生)を含んでおり、触媒過程である。この酸触媒により生じたエノールは、(臭素に対する求核的な反応により)臭素と反応して、置換生成物の他に、更に強酸である臭化水素を発生する。
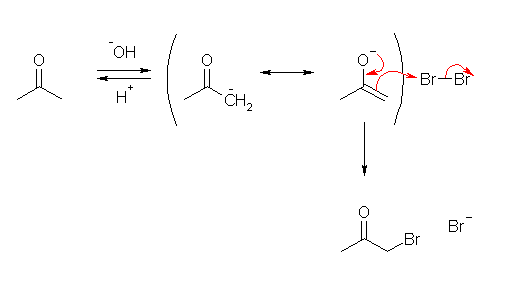
他方、エノラートを生成する過程は、塩基1当量と反応しており、塩基を再生していない。また、これにより生じるエノラートは、(臭素に対する求核的な反応により)臭素と反応して、置換生成物の他に臭化物イオンを発生する。この臭化物イオンは、強酸である臭化水素の共役塩基である。そのため、水と臭化物イオンの反応により、HBr と -OH を生じるような「加水分解の」反応は起きない。
22.10, 10
脱離の容易さは、その脱離するイオンの安定性で説明することができる。すなわち、単独でも安定なイオンは、脱離しやすい。また、単独でも安定なイオンの共役酸は強酸である。
(解答例)
ハロホルム反応における脱離基、-CX3 というカルボアニオンは、負電荷が電子求引性であるハロゲンによってイオン全体に非局在化をうけ、安定化されているため。
22.11-22.20
22.11, 11
マロン酸エステル合成では、R-X との反応により、R-CH2CO2H という置換酢酸を生じることを参考に計画せよ。
(d) ethyl cyclobutanecarboxylate は、5版のみの問題
(解答例)
(a) と (c) は、マロン酸エステルをモノアルキル化して、加水分解後、脱炭酸させる。(b) および (d) は、マロン酸エステルを2段階でジアルキル化して、加水分解後、脱炭酸させる。
以下、用いるハロゲン化アルキルのみを示す。各段階の反応については、教科書 p878 を参照すること。
(a) PhCH2Br
(b) CH3CH2CH2Br, CH3Br
(c) (CH3)2CHCH2Br
(d) BrCH2CH2CH2Br
(d) では、分子内で環状になるようにジアルキル化する。また、加水分解、脱炭酸後、再度エチルエステル化する。(エステルのままでは脱炭酸しない。)
を用いることのできる反応では、試薬の沸点の観点より、実際の操作の容易さを考慮した実験条件としては、CH3I
を選択することがある。(CH3Br
は、沸点が摂氏4度なので、常温で気体。CH3I
は、沸点が摂氏43度なので、常温で液体。)
22.12, 12
酢酸 CH3CO2H は、 α 水素を3つもつが、マロン酸エステル合成では酢酸ユニットの α 水素は2つしかない。そもそも、アルキル化反応において、エノラート型のイオンによるハロゲン化アルキルへの求核攻撃がキーステップであるが、マロン酸エステルの場合、2つのカルボニル基によって二重に安定化を受けるカルバニオンがあるため、この反応が容易に生じる。
(解答例)
マロン酸エステル合成では、2つのカルボニルによって活性化されたメチレンには、置換される水素が2つしかないから、二置換のマロン酸までを合成することができる。三置換のマロン酸にはならない。形式的には、マロン酸の一方のカルボキシ基は置換酢酸として残るが、もう一方のカルボキシ基は脱炭酸する。この脱炭酸した位置の水素が、二置換までの置換生成物において α 水素となっている。
22.13,
問い 22.11 と同様に考えること。
(解答例)
マロン酸エステルを2段階でジアルキル化して、加水分解後、脱炭酸させる。
各段階の反応については、教科書 p878 を参照すること。
用いるハロゲン化アルキルは、(CH3)2CHCH2Br および CH3Br である。
22.14, 13
アセト酢酸エステル合成では、R-X との反応により、R-CH2COCH3 という置換アセトンを生じることを参考に計画せよ。
(解答例)
アセト酢酸エステルをモノアルキル化して、加水分解後、脱炭酸させる。
以下、用いるハロゲン化アルキルのみを示す。各段階の反応については、教科書 p880 を参照すること。
(a) (CH3)2CHCH2Br
(b) PhCH2CH2Br
22.15, 15
生成物の構造を書き、アセト酢酸エステルの反応(途中のキーステップとして、R-X に対する求核置換反応により、最終的に、R-CH2COCH3 を与える。)が可能かどうか、検討せよ。
(解答例)
(a) もし、フェニルアセトン Ph-CH2COCH3 をアセト酢酸エステルの反応により得ようとするなら、PhBr に対する求核置換反応をすることになる。芳香族のハロゲン化物は、通常、求核置換反応を受けない。(分子内に、ニトロ基などがある場合を除く。)従って、アセト酢酸エステル合成では、フェニルアセトンを合成することはできない。
(b) アセトフェノン PhCOCH3 は、フェニル基がカルボニル基と結合しており、置換アセトンではない。(R-CH2COCH3 または RR'-CHCOCH3 または の形ではない。)そのため、アセト酢酸エステル合成では、アセトフェノンを合成することはできない。
(c) 3,3-ジメチル-2-ブタノン (CH3)3CCOCH3 は、3置換のアセトンR3-CHCOCH3 の構造である。問い 22.12 と同様に、アセト酢酸エステル合成で可能なのは二置換体までであるため、3,3-ジメチル-2-ブタノン をアセト酢酸エステル合成で得ることはできない。
22.16, 14
アセト酢酸エステルをジアルキル化して、加水分解後、脱炭酸させる。 各段階の反応については、教科書 p880 を参照すること。
(解答例)
BrCH2CH2CH2CH2Br
を用い、分子内で環状になるようにジアルキル化して、加水分解後、脱炭酸させる。
22.17, 16
マロン酸エステル合成やアセト酢酸エステル合成では、カルバニオンが2つのカルボニル基により安定化を受けるから、穏やかな塩基を用いることができるのに対し、ケトン、エステル、ニトリルを直接する際は、LDA (ジアルキルアミド Li+ R2N-)のような強塩基が必要である。
(解答例)
(a) PhCHCOCH3 に LDA を作用させて生じるアニオンに CH3Br を反応させる。(カルボニル基の α 位のフェニル基は、エノラートとハロゲン化物の反応では導入できない。)
(b) ペンタンニトリル CH3CH2CH2CH2CN に LDA を作用させて生じるアニオンに CH3CH2Br を反応させる。または、別法として、アセト酢酸エステル合成の応用として、シアノ酢酸エステル NC-CH2-CO2R を段階的にジアルキル化し、加水分解後に脱炭酸させることも可能である。(シアノ基は、アシル基と同様に α 位のアニオンを安定化する。そのため、シアノ酢酸エステルも、アセト酢酸エステルやマロン酸エステルと同様、活性メチレンを持つ化合物に分類される。)
(c) シクロヘキサノン に LDA を作用させて生じるアニオンに CH2=CCH2HBr を反応させる。
(d) シクロヘキサノン に過剰の塩基( LDA )と、過剰の CH3Br を作用させ、徹底的アルキル化を行う。カルボニル基の β 位などはアルキル化されない。
(e) PhCOCH2CH3 に LDA を作用させて生じるアニオンに CH3Br を反応させる。PhCOCH3 を出発原料としてジアルキル化をする場合には、形式上、トリアルキル置換体も生じるはずであるから、反応の制御に気をつけなければならない。または、アセト酢酸エステル合成の応用として、出発物質として PhCO-CH2-CO2R を用い、活性メチレンの部分をジアルキル化したのち、加水分解脱炭酸する方法がある。この方法では、トリアルキル置換体は生じない。
(f) 3-メチルブタン酸エステル (CH3)2CHCH2CO2R に LDA を作用させて生じるアニオンに CH3CH2Br を反応させる。または、マロン酸エステル合成を用い、イソプロピル化、エチル化を経て、加水分解、脱炭酸によって二置換の酢酸としたのち、再度メチルエステル化してもよい。
22.18, 17
22.8 節を参照すること。
マロン酸エステル合成では α 置換酢酸を、アセト酢酸エステル合成では α 置換アセトンを与える。
各段階の反応については、教科書 p878 ならびに p880 を参照すること。
(解答例)
(a) アセト酢酸エステル合成を用いる。
(CH3)2C=CHCH2Br をハロゲン化アルキルとして用いる。
(b) 2段階のジアルキル化を経たマロン酸エステル合成を用いる。
PhCH2Br と CH3Br をハロゲン化アルキルとして用いる。
22.19, 18
一般的に、β ジケトンでエノール型が安定となるのは、エノールの二重結合がもう一方のカルボニルと共役した形をとれるためである。そのため、2つのカルボニルに挟まれた位置のメチレンの酸性度が高い。問いで与えられた β ジケトンについて、下の立体構造を見ながら考えること。
bicyclo[2.2.1]heptane-2,6-dione の3次元模型
(解答例)
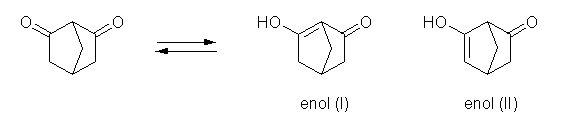
2つのカルボニル基の間の炭素は、ビシクロアルカンのブリッジヘッド(橋頭位)となっており、この炭素が関与するようなエノール体 (I) とするためには、次のような立体をとらないといけない。
bicyclo[2.2.1]heptane-2,6-dione のエノール体(I) の3次元模型
この構造は、二重結合が平面にならずにねじれており、歪みが大きく、安定に存在することができない。
一方で、ブリッジヘッド(橋頭位)の炭素を避けて、エノール体 (II) とすることもできる。
bicyclo[2.2.1]heptane-2,6-dione のエノール体(II) の3次元模型
この構造では、エノールの二重結合は、もう一方のケトンとの相互作用を持たないから、モノケトンのエノールと同程度の安定性のみが期待される。
22.20, 19
「C-H 結合が、C=O 二重結合の p 軌道(π 軌道)と平行である」ということは、「H+ が抜けたあとに生じる電子対(負電荷)が、π 軌道と共役することができる」ということを意味する。
(解答例)
カルボニル基に対しての α 水素がこの分子中では酸性である。そのうちでも、C=O 二重結合の p 軌道(π 軌道)と平行であるのは、アキシャル水素である。
22.21-22.30
22.21, 20
教科書 p872の、表 22.1 または、下巻の巻末付録 B を参照すること。
なお、(b)、(c) では複数の種類の水素が答えとなるので注意する。
(解答例)
pKa が25より小さいのは、大雑把に見ると、
1) カルボン酸(置換基によるが、5前後、酢酸で 4.75。)
2) アルコール(水とほぼ同じ、15前後)
3) フェノール類(アルコールより酸性度高い。10前後)
4) チオール類(アルコールより酸性度高い。10前後)
5) ニトロアルカン類(ニトロ基の α 位。10前後)
6) カルボニル化合物、カルボン酸誘導体。(カルボニル基の α 位。15 から 25程度。ただし、表からわかるようにアミドの α 水素は比較的酸性度は小さく、30程度。R-C(=O)X の X の種類により、カルボニル基に対する反応性が変化したのと同じ要因である。)
7) アルキンの sp 炭素に結合した水素
8) β ジケトン、ジエステルなど。活性メチレン化合物は、アルコールより酸性度が高いものが多い。
(a) カルボニル基の α 水素×4つ。pKa はおよそ 20程度。
(b) 活性メチレン(ジケトンに挟まれた炭素)上の水素×2つが一番酸性度高く、pKa は10程度。そのほかの4つの水素もカルボニル基の α 水素となるから、pKa はおよそ20程度。
(c) カルボニル基に共役した二重結合や三重結合は、その π 電子がカルボニル基によって分極している。そのため、カルボニル基に対する α 位(2つ、pKa はおよそ20程度)だけではなく、カルボニル基に共役した多重結合に対しての α 位(末端のCH3基上の3つ)も、同様に酸性度が高い。なお、水酸基をもつので、その水素(1つ)もまた、酸性度が高い(pKa は15前後)
(d) シアノ基の α 位の水素×2つ。シアノ基のみならず、フェニル基によってもアニオンは安定化をうけるから、活性メチレン化合物と同程度の酸性度と予想される。
(e) カルボニル基の α 水素×1つ。酸塩化物の カルボニル α 位だから、pKa はおよそ 16程度。
(f) カルボニル基の α 水素×1つ。pKa はおよそ 20程度。この問いの分子には存在しないが、(c) と同様、R-C(=O)-CH=CHCH3 のように、カルボニル基に共役した二重結合に対しても α 水素が存在する場合には、その水素も酸性になる。
22.22, 21
教科書 p872の 表 22.1 ならびに p782 の表 20.4 を、または、下巻の巻末付録 B を参照すること。
(解答例)
(a) 電子求引性基をもたないカルボン酸。pKa ~ 5。
(b) アルコール。pKa ~ 15。
(c) ジアルキルアミン。pKa ~ 40。
(d) ケトン。pKa ~ 19。
(e) β -ジケトン。pKa ~ 9。
(f) 電子求引性基をもつカルボン酸。pKa ~ 0.6
従って、酸性度の増大する順にこれを並べると、
(c) < (d) < (b) < (e) < (a) < (f)
なお、(c) の値から、LDA は、pKa が 40 より小さい程度の酸性水素を引き抜くことができることが判断できる。
22.23, 22
・共鳴構造式を書くときには、分子の回転や反転を行わず、原子核はもとの位置のまま、電子のみを動かす。
(解答例)
次の共鳴構造式では、負電荷を持つ原子を赤で示している。
(a) 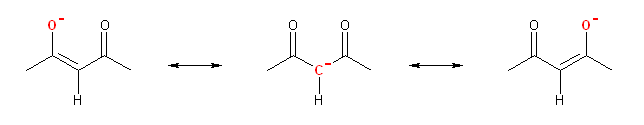
(b) 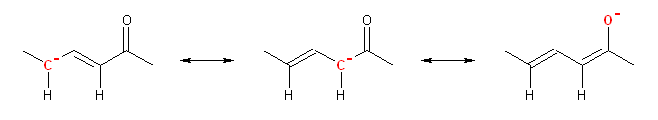
(c) 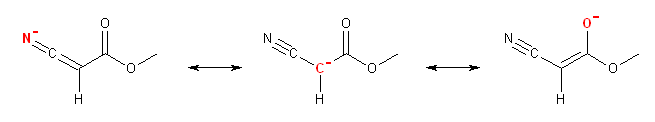
(d) 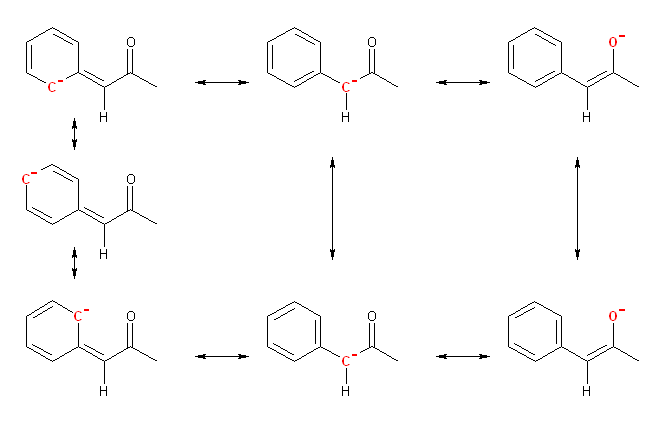
(e) 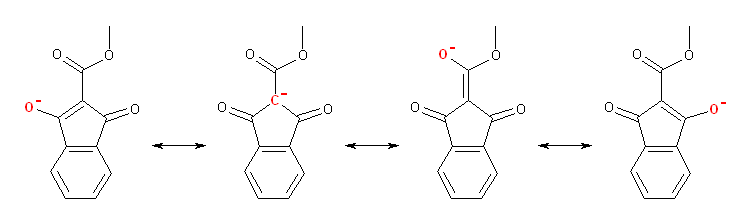
(e) では、ベンゼン環上の二重結合の位置の異なるもう一組が共鳴構造としてあるが、ここでは省略した。
22.24, 26
(a) マロン酸エステル合成を参照すること。
(b) β-ジケトンの活性メチレンの pKa は、約 9 程度である。すなわち、アルコールより強酸である。
(c) 教科書 22.4 節を参照のこと。
(d) 教科書 22.7 節を参照のこと。
(解答例)
(a) 脱炭酸により、cyclohexanecarboxylic acid を与える。
(b) アルコラートによって酸性水素が引き抜かれ、生じるカルボアニオンがヨウ化メチルに対して求核攻撃をする。2-methylcyclopentane-1,3-dione を与える。
(c) PBr3 により、カルボン酸は対応する酸ハロゲン化物に変換される。エノール体との平衡があるので、Br2 により、このカルボニル基の α 位が臭素化される。α 臭素化された酸ハロゲン化物は、加水分解され、カルボン酸を与える。A: 2-bromobutanoyl bromide, B: 2-bromobutanoic acid
(d) 塩基によって α 水素が引き抜かれ、生じたエノラートイオンは、ヨウ素に対しての求核攻撃をするので、ハロゲン化が起きる。モノハロゲン化が生じると、その位置の水素の酸性度はよりあがるから、未反応の基質(アセトフェノン)よりも、モノハロゲン化を受けた基質の方が反応しやすいので、1段階では止まらずジハロゲン化、およびトリハロゲン化が優先して生じることになる。生じたトリハロケトンは、水酸化物イオンによる求核攻撃でトリハロカルボアニオンを脱離して、カルボン酸とハロホルムとを与える反応である。 benzoic acid と iodoform を与える。
22.25, 27
教科書 p 874 の記述を熟読すること。
(解答例)
教科書 p 874 の記述の要旨:
・塩基条件でのカルボニルα 位のハロゲン化は、エノラートイオン中間体を経由する。
・少量のエノラートイオンが生成するとただちにハロゲンと反応する。
すなわち、エノラートイオンを生成する段階が律速段階で、ハロゲンとの反応はその律速段階に比べて十分に速い。(塩素、臭素は、そこにあるだけのエノラートと十分に速く反応してしまう。)
ハロゲンの種類のみが変化してエノラートとハロゲンとの反応の速さに変化があっても、そのエノラートイオンを生じる段階が律速段階であるから、全体とすると塩素化も臭素化も反応の速さに変化が見られない。
22.26, 28
構造式を書いてみること。その上で、問い 22.11 などと同様に考えよ。
(b) では、形式的に必要であるようなハロゲン化アルキルが、この反応に適するかどうかを判断する必要がある。
(解答例)
(a) 1-bromopropane を用いたマロン酸エステル合成により合成可能である。マロン酸をプロピル化し、加水分解後、脱炭酸することにより pentanoic acid が得られる。これをエステル化すればよい。
(b) 形式的には、2-bromopropane を用いたマロン酸エステル合成をすることになる。しかし、第2級のハロゲン化アルキルは、求核置換反応と競争して、強塩基の条件での脱離が生じうるので、実際問題としてマロン酸エステル合成を用いるのは、優れた方法ではない。
(c) 順次、1-bromoethane, bromomethane を用いて、マロン酸エステルをジアルキル化し、加水分解後、脱炭酸して得られる 2-methylbutanoic acid をエステル化すればよい。
(d) マロン酸エステル合成で、α 位を3置換した生成物を与えることはできない。
22.27,
問い 22.15 などと同様に考えよ。
(解答例)
ここに与えられた選択肢のうち (a) と (c) は、いずれもアセト酢酸エステル合成では得ることができない。その理由を以下に示す。
(a) 形式的には、3-bromophenyl 基をアセト酢酸エステルの α 位に導入しなければならないが、たとえば 1,3-dibromobenzene は芳香族求核置換反応をおこさない。(臭素が電子求引性の効果をもつとは言え、その効果の小さな m- 位であることもあり、芳香族求核置換反応を可能にするほどの効果ではない。)
(c) 形式的には、t-butyl 基を、アセト酢酸エステルの α 位に導入しなければならない。t-butylchloride などのような第3級のハロゲン化アルキルは、強塩基性の条件下、求核置換反応に優先して脱離反応を生じてしまう。
(b) は、1,5-dibromopentane などを用いたアセト酢酸エステル合成により得ることが可能である。
22.28, 29
アセト酢酸エステル合成では、 α置換のアセトンを生じる。
(解答例)
(a) 過剰の塩基と過剰のbromoethane によりアセト酢酸エステルの α 位をジエチル化し、加水分解後、脱炭酸すればよい。
(b) 順次、bromomethane, 1-bromopropane を用いてアセト酢酸エステルの α 位をジアルキル化し、加水分解後、脱炭酸すればよい。
22.29, 30
no hint
(解答例)
(a) マロン酸ジエチルと過剰の塩基(EtONa)、および CH3I により、ジメチル化する。塩基の選択としては、エステル交換や加水分解が生じないよう、エトキシドとする。
(b) 1,6-dibromohexane を用いて、アセト酢酸エステル合成をする。
(c) 1,3-dibromopropane を用いて、マロン酸エステル合成をする。
(d) CH2=CHCH2Br を用いて、アセト酢酸エステル合成をする。
22.30, 31
教科書 22.7 節を参照すること。
(解答例)
(a) および (b) は、アセチル基 -C(=O)CH3 のユニットをもち、ハロホルム反応に陽性である。
(c) および (e) は、アセチル基 -C(=O)CH3 のユニットをもたないので、ハロホルム反応に陰性である。
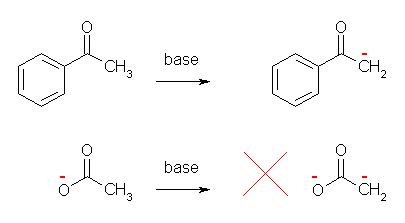
(d) は、アセチル基 -C(=O)CH3 のユニットをもつが、塩基性条件下ではカルボキシ基が解離してアセテートイオン CH3CO2- となる。アセテートイオンはすでに負電荷を持っているから、更にカルボニル基の α 水素が引き抜かれるような反応は起きない。
22.31-22.40
22.31, 23
cyclohexanone の分子式は、C6H10O である。
(解答例)
R-H + base → R-
R- + D2O → R-D + DO-
の反応で、酸性水素が重水素(原子量2)と交換される。
cyclohexanone、C6H10O から計算される分子量は 98 である。この分子中の酸性水素を、重水素で置換すると、分子量は4増えて102になる。これは、酸性水素が4つあることに対応する。
22.32, 24
問い 22.21 の解説を参照せよ。
また、共鳴構造を書いてみるとよい。問い 22.23 (b) などを参照すること。
(解答例)
カルボニル基に共役した二重結合や三重結合は、その π 電子がカルボニル基によって分極している。そのため、カルボニル基に対する α 位だけではなく、カルボニル基に共役した多重結合に対しての α 位も、同様に酸性度が高くなる。なお、次図のような共鳴構造によって「共役塩基の安定性」から酸性度を説明することもできる。
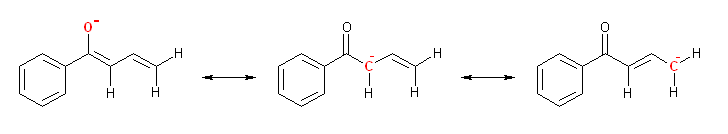
なお、共役エノンの π 電子系を、sp2 原子の p 軌道として表した図を付しておく。
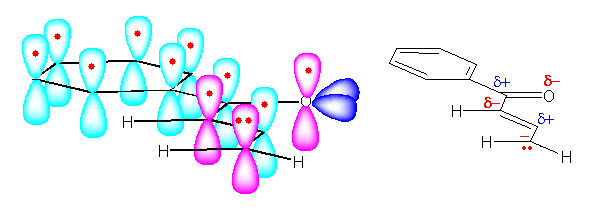
水色とピンクで π 系を示している。ピンクの p 軌道は、上の共鳴構造との比較からも判るように、分子軌道において電子密度が高いと予測される位置。これは、二重結合の分極(右図)とも対応している。なお、青の軌道は酸素の孤立電子対で、その他の π 系とは共役していない。
22.33, 25
問い 22.32 で与えられる分子との構造の違いに注意する。
「α 水素を持たない」わけではないことにも注意。
(解答例)
1-phenylprop-2-en-1-one は、カルボニル基の α 位にも、さらにカルボニル基に共役した二重結合の α 位にも、 p 軌道と平行の C-H 結合を持たない。
カルボニル基の α 位にひとつ水素があるが、この位置からプロトンが抜けても、残った電子対が π 系によって安定化を受けることができない。「この水素はビニル水素であるため、酸性ではない」という言い方をしてもよい。
22.34, 32
与えられる分子の構造を書いてみること。カルボニル基の α 位の水素は酸性であることにも注意。
(解答例)
酸性触媒では、ケト=エノールの互変異性化を経てカルボニル基の α 位のラセミ化が起きる。エノール体において、カルボニルの α 位に相当する位置の炭素は、sp2 混成、平面3配位型であるため立体は保持されない。
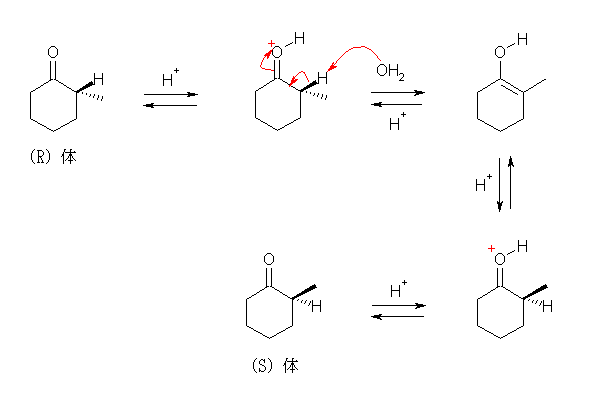
塩基性では、エノラートの形成を経てカルボニル基の α 位のラセミ化が起きる。エノラートにおいて、カルボニルの α 位に相当する位置の炭素は、sp2 混成、平面3配位型であるため立体は保持されない。(SN1 反応において、カルボカチオンを中間体に経由するために立体が保持も反転もされず、ラセミ化が起きたことを思い出すこと。)
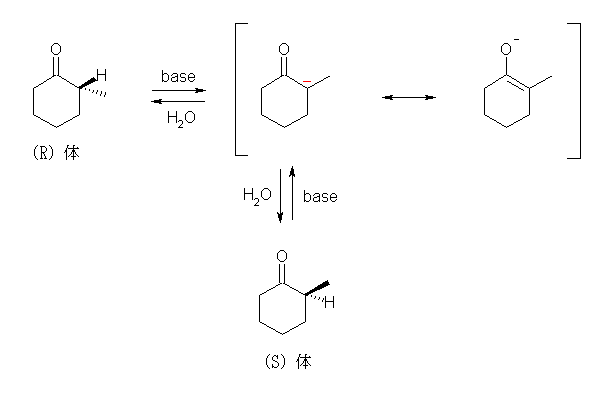
22.35, 33
問い 22.34 の反応機構をよく見ること。
(解答例)
酸触媒によるケト=エノール互変異性化においても、塩基によるエノラートの生成においても、カルボニル基の β 位であるキラル中心炭素は反応に関与しない。したがって、この位置の立体は変化せず、保持される。
22.36, 34
HVZ 反応の機構と、途中でどのような中間体を経由したかを思い出すこと。
(解答例)
HVZ 反応では、次図で示すように、PBr3 によって生成した酸ハロゲン化物のケト=エノール互変異性化と、その二重結合に対する臭素化反応を含む。このエノール体は、カルボニル基の α 位に相当する炭素が sp2 混成、平面3配位型であり、臭素化反応において面選択性がないため、生成物はラセミ混合物となる。
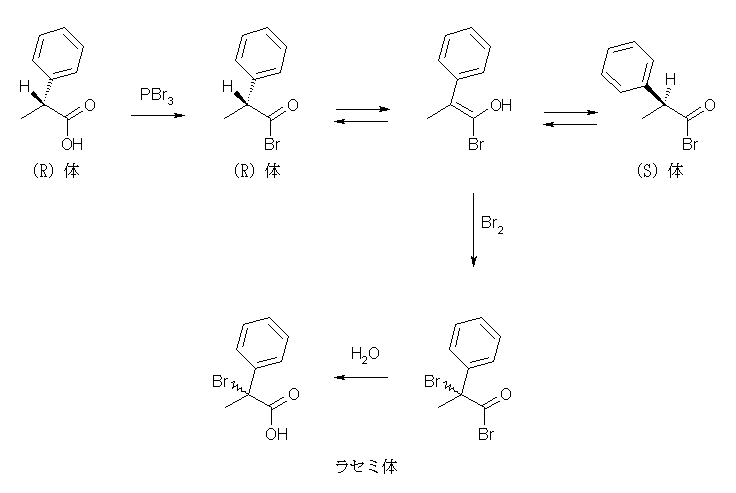
22.37, 35
反応基質は、β-ケトカルボン酸エステルであるから、マロン酸エステルやアセト酢酸エステルと同様に活性メチレン化合物である。
(解答例)
(a) NaOCH3, CH3I
(b) H3O+, heat または、NaOH-aq, heat, then H3O+
(c) LDA, then CH3I
(注意)(a) に用いる塩基は、「問題の解き方」ではナトリウムエトキシドとしているが、本来これは正しくない。あとでエステルは加水分解されてしまうので本質ではないかもしれないが、ナトリウムエトキシドを用いた場合、反応生成物として、メチルエステル以外にエチルエステルが混入するからである。(エトキシドアニオンにより、エステルのカルボニルに求核攻撃がおこり、そこでメトキシドアニオンが脱離するような置換反応が起きる。メトキシドアニオンを塩基として用いる場合でも、同様のカルボニル求核置換反応は生じるが、生成物はメチルエステルのままであるので見かけ上反応しないものとして扱える。)
(b) エステルの加水分解は、酸性条件、塩基性条件のいずれでも良い。ただし、脱炭酸のために酸性にするのが一般的である。
(c) の段階は、活性メチレンではないから、エノラートを生じるのに、LDA のように強い塩基が必要である。環の右側にすでに導入されているメチル基は、p 系に対して弱い電子供与性基として働くから、付け根の炭素の上野カルボにアニオンを不安定化する。(カルボアニオンは、級数の少ないほうが安定である。)そのため、この反応はメチル基をもたない側の α 炭素上で起きる。
22.38, 36
与えられた左右の構造に対し、ケト=エノール互変異性化反応を考えてみること。
(解答例)
次図のように、cyclohex-3-en-1-one (keto-1) は、ケト=エノール互変異性化により、cyclohexa-2,4-dien-1-ol (enol) となるが、これは、更にケト=エノール互変異性化により、cyclohex-2-en-1-one (keto-2) となることができる。したがって、酸触媒の下、keto-1 と keto-2 は互いに平衡にあることになるが、共役エノンである keto-2 の方が安定であるため、この平衡は keto-2 側に偏ることになる。
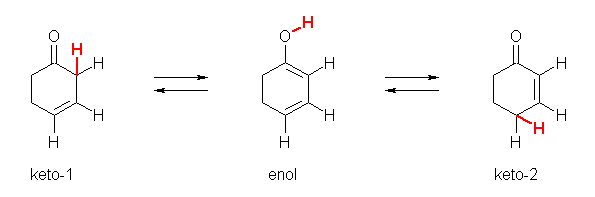
22.39, 37
問い 22.38 を参照すること。また、酸、塩基のそれぞれの条件での反応の比較という観点では、問い 22.09 や、問い 22.34 の解説も参照すること。
(解答例)
問い 22.38 で考えたような keto-1, keto-2, enol のそれぞれに対応した共通の共役塩基として、次図のような共鳴構造で書くことのできるエノラートアニオンが書けるため。
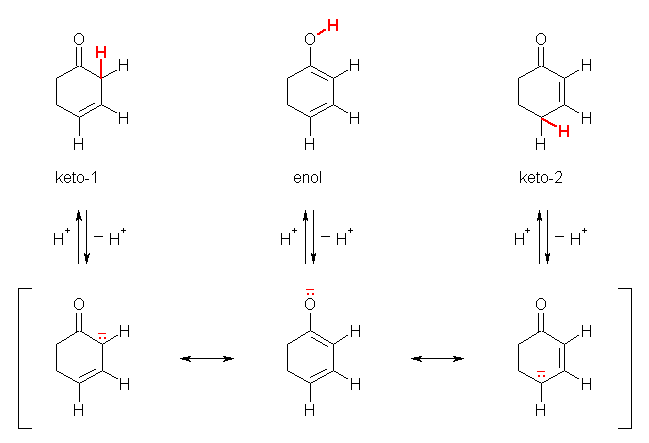
22.40, 38
カルボニル基(や、それに共役した二重結合)に対して α 位の水素であっても、ビニル位になっているものは酸性度がない。これは、C-H 結合の向きが、カルボニル(や、それに共役した二重結合)の π 系に対して平行に無いからである。
(解答例)
まず、塩基により、カルボニル基に対して α 位の水素のうち共役二重結合の無い方の(ビニル水素でない方の)水素が引き抜かれてカルバニオン(enolate-1 または enolate-2)を生じる。
このエノラートが酸素上にプロトンを受け取ると、エノール体(enol-1 または enol-2)を生成する。
(以上、塩基触媒によるケト=エノール互変異性化反応である。)
このエノール体は、下図、 anion-3 で示したような共鳴構造を書くことのできる共役塩基を持つから、カルボニル基の β 位に相当する位置の水素の酸性度が高く、容易に塩基によって引き抜かれる。
この anion-3 がプロトンを受け取る位置により、enol-1 と enol-2 は互いに平衡にある。
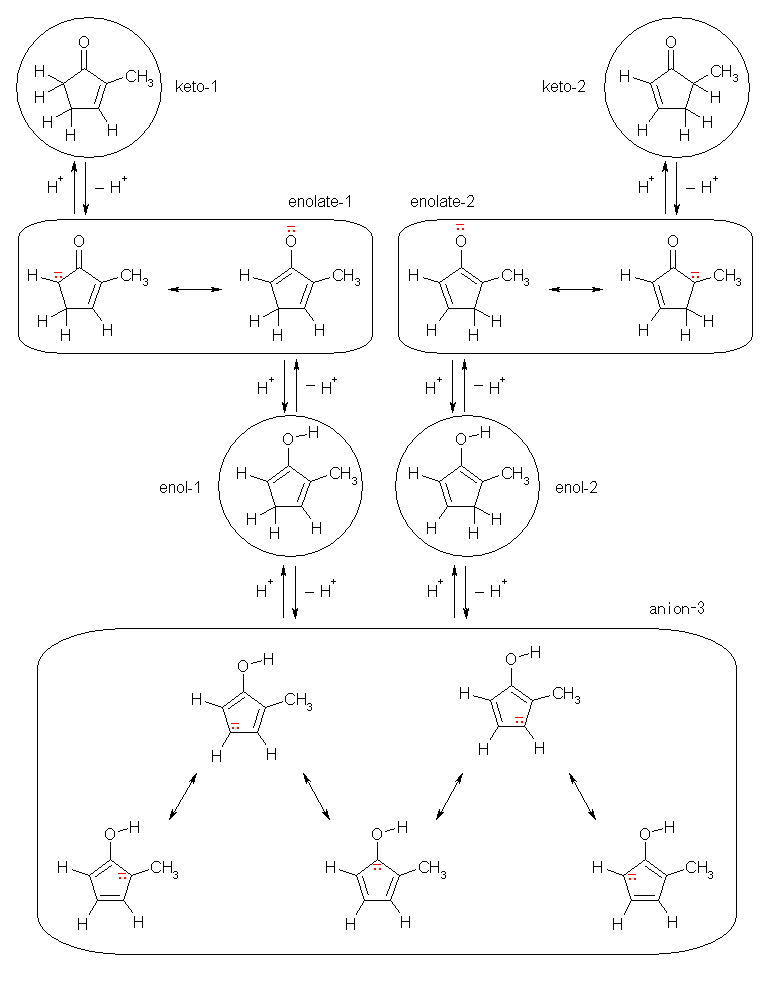
なお、anion-3 で与えられる共鳴構造は、6 π 系の芳香族性を示す。
22.41-22.50
22.41, 39
問い 22.40 の機構をよく睨むこと。また、カルボニル化合物や、共役エノンにおいて、酸性度の高い水素とはどういうものであったのかをよく思い出すこと。
(解答例)
カルボニル基に対しての α 位(下図中の赤)、および、カルボニル基に共役した二重結合に対しての α 位(下図中の青)の水素は酸性度が高く、塩基により引き抜かれる。
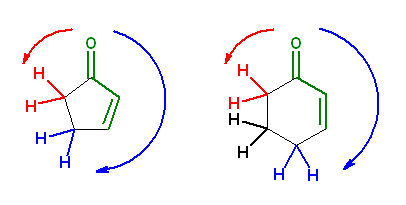
2-methylcyclohex-2-en-1-one が 5-methylcyclohex-2-en-1-one (環の二重結合の位置が動いているのだが、番号のつけ方が変わるので、命名においてはメチル基の位置番号が変わっていることに注意)に異性化するためには、カルボニル基に対して β 位の水素(上図では黒の太字で示した)が引き抜かれる必要があるが、この水素が酸性になる要因はない*から、塩基で引き抜くことができない。問い 22.40 では、カルボニル基に対する β 位は、カルボニル基に共役した二重結合に対しては α 位であったために塩基で引き抜くことができた。
22.42, 40
与えられた構造より、ニトロソ化合物からオキシムへの変換はどのような反応であるのかを考えよ。
(解答例)
第1級および第2級のニトロソ化合物は、ケト体とエノール体の互変異性化反応と同じ形式により、オキシムに変換することができる。これに対し、第3級のニトロソ化合物は、ニトロソ基の α 位の水素がないから同様の互変異性化をすることができない。
-N=O という部分構造を見ると、窒素と酸素では酸素の方が電気陰性度が高いから、>C=O という部分構造と同じような分極を持つことが推定できる。したがって、ある面では、ニトロソ基をカルボニル基と同様にみなすことができるということである。ニトロソ化合物およびオキシムにおける窒素を炭素に置換してやると、そのままケト=エノール互変異性化反応になる。ただし、ケト=エノール互変異性化反応においては、特殊な状況にある場合を除いて溶液中ではケト体の方が多く存在しているケースが多い。
互変異性化(tautomerization)とは、2つの異性体が、平衡により互いに速く相互変換するような反応をさす。その一例は、ケト=エノール互変異性化反応である。その他の例としては
・イミン ←→ エナミン
・ニトロソ ←→ オキシム
・ニトロ ←→ アシニトロ
などが知られている。
22.43, 41
どの位置が無変換で、どの位置がどのように変換されているか。
(解答例)
ゲラニオールを R-OH と書くと、これに対し、ゲラニル酢酸エチル は R-CH2CO2Et、ゲラニルアセトンは R-CH2COCH3 の構造をもつ。すなわち、ゲラニオール R-OH より対応するハライド R-X を合成し、マロン酸エステル合成およびアセト酢酸エステル合成をすればよい。
1) ゲラニオール R-OH は、PBr3 の処理により、ゲラニルブロマイド R-Br に変換できる。
2) マロン酸エステルを1モル当量の EtONa でエノラートとし、ゲラニルブロマイドと反応させる。
3) 加水分解、脱炭酸し、再度エステル化する。二重結合を持つ化合物なので、Fischer 法ではなく、カルボン酸を塩化チオニル SOCl2 で処理後、エタノールと反応させる。これによりゲラニル酢酸エチルを得る。
2') アセト酢酸エステルを1モル当量の EtONa でエノラートとし、ゲラニルブロマイドと反応させる。
3') 加水分解、脱炭酸する。これによりゲラニルアセトンを得る。
2'') 酢酸エチルを、1モル当量の LDA でエノラートとし、ゲラニルブルマイド R-Br と反応させることで、直接 ゲラニル酢酸エチルを得ることもできる。
22.44, 42
19~22 章の章末にまとめられた「反応のまとめ」を参照すること。また、問い 21.50 の解説も関連しているので参照すること。
(解答例)
種々の方法があり得るが、考え方の例のみを示す。反応条件等は各自章末の「反応のまとめ」等を利用して調べること。
(a) Wittig 反応が利用可能である。もし、Grignard 試薬(MeMgBr)やリチウム試薬(MeLi)を用いると、カルボニルに求核付加したのち、アルコールの脱水で二重結合を生成する際、より安定な多置換の環内のオレフィンを生成してしまうので注意。
(b) (a) で得たメチレンシクロヘキサンに対し、逆マルコフニコフ配向で水和(ヒドロホウ素化反応)し、そのアルコールから臭素化する反応を用いることができる。また、シクロヘキシルメタノールは、ホルムアルデヒドに対してブロモシクロヘキサンから合成される Grignard 試薬を作用させても得ることができる。ブロモシクロヘキサンはシクロヘキサノンのヒドリド還元(NaBH4など)によって生じるシクロヘキサノールから合成できる。
(c) カルボニル基の α 位をベンジル化すればよい。ベンジルブロマイド(PhCH2Br)は、トルエンのラジカル的な臭素化、またはベンジルアルコールの臭素化などで得ることが可能である。
また、19.9 節で学んだエナミンも、α 位のアルキル化に利用できる。問い 23.20 なども参照すること。
(d) モノ置換酢酸としてみた場合、(b) によって得たハロゲン化アルキルを用いたマロン酸エステル合成で合成することが可能である。
リンイリドは一般的にエステルとは反応しないので、シクロヘキサノンと BrCH2CH2CO2Et から誘導したリンイリドとの Wittig 反応により生じるアルケンを接触水素添加、エステルは加水分解する、というルートも考えられる。
ブロモシクロヘキサンから合成される Grignard 試薬 R-MgBr をエチレンオキシド(エポキシド)と反応させると炭素数が2増えたアルコール R-CH2CH2OH を与える。これを臭素化し、更にシアン化物イオンと反応の後加水分解(または、再度 Grignard 試薬としたのち、二酸化炭素と反応)することで目的のカルボン酸を与える。
(e) シアノヒドリンとしたのち、脱水で二重結合を導入、シアノ基を加水分解することができる。
(f) アルケンは脱離反応で生じるから、カルボニル基の α 位をブロモ化し、次いで塩基で脱離すればよい。
(g) (e) で得られる生成物を接触水素添加により得ることができる。また、(b) の途中で生じる1級のアルコール(シクロヘキシルメタノール)をクロム酸等で酸化しても対応するカルボン酸となる。ブロモシクロヘキサンから合成される Grignard 試薬を二酸化炭素で処理してもよい。
22.45, 43
二置換シクロアルカンの cis- 体および trans- 体が相互変換するためには、いずれかの置換基において、環の上下が入れ替わる必要がある。すなわち、その置換基の結合した炭素において立体が反転しなければならない。
問い 22.38 ~ 22.41 あたりの解説をよく読むこと。
(解答例)
塩基によって炭素の立体が反転することができるのは、カルボニル基(や、共役した多重結合)の α 位に特有である。この異性化は、酸性度が高い水素が塩基によって引き抜かれることで進行する。
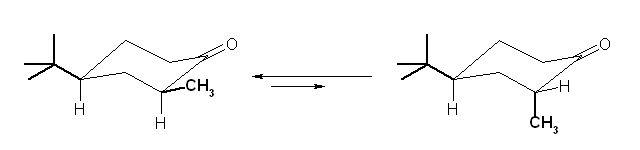
一方、非常に嵩高い置換基である tert-ブチル基は、シクロヘキサン環において、つねにエクアトリアル位をとる。そのため、次図にように、cis- 体においては2位のメチル基はエカトリアル位に、trans- 体においては2位のメチル基はアキシアル位に位置する。したがって、1,3-ジアキシアル相互作用の小さな前者の方が安定である。
22.46, 44
(a) 教科書 22.4節参照。
(b) 教科書 22.8節参照。
(c) 紛らわしいかも知れないがよく見て!
(解答例)
(a) 酸触媒の α 位のハロゲン化反応は、アルデヒド、ケトン(教科書 22.3節)および、酸ハライド(教科書 22.4節、HVZ 反応)に特有の反応で、カルボン酸、エステル、アミドはハロゲン化が起きるほど十分なエノール化は起きない。
(b) diethyl 2-methylpropanedioate (モノ置換のマロン酸エステル)から生じるエノラートを、ハロゲン化アルキル等と反応させることは可能であるが、ブロモベンゼンは芳香族求核置換を受けない。
(c) これはマロン酸エステル合成ではなく、アセト酢酸エステル合成である。したがって、生成物はモノ置換酢酸ではなく、モノ置換アセトンとなる。
22.47, 45
塩基性(H+に対する親和性)と求核性(C+に対する親和性)は同じようなものであるから、程度の差こそあれ、求核種はいつも塩基であり、塩基はいつも求核種であったことを思い出すこと。
(解答例)
重水の処理により、反応系から回収されるシクロヘキサンに重水素 D が導入されるということは、系中ではアニオンを生じていることを示唆している。すなわち、Grignard 試薬が塩基としてα 位の酸性水素を引き抜き、エノラートを生じることで消費されている。
求核種としての反応と塩基としての反応は、常に競争反応となる。tert-ブチル基は立体的に嵩高いから、求核性に劣るため、相対的に塩基としての反応性が見えていると考えられる。すなわち、同じ反応条件でも、Grignard 試薬の種類が変わり、たとえば CH3MgBr のように嵩の小さな(立体障害を受けにくい)求核種にしてやれば、得られる付加生成物の量が増える(または主生成物になる)可能性がある。
同じ理由により、Grignard 試薬はカルボキシ基や水酸基があると、求核攻撃の前に消費されてしまう。また、これを積極的に利用する方法として、R-Br → R-MgBr -(D2O 処理)→ R-D という標識化合物の合成もできる。
22.48, 46
この分子中で最も酸性度の高いのはカルボニル基の α 位で、かつ電子求引性基である臭素の付け根の位置の炭素上の水素である。しかし、Favorskii 転位の反応機構を書くためには、反対側の α 位の水素が引き抜かれるところから始めて書くとよい。途中に、シクロプロパノン型の中間体の構造が書ける。
(解答例)
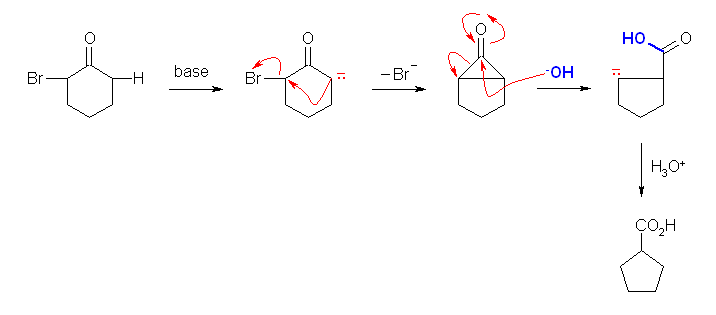
この反応では、シクロプロパノンへの水酸化物イオンの求核攻撃ののち、通常は脱離能のほとんどないアルキル基がカルバニオンとして脱離している。これは、シクロプロパン環のもつ大きな結合角歪みのためであると理解される。脱離によって開環すると、この歪みは解消される。
22.49, 47
ジアゾメタンの共鳴構造を書いてみること。ジアゾメタンの炭素は、孤立電子対による求核性とルイス酸性(すなわち求電子性)とを併せもつ。
(解答例)
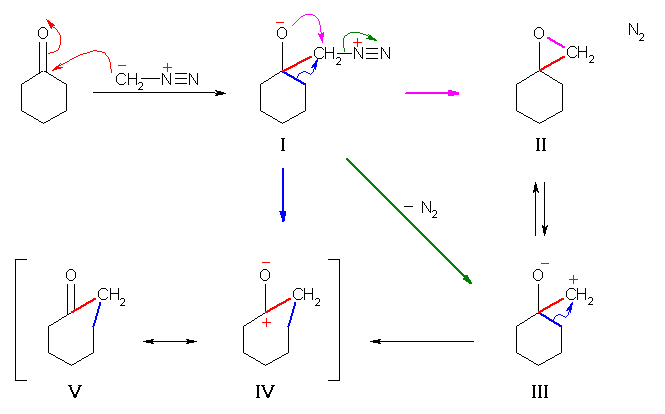
i) ジアゾメタンの炭素(孤立電子対をもつ)が、カルボニル基に求核付加して、中間体 I を生じる。
この中間体 I より、
ii) 負電荷を持つ酸素がジアゾ基をもつ炭素に求核攻撃し、脱離能の高い窒素 N2 が脱離すると、エポキシ環を持つ中間体 II となる。(ピンク矢印)
iii) 中間体 I より、窒素を脱離させると、エポキシ環のひとつの結合が不均一に開裂したような形の中間体 III を生じる。(緑矢印)
iv) この中間体 III をカルボカチオンとして捉えると、その隣接した位置の炭素上のアルキル基(やヒドリド)が、結合電子対をもったまま転位してくる反応があり、その結果として転位生成物 IV を生じる。この転位反応では、III と IV をカルボカチオンとして捉えたときの安定性の差(酸素原子により、III より IV の方がずっと安定である)が駆動力になっていると説明できる。
また、窒素の脱離が隣接炭素からのアルキル基の転位を促進するという観点で書いた反応機構の矢印が、中間体 I から IV への青の矢印である。
v) ところで、この転位生成物 IV は、よく見るとカルボニル基の共鳴で目的生成物である V を書き換えたものに過ぎないことがわかる。
カルボニル基にジアゾメタンが 1,2-付加して中間体 II を生成したあと、形式的なカルボカチオン III への分子内アルキル基の転位により IV を生じるという形で書くか、カルボニル基にジアゾメタンが求核付加して中間体 I を生成したあと、窒素の脱離によって促進され、アルキル基の転位を起こして IV を生じるという形で書くか、については、それぞれの流儀によるといったところだろう。
発展の項にも述べた、アルケンとジアゾメタン(またはカルベン)の反応によりシクロプロパン環を生成する反応との比較では、前者の方が理解しやすいかも知れない。
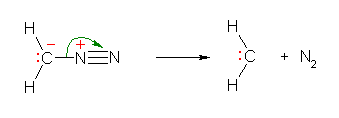
ジアゾメタンは H2C=N+=N- と H2C-−N+≡N の2つの極限構造式を持つような共鳴で書かれるため、後者の構造に由来して、炭素上の孤立電子対による求核性と、(高い窒素の脱離能に由来して、カルベンと同様の)ルイス酸性(すなわち求電子性)とを示す。(ルイス酸性に由来して)炭素上に求核攻撃があると、中性の窒素分子 N2 が脱離する。この N2 は、ほぼ最も強い脱離基である。光などの刺激により分解してメチレン :CH2 (カルベン) を発生することも知られている。
ジアゾメタンの関与する反応として、
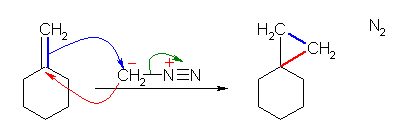
・カルベンとしての反応性については、7.6節で学んだ Simmons-Smith 反応とも関連する。アルケンと反応してシクロプロパン環を与える。
・カルボン酸のエステル化については、問い 21.44 の解説も参照すること。この反応は、フェノールの O-メチル化にも利用できる。(フェノール水酸基は弱いながらも酸性であることを思い出すこと。)
・カルボン酸塩化物との反応(Arndt-Eistert合成)は、Wolff 転位を含み、炭素鎖の伸張反応となる。
なお、ジアゾメタンは反応性が高く、衝撃、熱、光、アルカリ金属の存在により爆発する場合がある。そのため、安全上の観点より、実験室においては、多くの場合、代替試薬としてトリメチルシリルジアゾメタン((CH3)3SiCHN2)などが用いられる。
22.50, 48
p884 化学余話によれば、塩基性条件では、LDA によって生じるエノラートが求核種となり、セレン原子上での求核置換反応でセレノケトンを生じる。これを参考にし、酸触媒での反応条件を検討すればよい。
(解答例)
酸触媒によるケト=エノール互変異性化と、エノールの二重結合の π 電子によるセレン原子上での求核置換反応でセレノケトンを生じる。
22.51-22.55
22.51, 49
(a) 加熱によって容易に脱炭酸するのは、β-ケトカルボン酸の特徴である。マロン酸エステル合成、アセト酢酸エステル合成における加水分解後の脱炭酸の過程を参照すること。
(b) CrO3 による酸化では、第2級アルコールからはケトンが、また、第1級アルコールからはカルボン酸が得られる。
(c) 塩基による加水分解でアルコールを与えるのは、エステルである。
(解答例)
(a) 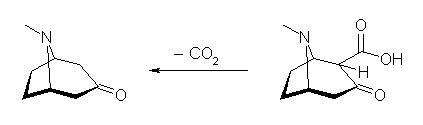
ケト酸:C9H13NO3
カルボニル基の α 位にカルボキシ基が付いた構造は、カルボキシ基が環の面の上下のどちらに結合しているのかに由来する立体異性体がある。また、トロピノンはカルボニルを通る面(プレキラル面)に対して左右対称だから、2つあるカルボニル基の α 位の炭素のいずれにカルボキシ基が結合するのかによって生じるのは、光学異性体である。したがって、4つの構造の候補が考えられる。ここではそのうちの1つのみを示している。
(b) 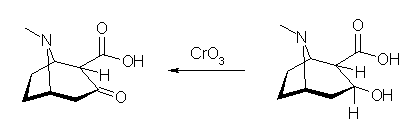
エゴニン:C9H15NO3
(a) のケト酸と分子量を比較すると、酸素数は同じ、水素数が2個多いことから不飽和度の1小さい化合物であることから、(a) のカルボニル基が還元された第2級アルコールであることがわかる。水酸基が面の上下のいずれかの立体化学に由来する異性体が候補である。(解答としては、いずれの異性体でも可である。上図では、天然のコカ葉中のエゴニン Ecgonine の構造を示している。)
(c) 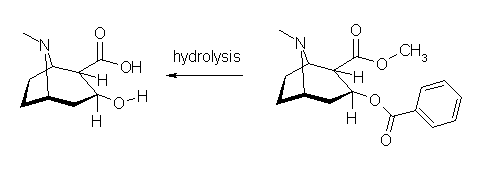
コカイン:C17H21NO4
塩基による加水分解でメタノール、エゴニン、安息香酸を与えるという条件より、エゴニンのカルボン酸をメチルエステルとし、アルコール部分を安息香酸のエステルとした構造が考えられる。この構造は、与えられた分子式と合致する。
コカインの3次元模型
22.52, 50
実際に得られた生成物の構造と、狙っていた目的生成物 ローレン Laurene の構造の相違を見つけること。また、問い 22.34 を参照すること。
(解答例)
原料となる化合物のカルボニル基の α 位での立体が逆転した生成物が得られてしまった。
Wittig 反応(機構は、教科書 p 744、図 19.13 参照)では、分子内のカルボニル基以外の部分に影響はないはずであるから、Wittig 反応に先立って立体の反転が起きていることを示唆する。立体の反転の起きた位置は、カルボニル基の α 位であることから、(リンイリドが塩基として働いて、)エノラートの生成を介したラセミ化(立体の反転の平衡)があるものと考えられる。
ただし、ここまでの説明では、ローレン Laurene およびその立体異性体の混合物となる結果を与える。ローレン Laurene が生成せずに、立体異性体のみが生成したのは、前駆体であるカルボニル化合物において立体の反転の平衡にある2つの異性体のうち、(両者が存在していても)一方のみが選択的に反応した*のか、あるいは平衡が一方に偏っていたのか、どちらかが説明できなければならない。
下図で青で示した結合の周囲の立体に注目すると、より嵩高い置換基(カルボニル基の α 位炭素ではメチル基、カルボニル基の β 位炭素ではトリル基)が、互いにトランス配置になった右側の構造 II(目的とする Laurene ではなく、その立体異性体を与えるような前駆体)の方が安定であることが判る。
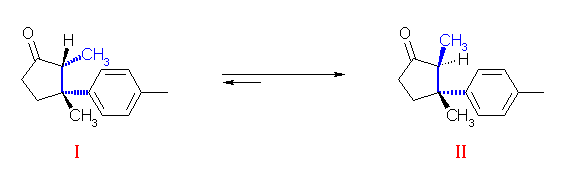
* もし、平衡下の I と II がともに存在しているのに、そのいずれか(生成物の構造を考えると II)のみが Wittig 反応をし、もう一方が Wittig 反応できなかったと考えると、ル・シャトリエの平衡移動の原理から、全量が II の形から反応していくことは説明できる。しかし、均一溶液系での Wittig 反応を考えたとき、I と II の構造にカルボニル基の周辺環境にさほど大きな違いがあるように見えず、一方のみが反応するという説明には無理が生じる。
22.53, 51
問いに与えられた中間体の構造を、出発物質であるケトトシラートと比較して書き直すとわかりやすいかもしれない。どこに新たな結合ができ、どの結合がなくなっているのかを確認すること。
トシルオキシ基 (TsO-)は、優れた脱離基である。これは、脱離したトシラート(TsO-)の共役酸(TsOH)が p-トルエンスルホン酸で、強酸だからである。
また、問い 22.19、22.48、22.52 も参照すること。
(解答例)
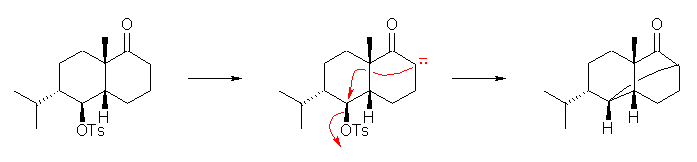
上図に示したような、塩基によるエノラートの生成と、カルボニル基の α 位の炭素による分子内の求核置換反応(SN2)。
最終段階は、カルボニル基からメチレンへの変換であるから、CH3Br から誘導したリンイリド CH2=PPh3 による Wittig 反応をすればよい。問い 22.52 とは異なり、上図右端の中間体の立体反転(やその平衡)は考慮しなくてよい。これは、第1に、カルボニル基の α 位炭素には、α 水素が1つあるが、この位置は橋頭位で C-H 結合の向きがカルボニル π 電子と平行な向きを向いていない(問い22.19を参照)ために酸性ではないためリンイリドによってエノラートを生じないためである。また第2に、環の構造上の制約からも、この炭素上での立体反転は生じることはできない。
22.54, 52
アセトアミドマロン酸エステルは、マロン酸の活性メチレンの位置にアミド基(アセチルによって保護されたアミノ基)が置換されたものと考えてよい。最終的に、アミノ酸(H2N-CHR-CO2H)に転換する際にこのアセチル保護基は加水分解により外される。なお、アラニンは、H2N-CHR-CO2H の表記では -R = -CH3 である。
(解答例)
アセトアミドマロン酸エステルの活性メチレンの位置がアミノ酸のカルボキシ基とアミノ基の結合した炭素(H2N-CHR-CO2H)になっていく。まず、EtONa でエノラートとしたのち、ハロゲン化アルキルでアルキル化する。アラニンを得る場合には、CH3Br 等を用いる。酸性水溶液で加熱することで、エステルおよびアミドの加水分解と脱炭酸が進行する。
22.55, 53
問題文には指示がないが、共通の出発物質から目的とするすべてのアミノ酸が得られるべきである。アミノ酸(H2N-CHR-CO2H)は、アミノ基とアルキル基 -R とをもつ酢酸として捉えることができるから、ここでは、マロン酸エステルがその共通の出発物質の1つとして利用できる。
HVZ反応については、教科書 22.4 節を参照のこと。
(解答例)
1) マロン酸エステル合成により、適切なカルボン酸(R-CH2CO2H)を得る。ロイシンを得る場合は、(CH3)2CHCH2Br をハロゲン化アルキル R-Br として用いればよい。
2) 次いで、HVZ反応により、カルボキシ基の α 位を臭素化する。R-CHBr-CO2H を得る。
3) 最後にアンモニアによるアミノリシス(臭素の結合した炭素上での、アンモニア窒素による求核置換反応)により、 α アミノ置換カルボン酸 R-CH(NH2)-CO2H が得られる。
ただし、問い 22.54 の方法においても、問い 22.55 の方法においても、光学異性体の等量混合物を与える。