24.01-24.10
24.01, 01
エーテルは、酸素の両側にアルキル基がついているのが当たり前で、非対称だった場合には、英語で「アルキル基1」+「空白文字」+「アルキル基2」+「空白文字」+「エーテル」と命名したが、アミンでは、たとえ2級でも「空白文字」を含む命名はしない。
第1級アミン RNH2 は、「アルキル置換基の名前の後に」接尾語 -amine をつけるか、または「母体分子の名前の後に」接尾語 -amine をつける方法で命名できる。butylamine という名称は前者に従いつけた名前で、butanamine や、1,4-butanediamine (or butane-1,4-diamine) という名称は後者に従いつけた名前である。
(a) 非対称な2級アミンだから、長い方の鎖を含む部分を母体とし、窒素上に置換基をもつ1級アミンとして命名する。「窒素上の」を表す "N-" は、イタリック(斜体)であることに注意せよ。
(c) 非対称な3級アミンである。(a) に準じて命名できる。
(b)(e) 対照な第2級および第3級アミンは、アルキル基に倍数接頭辞をつけて命名する。
(d) 環状のアミン(複素環アミン)であるので、固有の母体名を知らなければならない。教科書の説明に続いて描かれている構造については、名称を覚えること。
(f) 2価のアルキル基としてより、アルカンの母体名+接尾語 -amine として命名した方が単純である。
(解答例)
(a) N-methylethylamine,
(b) tricyclohexylamine,
(c) N-methyl-N-propylcyclohexylamine,
(d) N-methylpyrrolidine,
(e) diisopropylamine,
(f) 1,3-butanediamine (or butane-1,3-diamine)
(a) 1-methylethylamine と命名すると、isopropylamine, CH3CH(CH3)NH2 の構造となってしまう。
(f) アルキル基の場合は、遊離炭素(アルキル基のねもと)を1位とするので、sec-butylamine, CH3CH2CH(CH3)NH2 を系統名とするならば、1-methylpropylamine という命名になるが、「アルキル基の名前」ではなく「母体分子の名前」の後に接尾語 -amine をつけて命名しているのだから、NH2CH2CH2CH(CH3)NH2 は1-methyl-1、3-propanediamine とはならないことに注意する。
24.02, 02
必ず英語として名称を記述できるようにしてください。
(b) アリル(allyl)とアリール(aryl)を間違えないように。また、 allyl 基の構造を、vinyl 基と間違えないように。
(解答例)
(a) triethylamine
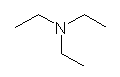
(b) triallylamine
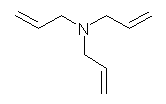
(c) N-methylaniline
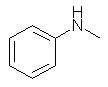
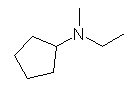
(d) N-ethyl-N-methylcyclopentylamine
(e) N-isopropylcyclohexylamine
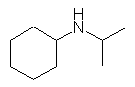
(f) N-ethylpyrrole, or 1-ethylpyrrole
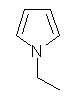
pyrrole は、窒素を含めた環の名前であるから、N-alkyl という置換基名は、位置番号で 1-alkyl と表現しても良い。
24.03, 03
環状のアミン(複素環アミン)の固有の母体名は覚えなければならない。番号のつけ方は、原則(環内の窒素を1位とする、縮合環の場合2つの環に共有される(置換される水素を持たない)炭素を抜かして周り順に番号をつける、など)で覚えておく。
(解答例)
(a) 5-methyoxyindole
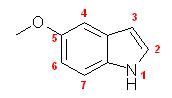
インドール環は、ベンゼン環とピロール環が縮合した形である。ピロールは二重結合の位置が固定である(窒素が二重結合と単結合を持つ形にすると、窒素上の水素を結合できない)が、ベンゼン環内の二重結合の位置は、通常の共鳴のルールにのっとってどちらの共鳴構造で描いてもかまわない。インドール環として書く場合も、ベンゼン環内の二重結合の位置は特に固定されないので、共鳴構造として2種類の描き方ができる。
(b) 1,3-dimethylpyrrole
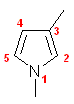
5員環を形成している窒素、炭素はすべて sp2 混成であるから、xylene と同じように2つのメチル基は5員環と同じ平面内に結合している。
(c) 4-(N,N-dimethylamino)pyridine
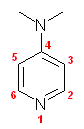
(b) 5-aminopiperidine
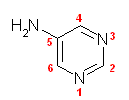
24.04, 04
アミンの塩基性が高いということは、窒素上に孤立電子対が局在化していて、その電子密度が高いということである。そして、水素との結合を作りやすい。共役酸は弱酸である。もし、アミンの孤立電子対が共鳴構造により(=分子内に非局在化して)安定化していくのであれば、水素との結合を作りにくく、塩基性が低い。「共役塩基の安定な酸は、強い酸である。」「弱塩基の共役酸は強い酸である。」
これらの塩基の pKb、またはこれらの塩基の共役酸の pKa のデータを調べれば、塩基性の比較をすることができるが、問題に与えられた組み合わせのように塩基性に大きな差があるものについては、これらデータが与えられなくても判断できるように、塩基性の差が生じる理由を理解すること。
(解答例)
(a) ethylamine is more basic than acetamide.
アミドは、窒素に隣接したカルボニル(弱い電子吸引性基)があるため、窒素の孤立電子対はカルボニル上に広がっている。そのため窒素の求核性、塩基性ともに低くなっている。
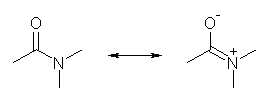
(b) sodium hydroxide is more basic than methylamine.
負の電荷をもつ OH- は、中性の分子である RNH2 に比べると、強く H+ を引き寄せるため、強い塩基であると予想できるだろう。これと等価な考え方として、以下のようにしてもよい。すなわち、OH- の共役酸は、水 H2O、アミン RNH2 の共役酸は、アンモニウム RN+H3 である。これらの酸性度を比較することを考えると、正の電荷を持つアンモニウムの方が強酸であると予想できる。
もちろん、電荷だけでは説明できないのは、たとえば同じように負の電荷を持つイオンでも、Cl- のように(強酸の共役塩基であるため)ほとんど塩基性を示さないものもあることからも明らかである。
また、注意しなければならないのは、NaOH と NaNH2 の比較ではないことで、実際これら2つの間の比較となれば、両方とも中性である H2O と NH3 の酸性度で考えることになる。より電気陰性度の高い酸素に結合した水の水素の方が、アンモニアの水素よりも酸性度が高い。したがって、水酸化物イオンの方が、アミドイオンよりも塩基性は低い。
(c) pyridine is less basic than dimethyamine。
アルキルアミン類と、アリールアミン(アニリンなどの芳香族アミン)や複素環アミンにも大きな塩基性の差がある。
芳香族アミンでは(フェノキシドの負電荷がベンゼン環のオルト位、パラ位に非局在化したのと同様に)孤立電子対がベンゼン環上に非局在化し、塩基性は弱くなる。
ピリジンの塩基性が弱いのは、窒素の孤立電子対が s 性の高い sp2 混成軌道に入っているからである。s 性が高いということは、その電子が原子核に強く引かれているので、他の原子( H+ )との結合形成に利用されにくい。すなわち塩基性が低い。この考えを更に演繹させると、ニトリル類( R-C≡N: )の塩基性についても類推が可能となる。ニトリルの窒素が持つ孤立電子対は、sp 混成軌道(s 性 50%)に入っており、ピリジンに比べてさらに塩基性が低いと結論される。
ピロールのような、窒素の孤立電子が 6π 系に含まれるような複素環についていえば、この孤立電子対が他の原子( H+ )との結合形成に利用されると芳香族性を失うため、ほとんど塩基性を示さない。
24.05, 05
共役酸のより弱いほうの塩基が、より強い塩基である。アンモニウムイオンは、アミンの共役酸。
塩基性度定数の取扱い(教科書 24.4 節参照)より、pKa + pKb = pKw (25℃においては、pKw = 14 )の関係がある。
(解答例)
与えら得た2つの間の比較では、共役酸であるアンモニウムイオンについてその酸性度の低い( = pKa のより大きな )ものは、プロピルアンモニウムイオンである。したがって、プロピルアミンの方が強塩基である。
pKb = 14 - pKa で計算すると、ベンジルアミンは 4.67、プロピルアミンは 3.29である。pKb は値が小さい方が強塩基である。
24.06, 06
芳香族アミンでは(フェノキシドの負電荷がベンゼン環のオルト位、パラ位に非局在化したのと同様に)孤立電子対がベンゼン環上に非局在化し、塩基性は弱くなる。したがって、その効果は、ベンゼン環の p-位についた置換基が電子吸引性基であるか、電子供与性基であるかによって変わってくる。より強い電子吸引性基が付いたほうが(フェノールでは酸性度が上がったように)アニリンの塩基性度は下がる。
なお、命名の上では、アミンは官能基の中で優先順位(教科書下巻、巻末付録 A 表 A-2 を参照すること)が低い方であるから、他の官能基がある場合にはそちらが主官能基となり、母体が「アニリン」ではない命名となるが、この問いにあたえられている化合物は、構造上、いずれも X-C6H4-NH2 である。
(解答例)
p-位の置換基が電子供与性から電子吸引性になる順に並べればよい。以下、カッコ内にはアニリンを母体として見たときのp-位の置換基を示した。
(a) p-bromoaniline ( -Br )>
p-aminobenzaldehyde ( -CHO )>
p-nitroaniline ( -NO2 )
(b) p-methylaniline ( -CH3 )>
p-chloroaniline ( -Cl )>
p-aminoacetophenone ( -C(=O)CH3 )
(c) p-methylaniline ( -CH3 )>
p-(fluoromethyl)aniline ( -CH2F )>
p-(trifluoromethyl)aniline ( -CF3 )
24.07, 07
ニトリル R-CN は、LiAlH4 などによるヒドリド還元により、1級アミン R-CH2NH2 へと変換することができる。ニトリルを直接還元しても、2級や3級のアミンを得ることはできない。
教科書 18章、章末問題 18.38 ででてきた強力なアルキル化剤 Meerwein試薬 R'3O+BF4- は、ニトリル R-CN をアルキル化して R-C≡N+-R' (N-アルキルニトリリウムイオン)を与える。これは、NaBH4 により還元されて、2級のアミン R-CH2NH-R' となる。
酸アミド類 RCONH2、RCONHR'、RCONR'2 は、いずれも LiAlH4 などで還元されて、アミン RCH2NH2、RCH2NHR'、RCH2NR'2 を与える。とはいえ、他のエステルなどの官能基に比べると、還元される速度はずっと遅いため、アミドとエステルやケトンを含む化合物を、アミド部分だけ残して選択的に還元することも場合により可能である。ボラン BH3 での処理や、1- プロパノール中での金属ナトリウム処理によっても同様の酸アミドの還元反応が進行する。
(解答例)
(発展)
ニトリルの還元に用いることのできる還元剤は、LiAlH4 のほか、BH3-Me2S などがある。NaBH4 は単独ではニトリルを還元しないが、CoCl2 を触媒として加えたアルコール溶媒中でや、ラネーニッケル共存下では還元を行うことも知られている。
R-CN → R-CH=NH の反応の生成物は imine イミンである。イミンは、更に還元されるとアミン R-CH2NH2 となるが、その前に加水分解されるとアルデヒド R-CH=O となる。したがって、ニトリルの還元で、反応系中に生じたイミンを単離せずに加水分解すればアルデヒドを得ることが可能である。ニトリル R-CN にグリニヤル試薬 R'-MgBr を反応させて生じたイミンの塩 RR'C=N-MgBr+ を加水分解することでケトン R-C(=O)-R'が得られ、また、ニトリル R-CN に無水塩酸存在下アルコール R'OH を付加させるて生じる R-C(OR')=NH を加水分解することでエステル R-CO2-R' が得られることと対応している。
Stephen 還元 R-CN → R-CHO
ニトリル R-C≡N は、窒素の電気陰性度が高いため、炭素上に正の部分電荷を持っている。塩酸が付加すると、R-C(Cl)=NH2+Cl- のような塩を生じるが、これを無水の SnCl2 で還元すると、イミン R-CH=NH が SnCl4 の錯体として沈殿する。これを加水分解することでアルデヒドとなる。この Stephen 還元は、主に芳香族のニトリル Ar-CN での合成例が多く知られている。Ar-C(Cl)=NH2+Cl- のような塩は、Ar-CONHPh を PCl5 で処理することでも生じる。これを無水の SnCl2 で還元、加水分解してアルデヒドへ変換する方法は、Sonn-Müller 法と呼ばれている。
24.08, 08
学生実験で学習した、エステルのケン化(アルカリ性条件下での加水分解)反応の機構と同じように考えればよい。すなわち、(エステルと同様に)イミドのカルボニル基に、水酸基が求核付加するところから反応は開始される。これにより環の開裂がおきアミド酸(分子内に、カルボキシ基とアミド基を持つ分子)が生じる。続いて、同様の反応がアミドのカルボニル基に対しておきればアミンとフタレート(フタル酸イオン)となる。
(解答例)
24.09, 09
ハロゲン化アルキル R-Br をアミン R-NH2 にする反応経路を2つ示す。教科書 24.6 節参照のこと。アンモニアとの反応では、第2級、第3級のアミンや、第4級のアンモニウム塩が副生する。第1級のアミンを選択的に合成するための方法には、アジド合成、ガブリエル合成などがある。
(解答例)
(発展)
ハロゲン化アルキル R-Br より、チオール R-SH を選択的に合成する際にも、水硫化物イオン SH- を用いたのでは(アミンの合成では、第2級アミンに相当するような)スルフィド R2S が副生するので、その代わりにチオウレアを用いた。教科書 18.9 節参照。
24.10, 10
ニトリルの還元の途中に生じたイミンは、加水分解によりアルデヒドを与えた。この逆の反応により、アルデヒドやケトンはアミンと脱水縮合してイミンを与え、更にイミンが還元されるとアミンとなる。(問い 24.7の発展など、参照)
アミン窒素の孤立電子対が、カルボニル基を求核攻撃するところからはじまる求核付加によりイミンを生じる反応を、還元剤の存在下で起こすのが還元的アミノ化と呼ばれる反応である。アンモニアを用い、カルボニル化合物とのイミン中間体を経ると、1級アミンを生じる。1級および2級のアミンとカルボニル化合物との間でイミン中間体を生じさせ、これを還元すると、2級および3級のアミンが得られる。
この反応の機構から考えて、目的生成物となるアミンが2級以上である場合は、その前駆体であるイミンは1種類だけとは限らない。この問いでも、(a)、(c) はそれぞれ2つの組み合わせがある。(b) も2級のアミンであるが、窒素上の一方のアルキル基(フェニル基)に、α 水素がないため、これは前駆体となるイミンは1種類しか考えられないことになる。
(解答例)
(24.07-24.10 は、現在ヒントのみです。)
24.11-24.20
24.11
問い 24.10 と同様に考えること。
(解答例)
24.12, 11
Hofmann 転位の反応機構(教科書24.6節、図24.5(5版、6版とも))を参照すること。Hofmann 転位では、窒素上に置換された臭素がアニオンとして脱離する際に、隣接位の炭素からアルキル基が移動する過程を含むのに対し、Crutius 転位では、アジドの窒素から N2 が脱離する際に隣接炭素からアルキル基が移動する過程を含む。
(解答例)
24.13, 12
トータルの反応としてどのような変化が起きているのかについて、反応機構とともに押さえておかなければならない点である。そうでないと、このような問題は解けない。また、自分であるターゲット分子の合成のルートを考えるときにも必要となる。
Hofmann 転位および Crutius 転位は、いずれもトータルでは R-COX → R-NH2 のタイプの反応式となる。
(解答例)
24.14, 13
Hofmann 脱離は、教科書 24.7 節に述べられているように、R-X より Zaitsev 則とは逆の位置選択性で HX が脱離してアルケンを与える反応である。
すなわち、Zaitsev 則では、R-Br などハロゲン化アルキルから HBr などハロゲン化水素が脱離し、二重結合に結合したアルキル基がなるべく多いようなアルケンを与える。このようなことは脱離基 X- が容易に脱離しうる時に実現される。すなわち、この反応における遷移状態は生成物により近い構造を持つようになるため、熱力学的により安定な生成物を与える経路において低い活性化エネルギーとなるため、そのような生成物として多置換アルケンを与える。
これに対し、Hofmann 脱離では、X として比較的脱離しにくい窒素(4級のアンモニウム塩より3級のアミン)が脱離するために、遷移状態においても、この過程に先立って塩基によるプロトンの脱離過程が十分に進行して(かつ、まだ X の脱離過程が十分に進行していないような)カルボアニオン的な性格を持つ。つまり、プロトンの脱離のしやすい(その水素の酸性度が高い)側で二重結合を形成していく。言い換えるなら、E1CB 的な性格を持つ脱離反応となる。カルボアニオンは(電子供与基である)アルキル置換の少ないほうが安定となるから、結果として置換数の少ないアルケンを与える。
以上の酸性度による説明は、教科書でなされている「塩基により立体的に空いているほうの水素が引き抜かれる」という立体要因による説明と矛盾せず、同じ立体化学(位置選択性)を与える。実際には、これらの両方の寄与があると考えられる。
(解答例)
24.15, 14
この反応は、分子内での脱離となるが、2級のアミンのままでは進行しない。
Hofmann 脱離反応は、4級のアンモニウム塩からの3級アミンの脱離で進行する。したがって、1回脱離が起きたあと、3級アミンを再度4級アンモニウム塩に戻す過程を経なければ2回目の脱離は起きない。
(解答例)
24.16, 15
チアゾール( C3H3NS の5員の複素環 )骨格部分は、自分で合成しようとせずに、2-aminothiazole を用いたらよい。
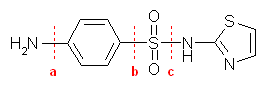
上図の、a, b, c の結合形成を、どの順で行うのかを考える際に気をつけることは、それぞれの反応に対する位置選択性である。必要に応じて官能基を保護する必要がある。
(解答例)
24.17, 16
(b)~(c) は、置換基導入をどの順で行うかがポイントである。先に導入した置換基が続く反応に対する位置選択性が、オルト-パラ配向性であるのか、メタ配向性であるのかを考えればよい。また、必要に応じて官能基を保護する必要がある。
(解答例)
24.18, 17
5版で、「(e) m-1,2,4-トリブロモベンゼン」は、誤植。正しくは、「(e) 1,2,4-トリブロモベンゼン」。
まずは、与えられた名称に対応する構造式を描いてみること。
ジアゾニウム置換反応では、Ar-NH2 → Ar-X の変換が起こる。X として導入することが可能な置換基は、ハロゲン、水酸基、シアノ基などである。また、これらの置換基を変換することにより、X としてエーテル基、カルボキシ基(およびカルボン酸の誘導体であるエステルやアミド)、アルデヒド基なども適用可能である。(教科書 24.8 節、図 24.6 参照のこと。)また、ベンゼン環上のアミノ基は、一般的な方法としてニトロ基を還元する方法で得られる。すなわち、Y-Ar-X が目的生成物だとして、X がジアゾニウム置換反応で導入される置換基だとすると、Y を導入するタイミングによって大きくわけて以下のルートで合成することになる。
Ar → Y-Ar → Y-Ar-NO2 → Y-Ar-NH2 → Y-Ar-X
Ar → Ar-NO2 → Y-Ar-NO2 → Y-Ar-NH2 → Y-Ar-X
Ar → Ar-NO2 → Ar-NH2 → Y-Ar-NH2 → Y-Ar-X
それぞれ、反応の配向性に注意してこの順を決めることになる。ただし、アミノ基は必要に応じて保護される必要がある。
(a),(b),(d) のカルボキシ基は、1) 側鎖のアルキル基またはアシル基を酸化する、2) シアノ基を加水分解する、などの方法で導入可能である。
(解答例)
24.19, 18
問題文の上の図からもわかるように、ベンゼンジアゾニウム塩と、N,N-ジメチルアニリンのアゾカップリング反応により合成される。したがって、ベンゼンを原料として、ベンゼンジアゾニウム塩および、N,N-ジメチルアニリンを合成することを考えればよい。この両者は、いずれもアニリンから合成できる。
「合成する方法を考えよ」という問いに対しては、合成のルートだけではなく、それぞれの反応に必要な試薬等も併せて示すこと。
(解答例)
24.20, 19
化合物 A から化合物 Bへの変換の条件(アンモニアとNaBH3CN)は、典型的な還元的アミノ化反応である。したがって、化合物 A はカルボニル基を持ち、化合物 B は、その対応した位置にアミノ基を持つ。
化合物 B の 1H-NMR スペクトルにおいて、2.6 ppm 付近に見られる積分比1のピークは、アミノ基の結合した炭素についた水素(化合物 A において、カルボニル炭素だったところ)である。このピークは、高さ比がおよそ 1:3:3:1 の4重線となっているのは、隣接した炭素に3つの水素があることを示唆しており、メチル基の存在を示唆する。
アミノ基の水素(2H)は、1 ppm 付近に幅広いピークとして見られている。
ほぼ同じ位置の 1 ppm 付近には、鋭いピークが2つ見られる。うち、背の低いほうの積分比3のピークは、よく見ると2重線である。これは、1つの水素(アミノ基のつけねの炭素上の水素)とカップリングしたメチル基に由来する。もう一方の背の高いピークは(図からは少し小さく見えるが、組成式から考えて)積分比9で、1重線であることから隣接原子上に水素の無い構造である。
(解答例)
(24.11-24.20 は、現在準備中です。)
24.21-24.30
24.21, 20
青が窒素原子。まずは、骨格構造式に描き直してみること。
(解答例)
(a) N-methylisopropylamine, secondary (2°)
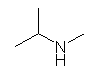
(b) trans-(2-methylcyclopentyl)amine ( 絶対配置で示すなら、(1S,2S)-(2-methylcyclopentyl)amine ), primary (1°)
複合官能基であることを示すカッコ(上、赤字)を忘れてはならない。
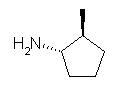
「アルカン+アミン」で命名すると、trans-2-methylcyclopentanamine となる。この場合 cyclopentane の最後の e は、母音アルファベットから始まる amine が続くので省略されていることに注意。
(c) N-isopropylaniline, secondary (2°)
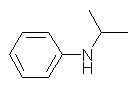
24.22, 21
教科書 24.4 節を参照のこと。
(解答例)
窒素原子のもつ塩基性は、アルキルアミン > ヘテロ環アミン(ピリジン) > アミド窒素 の順になる。アミドは塩基性を持たない。
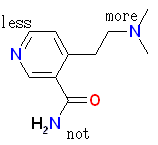
24.23, 22
プロピルアミンの誘導体として命名する。
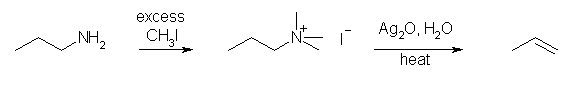
ヨードメタンと酸化銀の処理は、アミノ基の窒素のメチル化反応である。また、生成するアルケンの立体配置(シス-トランス)は、脱離は、常にアンチの位置にある水素が脱離することにより決まる。
(解答例)
出発物であるアミンの名称:
(1S,2S)-(1,2-diphenylpropyl)amine
(カッコ内は、複合官能基、1,2-diphenylpropyl 基である。窒素上にフェニル基のある化合物(N,N-diphenylpropylamine)と間違える可能性があるから、カッコは省略しない。)
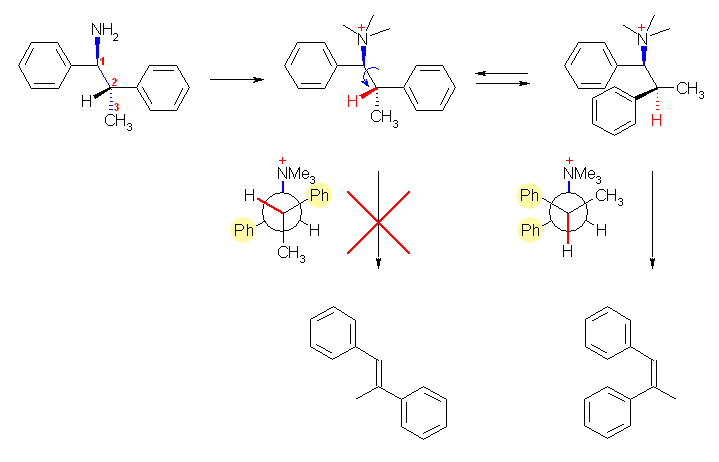
脱離反応は、アンチ脱離で優先的に進行するから、
(Z)-1,2-diphenyl-1-propene を与える。
24.24
教科書 24.4 節を参照のこと。Indole 環の窒素は、pyrrole とほぼ同じ塩基性を持つものと考えてよい。
(解答例)
Indole 環の窒素は、pyrrole と同様に、窒素の孤立電子対が芳香環の π 系の一部として使用されていて、環全体に広がっており、ルイス塩基性を示さない(ルイス酸に配位しにくい)。静電ポテンシャルマップからもわかるように、アルキルアミン部分の方が電子密度が高く(赤く)なっており、より塩基性であると考えられる。
24.25, 23
(b) および (c) は複数の窒素原子を持つから、それぞれについて解答すること。
(解答例)
(a) 第2級
(b) ともに第2級
(c) Indole 環部分の窒素は、第2級。もう一つのアミン窒素は第3級。なお、アミド窒素も第3級である。
24.26, 24
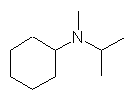
5版のみの問題:(f) N-イソプロピル-N-メチルシクロヘキシルアミン
カッコで括られている部分は、複合官能基名でひとつの置換基に対応するものとなっている。
(解答例)
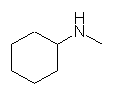
(a) N,N-dimethylaniline
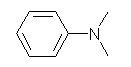
(b) (cyclohexylmethyl)amine
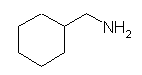
(c) N-methylcyclohexylamine
(d) (2-methylcyclohexyl)amine, or 2-methylcyclohexanamine
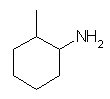
(e) 3-(N,N-dimethylamino)propanoic acid
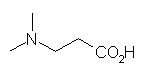
(f) N-isopropyl-N-methylcyclohexylamine
24.27, 25
複合官能基には、カッコをつけて表すこと。
(解答例)
(a) 2,4-dibromoaniline, (b) (2-cyclopentylethyl)amine, or 2-cyclopentylethanamine, (c) N-ethylcyclopentylamine, (d) N,N-dimethylcyclopentylamine, (e) N-propylpyrrolidine, or 1-propylpyrrolidine, (f) 4-aminobutanenitrile
24.28, 26
(a) ~ (c) ともに、条件に合致する化合物は複数考えられる。
(a) キラルであるから、その中心原子である窒素にはすべて異なる置換基が結合している。第4級アンモニウム塩であるから、それらの置換基はアルキル基(アリール基, -Ar を含む)である。水素は不可。
(b) 複素環とは、炭素以外の原子(硫黄、酸素など)を含む環状化合物の総称である。その中でも芳香族性を示すものを、複素環式芳香族化合物と呼ぶ。したがって、単に複素環のものという指定であれば、必ずしも芳香族性のものである必要はない。
(解答例)
以下は、一例である。条件を満たせば他の構造でもよい。
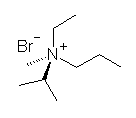
(a) (S)-ethylisopropylmethylpropylammonium bromide
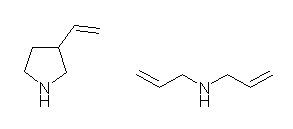
(b) 左 pyrrole、右 pyrrolidine
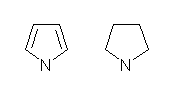
(c) 左 3-vinylpyrrolidine、右 diallylamine
24.29, 27
アニリン誘導体の反応性は、窒素の孤立電子が共鳴的にベンゼン環上に流れ込む(共鳴効果によりアミノ基が強い電子供与性基として働く)ことに由来する。したがって、フェノール(酸素上に孤立電子があるため、水酸基は同様に共鳴効果による強い電子供与性基である)と類似の反応性を持つことに留意する。ただし、(b) のような条件では、フェノールは塩基性条件下、フェノレートにしないと反応しなかったのに対し、窒素は酸素より求核性が高く、アルキル化が容易に進行する。
(a) および (e) では、m-メチル基が反応の配向性にどのような影響を与えるかに注意すること。
(解答例)
(a) Br2 と芳香環の反応は、π 電子によって誘発された正の部分電荷を持つ臭素が求電子試薬として働いて生じるイオン的な性格をもつ置換反応である。したがって、反応式は、Ar-H + Br2 → Ar-Br + H-Br である(教科書 16.1 節参照)。また、新たに導入される臭素は、電子吸引性により求電子置換反応に対して不活性化基としてはたらくから、反応生成物よりも出発物質の方が臭素とより速く反応する。したがって、1当量の臭素により1箇所のみが臭素化されたものが生じると考えてよい。
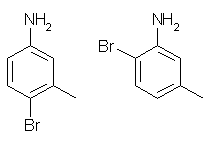
この反応においては、メチル基、アミノ基ともに電子供与性基であるが、アミノ基の方がずっと大きな効果を持つ。したがって、臭素はアミノ基に対してオルト、パラの位置に置換される。(結果としては、メチル基に対してもオルト、パラの位置になるが。)メチル基とアミノ基の間の位置への置換は立体的に不利であるため、反応の条件によっては生成しにくい。
左 4-bromo-3-methylaniline, 右 2-bromo-5-methylaniline
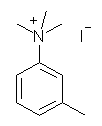
(b) 徹底的メチル化の条件であるから、第4級のアンモニウム塩を生じる。
(c) Friedel-Crafts アルキル化反応の条件である。ベンゼンからは、トルエン(や、キシレンなど、複数の位置にメチル化されたものも含めて)などが生じる条件であるが、アニリン類を用いる場合は、注意しなければならない。アミノ基はプロトン性の酸の存在下、プロトン化を受けて第4級のアンモニオ基となる。また、アミノ基はその他のルイス酸にも強く配位する(下図)。これらは、いずれも窒素上に正の電荷を持つため、強い電子吸引性基としてはたらく。(下図では、矢印を使った配位結合で表しているため、形式電荷を表記していないが、窒素上に正の、アルミ上に負の形式電荷がある。)Friedel-Crafts 反応は、強い電子吸引性基をもつ芳香環の上では起きない。(ニトロベンゼンなども、Friedel-Crafts 反応の基質とならないので、溶媒として用いることもできるほどである。)この反応の場合も、Friedel-Crafts 反応は起きない。もし、Friedel-Crafts アルキル化反応を起こしたいのあれば、アミノ基をアセチル化(この問いの (d) 参照)し、塩基性を示さないアミドとした後に、同じ条件を作用させればよい。
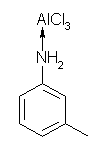
(d) N-アシル化は、アニリンの窒素が求核種として作用する、カルボニル求核置換反応である。
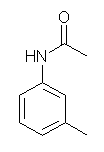
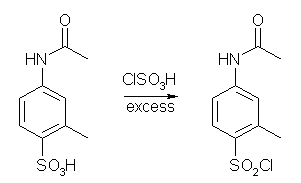
(e) クロロスルホン酸(クロロ硫酸、chrolosulfonic acid, chrolosulfuric acid, sulfuric chlorohydrin ) HSO3Cl ( HO-SO2-Cl ) は、硫酸(スルホン酸)H2SO4 ( HO-SO2-OH ) のモノ酸塩化物である。芳香環のスルホン化(教科書 16.2 節)には、濃硫酸、発煙硫酸や SO3 のほか、クロロスルホン酸などが用いられる。このスルホン化は芳香族求電子反応で、HSO3+ や SO3 が求電子種としてはたらく。形式的に、硫酸から HSO3+ イオンを生じるためには、まず強酸性条件下にプロトン化を受けた硫酸 ( HO-SO2-OH2+ ) より、中性の水が脱離すればよい。これは、酸性条件における第3級アルコールからのカルボカチオンの生成と似ている。クロロスルホン酸は、スルホン酸の一方の水酸基が塩素基となっていることにより、その脱離が起きやすく、HSO3+ イオンを生じやすいと考えられる。したがって、この試薬はスルホン化剤としてはたらくものと理解できる。置換(スルホン化)の起こる位置については、(a) と同様である。
クロロスルホン酸を用いた同じ条件によって、芳香環のスルホン化以外に、クロロスルホン化を生じることが知られている *。これは、中間体として生じた芳香族スルホン酸が、過剰のクロロスルホン酸との反応で生じるものと考えられている。( *:出典 J. March, "Advanced Organic Chemistry" (4th edition), pp528-529. )
24.30, 28
(b) は、窒素原子の塩基性に由来する反応である。
(e) は、アミンが酸として作用する反応である。これは、グリニヤル試薬が相対的により強い塩基であるからである。
(a), (d) は、窒素原子のもつ求核性による反応である。
(c) のジアゾ化も、亜硝酸より生じたニトロソ二ウムイオンによる窒素上のニトロソ化に端を発するから、ニトロソ二ウムイオンから見た場合には求電子反応、窒素原子から見た場合には求核反応である。(芳香族化合物のニトロ化が、芳香族求電子反応であったことを思い出すこと。)
(g) では、芳香族ジアゾニウム塩に対して、芳香族求核置換反応が生じる。これは、窒素分子 N2 が、非常に脱離しやすいためである。(ブロモベンゼンのような化合物では通常の条件では芳香族求核置換反応を示さない。)
一方、(h) は、前の問いの (a), (e) で見たのと同様に、芳香族求電子反応である。アシル基で保護されたアミノ基、すなわちアミド基は、まだ十分に強い電子供与性基である。
(f) の反応は、(g) と条件が似ているが、アニリンのアミノ基がアシル化されていないことに注意しなければならない。このため、アミド基とは異なり、アミノ基が十分な塩基性を残しているため、酸との反応が起こる。プロトン酸の存在下 Ar-NH2 → Ar-NH3+ となるように、ルイス酸の場合は、Ar-NH2 → Ar-NH2+-AlCl3- のように配位が起こる。この結果、窒素上に正の電荷が生じるから、ベンゼン環上の電子は強く吸引されるため、芳香族求電子反応はおきない。(アミノ基は強い電子供与性基である。また、アンモニオ基は強い電子吸引性基である。)
(解答例)
(a) 徹底的メチル化の条件なので、第4級アンモニウム塩を生じる。
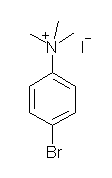
(b) 塩酸塩を生じる。
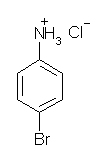
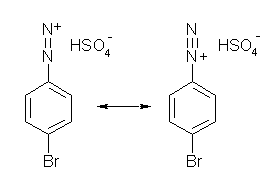
(c) ジアゾ化の条件である。亜硝酸 HNO2 の代わりに亜硝酸ナトリウム NaNO2 を用いる場合もあるが、酸性条件で行うから同じである。生じたジアゾニウム塩は次図のような共鳴構造を持つ。
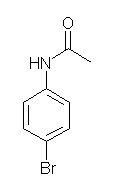
(d) アセチル化である。前の問いの (d) では、塩基触媒としてピリジンを用いている。
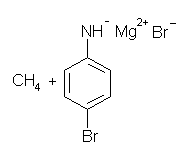
(e) アルカンは有機物の中で酸としては一番弱いものである(メタンの pKa ~ 60)から、その意味で、その共役塩基であるグリニヤル試薬(厳密には、メタンの共役塩基はメチルアニオン CH3- であるが、反応において、メチルグリニヤル試薬とメチルアニオンは等価であると考えてよい場合がほとんどである。)は、アミンなどと比較にならないほど強塩基である。したがって、1級アミンとグリニヤル試薬を混合すると、アミンは酸として反応する。したがって、メタンとアミドイオンを生じる。
(f) 前問の (c) を参照のこと。
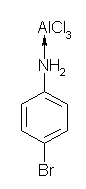
(g) ジアゾニウム塩の反応(Sandmeyer 反応)については、教科書24.8 節を参照のこと。
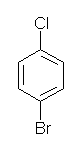
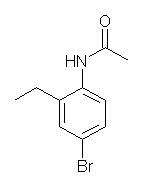
(h) (f) および 前問の (c) とは異なり、アミノ基がアセチル化され、塩基性度の小さなアミドとなっているため、ルイス酸の配位による不活性化はおこらず、Friedel-Crafts アルキル化が起きる。
求電子反応に対する反応は、臭素が(不活性化基でありながら)オルト、パラ配向性ではあるが、アミノ基(および、アシル化されてアミドとなったときのアセチルアミノ基)のオルト、パラ配向性の方が強く、優先となる。
図ではモノ置換体のみを挙げたが、副生成物として2置換体が生じる可能性もある。その場合はアセチルアミノ基のオルト位の両方がエチル化されたものであると予想される。
24.31-24.40
24.31, 29
「合成する方法」として、試薬等(特に必要な場合は、反応条件も)を示せばよい。
(a), (b), (e) アミンの合成の一般的な反応は、ハロゲン化アルキルから出発するものであった。したがって、まず、アルコールをハロゲン化アルキルに変換する。目的物が、(a) では1級のアミン、(b) では2級のアミンであることに注意して、反応を選ぶ。いずれも、アミン(やアンモニア)とハロゲン化アルキルの反応では混合物が得られるため適切ではない。2級や3級のアミンを選択的に合成するためには、対応する酸アミドを還元するか、または対応するアルデヒドを用いて還元的アミノ化反応をするとよい。
(c) 炭素数が1つ少なくなっていることに注意する。このような反応として、 R-COX → R-NH2 のタイプの反応式を用いることができる。すなわち、Hofmann 転位または Crutius 転位が使用できる。
(d) 炭素数が1つ増えている。すなわち、炭素-炭素の結合形成が起きている。炭素-炭素結合を形成する反応の典型的なものは、正の部分電荷を持つ炭素上で、負の形式電荷(または部分電荷)を持つ炭素により求核置換が起きる例である。ハロゲンや酸素、窒素などのヘテロ原子と結合した炭素は正の部分電荷をもつ。負の形式電荷を持つ炭素は、ずっと例は少ない。たとえば Grignard 試薬のような有機金属試薬、または CN- のようなイオンである。
ハロゲン化アルキルと CN- の反応によって生じるニトリルは、還元によりアミンに、加水分解によりカルボン酸になる。カルボン酸は還元されてアルコールを生じるから、炭素鎖を1つ伸ばす反応の例として覚えておくべきである。
ハロゲン化アルキルは、Grignard 試薬とすることが可能であれば、ついでカルボニル化合物との反応で任意の炭素数の増えたアルコールとすることが可能である。このような反応も、炭素鎖を伸ばす反応の例として覚えておくべきである。
(f) アルコールからアルケンを得るためには、単に脱水すればよいのであるが、この反応では、炭素数がひとつ減っているのでそのままでは使用できないことに注意する。すなわち、(c) の反応を利用することを考える。ただし、アミンをアルコールに戻さなくても、アミンを出発物質としてアルケンにすることができる。Hofmann 脱離は、その位置選択性に特徴があるので、併せて整理しておくこと。
(解答例)
(a) ハロゲン化アルキルより1級のアミンを合成するときは、アジドを経由してこれを還元するか、N-アルキル化されたフタルイミドを経由する Gabriel 合成を用いる。アルコールをアルデヒドとしたのち、還元的アミノ化の条件を用い、イミンを還元してもよい。(下のスキームでは中間体であるイミンを明示しているが、イミンを単離する必要はなく、ワンポットで合成する。)
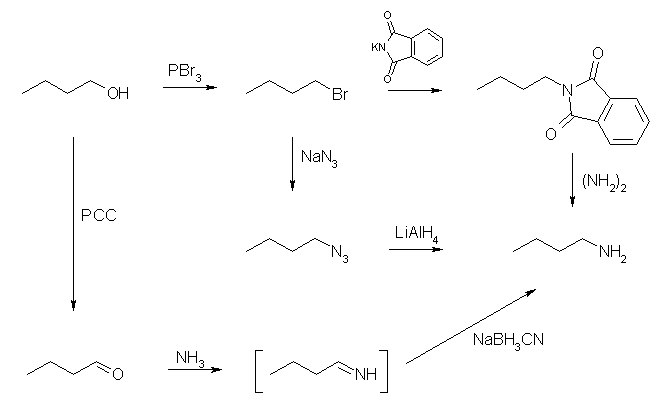
(b) 2級のアミンを得るための、酸アミド、イミンのいずれも、(a) で合成したブチルアミンを用いて合成することになる。酸アミドを得るためには、アルコールを対応するカルボン酸に、イミンを得るためには、アルコールを対応するアルデヒドにそれぞれ酸化する必要がある。
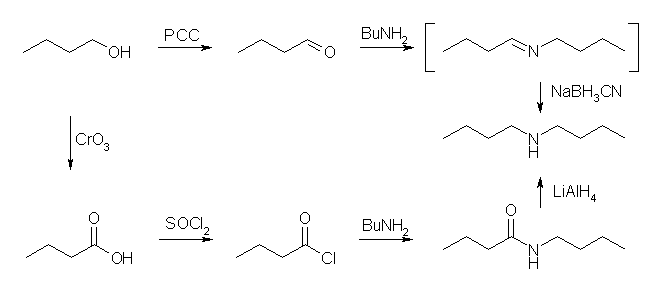
(c) Hofmann 転位または Crutius 転位を利用する。ブタン酸塩化物までは (b) と同様にして合成するものとし、その続きを示す。
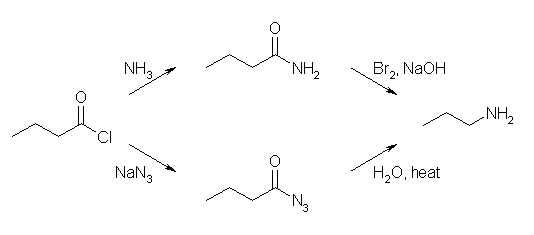
(d) グリニヤル試薬経由で、ブタノールより炭素鎖のひとつ伸びたペンタノールを合成することができる。これと (a) を組み合わせれば解のひとつであるが、ハロゲン化アルキルからニトリルとすることで、直接炭素の1つ多い化合物に変換することができる。
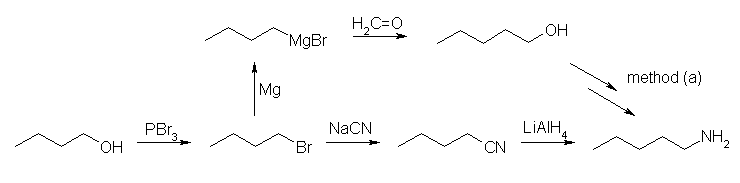
(e) (a) で合成したブチルアミンを用いて、CH3I でメチル化する方法は、条件により第4級アンモニウム塩を副生してしまうため、一番良い方法ではない。還元的アミノ化を用いる方が選択的である。
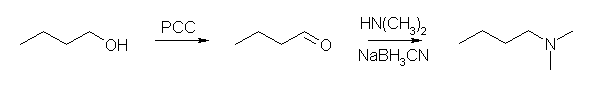
(f) 脱離における位置選択性は、この生成物(propene)の場合は考慮に入れなくてよいが、Zaitsev 則に従うものではより多置換の(安定な)アルケンを生じ、Hofmann 脱離においては、最も置換の少ない(末端の)アルケンを生じる。特に、酸性条件下でのアルコールからの脱離では、カルボカチオンからのプロトンの脱離によるアルケンの生成と、アルケンへのプロトンの付加がともに生じるため、アルケンの位置は容易に移動してしまう。
この問いにおいては、位置選択性を考慮しなくてもよいので、1- および 2- ハロゲン置換のプロパンからの Zaitsev 脱離によっても、1- および 2- アミノプロパンからの Hofmann 脱離によっても同じ生成物を得る。
出発物質であるブタノールよりも炭素数が3と、1つ短いから、(c) で合成した propylamine を出発物質としたルートを示す。
24.32, 30
「合成する方法」として、試薬等(特に必要な場合は、反応条件も)を示せばよい。
(a) カルボン酸の誘導体の合成については、教科書 21章(21.3 節など)を参照すること。
(b) 炭素数が1つ減っていることに注意。上の問いの (c) などを参照すること。
(c) 炭素数は維持のまま、アミンとしている。カルボン酸は、還元によりアルコールになると考えれば、上の問いの (a) と同じように考えることができる。また、(a) で酸アミドとしたものを還元してもよい。
(d) カルボン酸の α 位の臭素化反応である。教科書 22.4 節を参照すること。(教科書 24章の範囲ではない。)
(e) 教科書 21.8 節を参照すること。炭素数が同じニトリルを合成するなら、酸アミドを脱水することにより得られるが、この問いでは、炭素数が1つ増えている。上の問いの (d) も参照すること。
(f) 上の問い (d) を参照すること。
(解答例)
以下のような言葉だけではなく、反応スキームを構造式を用いて描いておくこと。また、反応機構の不明なものについては、きちんと調べておくこと。
(a) 塩化チオニル SOCl2 で処理して酸塩化物としたのち、アンモニア NH3 で処理。
(b) (a) で得た pentanamide を、臭素と塩基で処理して、Hofmann 転位させる。
(c) (a) で得た pentanamide を、水素化リチウムアルミニウム LiAlH4 で還元する。
(d) 臭素 Br2 と三臭化リン PBr3 の混合物で処理し、Hell-Volhard-Zelinskii 反応(教科書 22.4 節参照のこと)により、α 臭素化する。
(e) ペンタン酸を還元して 1-pentanol とした後、PBr3 で処理して 1-bromopentane とし、シアン化ナトリウム NaCN による求核置換反応(求核種は、シアン化物イオン CN-)を行う。
(f) (e) で得た hexanenitrile を水素化リチウムアルミニウム LiAlH4 で還元する。
24.33, 31
アニリンのような芳香族アミンの合成法において、アルキルアミンとの差は、一般的に芳香族求核置換反応が利用できないため、対応するハロゲン化物からの合成以外の方法を考えなければいけないことである。また、ニトリルや酸アミドを還元した場合も、ベンゼン環とアミノ基の間にメチレン CH2 が入ってしまい、芳香族アミンにならない。
(a) フェノール類やアリールエーテルが、芳香環上に電子吸引性基があり、活性化されているなどの例外を除いて、芳香族求核置換反応では合成できなかったのと同様、アニリン類も、芳香族求核置換反応(アンモニアなど、孤立電子対をもつアミンが求核種)では合成されない。
芳香族アミン(アニリン類)の合成に一般的に用いられるのは、ニトロ基の還元である。(3年でやった学生実験を思い出すこと。)
(b) また、Hofmann 転位または Crutius 転位も芳香族アミンの合成に適用可能である。
(c) メチル基は脱離基として働かないから、直接の置換反応による他の置換基への変換はできないから、これを何か別の形に変換してからアニリンへ持っていくことを考える。トルエンのメチル基は、ハロメチル基 -CH2Br や 水酸化メチル基 -CH2OH、アルデヒド基 -CHO や カルボキシ基 -CO2H などへと誘導することができる。
(解答例)
以下のような言葉だけではなく、反応スキームを描いておくこと。また、反応機構の不明なものについては、きちんと調べておくこと。
(a) 混酸(硝酸 HNO3 と硫酸 H2SO4 の混合物)にてニトロ化し、ニトロベンゼンとしたのち、これを金属スズ Sn(または、塩化スズ(II) SnCl2)を塩酸中で作用させる。生じるアニリン塩酸塩は、塩基で処理することにより、アニリンを遊離させる。
(b) 臭素と塩基で処理して、Hofmann 転位させる。
(c) トルエンを酸性の過マンガン酸カリウム KMnO4 溶液で処理することにより、安息香酸 PhCO2H となる。安息香酸への変換を、より温和な条件で行うためには、トルエンのベンジル位を臭素化(NBS, BPO)し、酢酸ナトリウムによる求核置換反応(休核種は、酢酸イオン CH3CO2-)して benzyl acetate (PhCH2OCOCH3) としたものを、アルカリにより加水分解して benzyl alcohol (PhCH2OH)を得た後、これをクロム酸 CrO3 で酸化してもよい。安息香酸を塩化チオニル SOCl2 で処理して酸塩化物としたのち、アンモニア NH3 で処理すると benzamide (PhCONH2)を得るので (b) に帰着する。
24.34, 32
(a), (b) ジアゾニウム塩を経由することで、アミノ基はさまざまな置換基へ変換することができる。(b) のカルバモイル基( -C(=O)NH2 )は、カルボキシ基( -C(=O)OH )からの誘導、またはシアノ基( -CN )の加水分解で得ることができる。
(c) しかしながら、アミノ基を直接的にアルキル基に置換することは(おそらく)できないので、この変換は、アミノ基の除去とメチル基の導入の2段階で行う。(もちろん、そのような意味では、(b) の問いも、(a) でベンゼンへと変換している以上、そのベンゼンからベンズアミドへと変換するルートも可能であることになるが、まぁ、これは考えなくてよいだろう。
(解答例)
24.35
ベンジルアミンは、1級のアルキルアミンであるから、臭化ベンジル PhCH2Br などから各種方法で合成可能なほか、ベンズアミド PhCONH2 やベンゾニトリル PhCN の還元でも得られる。
(解答例)
24.36, 33
(a), (b), (f) 炭素数は同じままである。
(c), (e) 炭素数が1つ増えているから、問い 24.31 (5版では、問い 24.29)の (d) に帰着することを考えればよい。1-ブテンは、1-ブタノールに変換できる(この際、位置選択性に注意すること)ことを考えると、この二つの問題は共通のものと考えてよい。
(d) 炭素数が1つ減っている。問い 24.31 (5版では、問い 24.29)の (c) などと同様に考える。
(e) 5-デセンに比べて、目的物は炭素数が半分である。アルケンを酸化開裂させる反応があったことを思い出すこと(教科書 7.8 節参照)。得られる化合物がアルデヒドの場合は還元的アミノ化により、また得られる化合物がカルボン酸の場合は酸アミドとした後還元により、それぞれ目的物を得ることが可能である。
(解答例)
24.37, 34
Hofmann 脱離反応においては、ハロゲン化アルキルからのハロゲン化物イオンの脱離等とは逆の位置選択性で、4級のアンモニウム塩より中性のアミンが脱離し、4級窒素上のアルキル基のひとつがアルケンとなる。この問いに与えられたような問題の場合には、窒素上のどのアルキル基がアルケンとなるかには、選択の余地がないことに注意せよ。(窒素上のメチル基やフェニル基など、水素を有する β 炭素が存在しない基は、アルケンになりようがないので。)
(解答例)
24.38, 35
(a) Hofmann 脱離である。教科書 24.7 節を参照のこと。ただし、この脱離自体は、「加熱」で進行している。B の構造については、教科書の記述を読むこと。
(b) Crutius 転位である。教科書 24.6 節を参照のこと。
(c) Gabriel 合成法である。教科書 24.6 節を参照のこと。
(d) 「1当量の」とあるから、1対1での反応生成物を考えること。実際に1対1で反応させるためには、反応の条件を工夫する必要がある。
(解答例)
24.39, 36
(a) 還元的アミノ化。
(b), (c) 脱離。
(d) エポキシドへの酸化。教科書 18.7 節参照。
(e) エポキシドに対する求核付加による開環反応。教科書 18.8 節参照。
(解答例)
24.40, 37
(a), (c), (e) は、与えられた反応条件で反応がおきるが、生成に誤りがある。正しい生成物の構造を記すこと。
(b), (d) は、ここに示された条件では、反応自体がおきない。目的生成物を得るための正しい試薬は何かを記すこと。ただし、(d) に与えられた目的生成物は、通常、単離されずに引き続いて別の生成物に変化する。
(解答例)
(24.31-24.40 は、現在準備中です。)
24.41-24.50
24.41, 38
共鳴式がたくさんかけるものの方が安定である。
(解答例)
24.39
ジフェニルアミンは希塩酸に溶けにくい。このことを称して「塩基性ではないようにみえる」と表現している。(「塩基性ではない」ではない。)つまり、問題の趣旨は「希塩酸に溶けにくい理由を示せ」ということと解釈してよい。
(解答例)
24.42, 40
「 塩基性度が低い = その共役酸の酸性度が高い 」という図式を思い出すこと。すなわち、アミンの共役酸であるアンモニウムイオンの pKa で議論することができる。
ただし、この問いでは、 pKa の数値から議論するのではなく、構造から議論する必要がある。「 塩基性度が低い = プロトンを受け取りにくい 」ということであるから、「その塩基が単独で安定になる」または「塩基中の孤立電子対が分子全体に非局在化する(広がる)」(← いずれも、共鳴構造がたくさんかける、ということと等価である)ことで説明できる。
(解答例)
(発展)
酸性度や塩基性度に対して置換基が与える影響は、共鳴効果だけではなく、誘起効果による寄与も考える必要がある。
24.43, 41
「ピラミッド反転が非常に速やかに起こる → 鏡像異性体に分割できない(交互に入れ替わってしまう)」
↓
「ピラミッド反転が無視できるほど遅い(または起こらない) → 鏡像異性体に分割できる」
(解答例)
24.44, 42
図 24.4 を参照すること。ただし、接触水素還元ではなく、ヒドリド還元であることに注意する。ヒドリドは、H- で求核種である。
(解答例)
24.45, 43
例題 24.1 や、問い 24.10 などと同様に考えよ。教科書 24.6 節参照。
(解答例)
24.46, 44
副生成物である、N-メチルジベンジルアミンの構造を描いてみること。その上で、この副生生物が生じるために、どのような反応がおきているのかを考えること。
(解答例)
24.47, 45
メチル基はオルト、パラ配向性であるから、m-キシレンを臭素化すれば、目的物となる可能性がある。しかし、メチル基の配向性を考えると、ベンゼンから出発して m-キシレンを(少なくとも主生成物としては)得ることはできない。
また、臭素も求電子芳香族置換反応に対し不活性化基でありながらオルト、パラ配向性であるから、ブロモベンゼンをメチル化する反応経路を考えたとき、仮に2つのメチル基が臭素に対しオルトおよびパラの位置で置換すれば目的物を与える可能性がある。とはいえ、はじめのメチル化で生じるであろう 4-ブロモトルエンの2段階目のメチル化がどの位置で起こるかを考えたとき、臭素は反応に対し不活性化基で、メチル基が弱いながらも活性化基であることを考え合わせると、4-ブロモ-1,2-ジメチルベンゼンを与える可能性がある。
したがって実際には、アミノ基をジアゾ化して臭素に変える過程を含む経路を考えた方がよい。これは、アミノ基(や、それを保護したアセチルアミノ基)が(メチル基よりも)ずっと強いオルト、パラ配向性で、したがって、反応の起こる位置を決定する際に、より支配的にはたらくと予想されるからである。
(解答例)
24.48
問い 24.39 (e) の過程と同じように、エポキシドに対する求核的な開環反応で生じる。教科書 18.8 節参照。
(解答例)
24.49, 47
目的生成物は2級のアミンである。したがってこれを選択的に得るためには、還元的アミノ化が利用できる。であるから、そのためのカルボニル化合物を、炭素数が5以下のものから作る方法を考えればよい。まずは、シクロペンチル基の部分だけで炭素数が5であるので、これに対応した Grignard 試薬を用いるとよい。
(解答例)
24.50, 48
一般に目的物の構造が判っているものの合成については、逆合成の手法で考えるとよい。すなわち、最終的に D という目的生成物があったとき、その前駆体となりうる構造を考える。その構造は1つとは限らない。C1 および C2 が D へと変換することが可能であるなら、次にこれら C1, C2 へと変換することができる前駆体を考える。B1, B2 が C1 に、B3 が C2 に変換可能であれば、更にそれらの前駆体を考える。A1, A2 が B1 に変換可能で、A3 が B3 に変換可能だとする。また、B2 を合成する方法が見当たらないとする。そうすると、結局、可能なすべての合成ルートは、以下の通りとなる。
A1 → B1 → C1 → D
A2 → B1 → C1 → D
(×) B2 → C1 → D
A3 → B3 → C2 → D
実際には、それぞれのルートの長さもまちまちであるし、もっと複雑なスキームになるだろう。これらを見比べた中で、もっとも効率よく実現できそうなルートを選択することになる。いろいろな合成を知っている方が、最終生成物に辿り着くルートの幅に広がりができ、選択肢が多くなる。
テトラカイン中に含まれる官能基として、ベンゼン環の一方には2級のアミノ基があり、そのパラ位にはエステル結合がある。エステルのアルキル基上には3級のアミノ基がある。
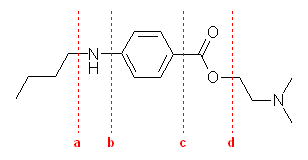
b の結合はベンゼン環上での芳香族求核置換反応が起こらないので、はじめからアニリン誘導体を使うか、フェニル基をニトロ化することで導入するなどするしかない。また、c の結合も、炭素-炭素結合であるから、フェニルグリニヤル試薬と二酸化炭素などを反応させるか、アニリンからジアゾニウム塩経由でシアノ基を導入した後に加水分解するなどの手法で合成することになる。または、Friedel-Crafts 反応でメチル基またはアセチル基を導入して、これを酸化してもよい。
まずは、2級のアミノ基とエステル結合の導入順序を考える。つまり、上図中、a, d のどちらの結合を最後に導入するかであるが、一方の官能基の存在下で、もう一方の官能基を合成することができるかが、鍵となるであろう。
2級アミンは、酸アミドの還元でも合成できるが、この条件(LiAlH4 など)では、一般にエステルも還元されてしまうため、エステル存在下ではこの条件は適切ではない。しかしながら、還元的アミノ化によっても2級アミンを導入できる。したがって、2-(N,N-dimethylamino)ethoxycarbonyl 基をパラ位にもつアニリン誘導体を用いればよいことがわかる。
一般にエステルは、カルボキシラート RCO2- によるハロゲン化アルキルへの求核置換反応でも合成できるが、アミノ基を持つ分子が近傍にあると、ハロゲン化アルキルによるアミンのアルキル化が副生するため適切ではない。また、エステルは酸ハロゲン化物とアルコールの反応でも生じるが、2級アミンの存在下では酸アミドが生じる恐れもあり、2級アミンの導入後のエステル化としてはこの条件は適切ではない。したがって、カルボン酸とアルコールを酸触媒で脱水縮合させることが選択肢となる。
上記のように順を追って考えていくことで最適な合成ルートを見出すことができる。
(a) アニリン誘導体を用いてよいということであるから、上の図の a の結合形成の反応の条件を示せばよい。
(b) p-ニトロ安息香酸を出発物質とするのであるから、上図の a, d の結合を導入することを考えることになる。すなわち、p-ニトロ安息香酸から上の (a) で用いるアニリン誘導体を合成することができれば、(a) に帰着することができる。
(c) ベンゼンから p-ニトロ安息香酸を合成することができれば、(b) に帰着できる。
(解答例)
(24.41-24.50 は、現在準備中です。)
24.51-24.60
24.51, 49
「塩基による加水分解で、カルボン酸(トロピン酸)とアルコール(トロピン)を与える」のであるから、アトロピンは、トロピン酸とトロピンがエステル結合した構造を持つ。トロピン酸( 3-hydroxy-2-phenylpropanoic acid )は、構造式が問題文中に与えられている。トロピン酸は不正炭素を持つが、この部分の立体は無視して考えてよい。
「トロピンは光学不活性なアルコールであり、脱水によりトロピデンを与える」のであるから、逆に、問題文中に図で与えられたトロピデンの二重結合に水和した構造がトロピンである。このとき、水酸基の位置は、「光学不活性な」アルコールである点より考えること。ただし、水酸基の位置は決定できても、その立体配置は問題文からは判断できない。実際には、トロピンの水酸基は、窒素を含まない7員環に対して、窒素による架橋とはトランス(環の下側)に結合している。
(解答例)
(発展)
トロピン酸( 3-hydroxy-2-phenylpropanoic acid )は不正炭素を持つが、アトロピン Atropine 中においては、この部分はラセミである。ただし、ベラドンナ、ハシリドコロ、チョウセンアサガオといったナス科植物中では、トロピン酸部分は、(S)-体で存在している。光学活性なものをヒヨスチアミン (ヒオスシアミン) Hyoscyamine と呼ぶ。アトロピンは、これを植物体から抽出するときにラセミ化したものである。ラセミ化が起こるのは、この位置にフェニル基およびカルボニル基が結合しているため、この炭素に結合した水素の酸性度が高いからである。
24.52, 50
トロピリデン( 1,3,5-cycloheptatriene )は、3つの二重結合を持っている。アルケンを合成するためには、脱離反応が利用できる。
(解答例)
24.53, 51
接触還元では、一般にカルボニル基は還元されない。ここでは、まずシアノ基部分が還元される。ただし、最終生成物の組成式は C9H17N であり、酸素を含まない。これは、分子内での還元的アミノ化が起きているためである。
(解答例)
24.54, 52
まずは、Hofmann 脱離生成物である 5-(N,N-dimethylamino)-1-octene の構造式と、その組成式を書いてみること。
脱離によりアルケンを与えるのであるから、生成物の二重結合の炭素のいずれかにもともとアミノ基がついていたことがわかる。コニイン coniine が2級アミンであることから、その位置などがわかる。なお、この問題文で「Hofmann 脱離の条件下で反応」とあるのは、過剰の CH3I で処理して4級のアンモニウム塩にする段階も含むものと解釈してよい。
(解答例)
24.55, 53
問題 24.53 (5版では、問題 24.51)を参照するように指示されているので、同じ方法で合成することを前提に考えてみることにする。すなわち、コニイン合成の最終段階を、分子内の還元的アミノ化で行うものとしたときの前駆体物質(分子内にカルボニル基とアミノ基を含む)の構造を描いてみること。次に、このアミノ基をシアノ基の還元により得るならば、その前駆体であるニトリルはどのような構造であるか。
では、このニトリルを 3-オキソヘキサン酸エチルとアクリロニトリルより合成するにはどうしたらよいか、考えればよい。
3-オキソヘキサン酸エチル(構造を骨格構造式等で書き下してみること)は、典型的な β-ケトエステル(1,3-ケトエステル)である。教科書 22.5 節、表 22.1 などを参考にすること。生じたエノラートアニオンがアクリロニトリルに対して示す反応は、Michaenl 反応(教科書 23.11 節)と類似であると考えてよい。
(解答例)
24.56, 54
プロプラノロール propranolol は、分子内にエーテル結合を持つ。このエーテル結合は、一方がナフチル基であるから、Williamson エーテル合成では、ナフトール(=ヒドロキシナフタレン)より生じさせたアニオン ArO- とハロゲン化アルキルを用いる。ここで、プロプラノロールは、2級アミノ基も含むが、ハロゲン化アルキルとアミンは反応してしまうため、アミノ基の導入はエーテル結合の生成よりも後にしないといけない。
プロプラノロール propranolol と、問題 24.39 (5版では、問題 24.36) の最終生成物の構造の類似性に着目して、合成のスキームを考えること。
(解答例)
24.57, 55
ベンゼンからのフェノールの合成(教科書 17.10 節参照)は、スルホン化後、アルカリ熔融による場合、かなり厳しい条件となるためアルキル側鎖以外の官能基の存在下で適用するのは適切ではない。また、フェノールの合成法として、アニリンをジアゾ化した後に加水分解する方法(教科書 24.8 節、および以下の(発展)項参照)が利用できるが、ジアゾ化は芳香族アミンに限らずアルキルアミンでも起きる。以上を考えると、チラミン Tyramine の末端のアミノ基は水酸基よりも後から導入するほうが良さそうである。
また、エチルベンゼンをハロゲン化して (2-bromoethyl)benzene ( PhCH2CH2Br )は得ることができないが、(1-bromoethyl)benzene は容易に得られる。これはベンジル位の反応性が高いためである。
(解答例)
(発展)
ジアゾカップリングなどの反応時に、ジアゾニウム塩が水と反応して(加水分解により)フェノール類を生成する副反応をおこすことが知られている。この副反応を抑えるために、一般に低温で反応を行う。この副反応を積極的にフェノール類の合成に利用する目的で、水やアルコール中でジアゾニウム塩を加熱すると、対応するフェノール類やフェニルエーテル類が得られる。また、教科書 24.8 節の記述にあるように、硝酸銅(II)水溶液中、酸化銅(I) と反応させることによってもフェノール類へと変換することができる。
形式的には、ジアゾニウム塩に対する芳香族求核置換反応で進行するため、水酸化物イオンを反応させればよいように見えるが、「芳香族ジアゾニウム塩を水酸化ナトリウムで処理してアルカリ条件下で分解するとラジカル機構で進行し、相当するアミノ基位置で二量化したビアリール化合物を与える」という記述があった。( → Wikipedia「ジアゾ化」)
24.58, 46
アゾ色素の合成には、一般的にジアゾニウムカップリング(ジアゾカップリング、アゾカップリング)(教科書 24.8 節参照)が用いられる。ジアゾニウムイオンは弱い求電子種であるため、電子豊富な芳香環に対してしか反応しない。プロントシル prontosil の構造を見てみると、一方の環にはスルホンアミド構造( -SO2NH2 は、アミノスルホニル基である。-NHSO2R がスルホンアミド基。)が結合しており、ジアゾニウムイオンとは反応しにくいと予想される。また、1,2,4-トリアミノベンゼンの1つのアミノ基のみを選択的にジアゾ化することは不可能である。
(解答例)
(発展)
スルホンアミドは、アミノ基の保護基として用いられることもある。一般に、酸性、塩基性、ヒドリド還元、接触還元に対して安定だが、バーチ還元で外すことができる。スルホニル基として代表的なものは、p-トルエンスルホニル基(=トシル基)など。(アルコールをトシル化することで、脱離基に変換できることは、すでに学んだ。)
アミノ基の保護基に使用されるそのほかのスルホニル基として、p-ニトロベンゼンスルホニル基(=ノシル基)が知られている。これは、塩基性条件下チオールを作用させることで容易に脱保護でき、ノシル基で保護した1級アミンを穏和な条件で N-アルキル化できるため、1級アミンから2級アミンの合成する方法として有用である。
24.59, 56
(b) の前駆体として考えられるのは、4-methylbenzonitrile または 1-bromomethyl-4-methylbenzene など。
(c) は、メトキシカルボニル基が電子吸引性基で、メタ配向性をもつことに注目すると、簡単に合成できるように見える。ただし、芳香族求電子置換によるハロゲン化の中でも、ヨウ素化は臭素化や塩素化とは異なる条件が必要であること(教科書 16.2 節)に留意する必要がある。また、ヨウ素をジアゾニウム置換反応により導入するような反応を設計すると、経路は若干長くなるが、個々の反応が効率よくすすめば全体としてより良い場合もある。
ジアゾニウム置換反応を用いるもうひとつの経路として、考えられるのは、メトキシカルボニル基のパラ位に導入されたアミノ基を使って、芳香族求電子置換によるヨウ素化を加速する方法である。アミノ基は、ジアゾニウム置換反応により水素に置換してしまうことが可能であるため、1-bromo-3-methylbenzene のような本来の配向性とは異なる位置への置換基導入のために使用されることもある。
(解答例)
24.60, 57
問い 24.56 (第5版では、問い 24.53) で合成したプロプラノロール propranolol との構造の類似性に注目すると良い。
(解答例)
(24.51-24.60 は、現在準備中です。)
24.61-24.70
24.61, 58
(a) アントラニル酸より生じさせたジアゾニウム塩は、その電荷補償イオンが分子内のカルボキシラートである。
(b) ジエンと特有の反応を示すこの中間体については、すでに教科書 16 章(16.10 節参照)で学んでいる。ジエンとの反応については、教科書 14.8 節を参照のこと。
(解答例)
(発展)
芳香族アミンを亜硝酸 HNO2(←しばしば、強酸の存在下、亜硝酸ナトリウムから発生させる)と処理することにより、芳香族ジアゾニウム塩を生じることをすでに学んでいる。ジアゾニウム塩の構造式を描けば判るとおり、ジアゾニウムイオンは正の電荷を持つ。通常のジアゾニウム塩は、電荷補償イオンとして、HSO4- や ClO4- などの負のイオンを持つ。
芳香族ジアゾニウム塩は、条件により固体として単離することが可能であるが、単離されたジアゾニウム塩は加熱、光照射等の条件下、発熱的に分解して窒素を放出する。(大量のジアゾニウム塩は爆発する場合がある。)(脂肪族アミンから生させたジアゾニウム塩は、芳香環による共鳴安定化がないので、氷冷下においても速やかに分解し、単離できない。)
24.62, 59
問題 24.52 (第5版では、問い 24.50) で、トロピデンよりトロピリデンを合成したのと同じように考える。
さらにシクロオクタテトラエンへ変換する方法については、アルカンからアルケンへの変換として考えればよい。教科書 10.5 節についても参照すること。
(解答例)
24.63, 60
Hofmann 転位により、R-CONH2 → R-NH2 + CO2 の反応がおきる(機構については、教科書 24.6 節、図 24.5 などを参照のこと)。
α-ヒドロキシアミドを出発物質として考えた場合、同様の Hofmann 転位が起きるかどうかは、同じ反応機構を無理なく描くことができるかを考えて判断する。(反応機構、およびここで予想される生成物を、図 24.5 などに倣って描いてみること。)
この問題に与えられた反応の場合は、二酸化炭素だけではなく、更にアンモニアまで脱離している。教科書 19.6 節や、19.9 節などを参考にしながら、通常の Hofmann 転位の生成物の構造が、引き続いてどのような反応を示すのかを考える。
(解答例)
24.64, 61
2段階とも、アミンのもつ求核性がこの反応の原動力となっている。反応の出発原料のアミンは1級であり、はじめに共役求核付加がおこり、2級のアミンを生じる。続いてエステルのカルボニル基への分子内求核攻撃により生成物を生じる。これは、エステルのアミノリシスにより酸アミドを与える反応であり、結果として生成物は環状アミド(ラクタム)となっている。問題文に与えられたセクション(共役付加に対して教科書 19.14 節、カルボニル求核置換に対して教科書 21.2 節)をそれぞれ参照すること。
(解答例)
(発展)
まず、反応物質と生成物質の構造を比較して、どの位置とどの位置で結合が生成しているかを確認してみること。
pyrrolidin-2-one 骨格は、慣用名 pyrrolidone ピロリドンと呼ばれる。したがって、この反応生成物は、4-acetyl-1-methylpyrrolidone と呼んでも差し支えない。
なお、N-メチルピロリドンは、NMP と略されることのある極性非プロトン性溶媒の一種で、高分子分野、リチウムイオン二次電池の合材のバインダ溶媒など、さまざま分野で多用される。沸点 202℃。
また、N-ビニルピロリドンを重合させた構造であるポリビニルピロリドン(PVP)は、非イオン性の水溶性ポリマーで、市販のスティックのりの成分としてなど、幅広い分野で使用されている。
24.65, 62
まず、反応物質と生成物質の構造を比較して、どの位置とどの位置で結合が生成しているかを確認してみること。
はじめに2級アミンがハロゲン化アルキルによりアルキル化される反応が生じる。(アミノ基の求核性により、ハロゲン化アルキルのハロゲンの結合した炭素上で求核置換を起こす。)
つづいて、分子内でのアルコールによる共役求核付加が生じる。
中性の水やアルコールによる求核攻撃は、分子間では速くないが、この反応においては分子内であるために通常よりずっと起こりやすい。
(解答例)
24.66, 63
スペクトル問題につき、省略。
(解答例)
24.67, 64
スペクトル問題につき、省略。
(解答例)
24.68, 65
スペクトル問題につき、省略。
(解答例)
24.69, 66
まず、反応物質と生成物質の構造を比較して、どの位置で結合が切れ、どの位置とどの位置で結合が生成しているかを確認してみること。
問題 24.65 (第5版では、問い 24.62) と同様に、反応は2段階で進行する。まず、ヒドラジン(どちらの窒素も、モノ置換アミンと同様の反応性を示す)により、イミド構造のカルボニルに対して求核的に反応が進行(アミノリシス)して、開環が起きる。つづいて、分子内の共役求核付加が生じる。
ヒドラジンによるアミノリシス(の1段階目)については、Gabriel 合成の最終段階(教科書の記述のような、N-アルキルフタルイミドに対して水酸化物イオンを作用させて開環することにより1級アミンを遊離させる方法以外にも、授業でやったようにヒドラジンを使うことで効率よく1級アミンを得ることができる)と類似である。
(解答例)
24.70, 67
アンモニウムイオンは、アンモニアとの間に酸-塩基平衡にあり、系中で、まずこのアンモニアがアルデヒドと反応してイミニウムカチオンを生じると考えられる。このイミニウムカチオンに対して、シアン化物イオンが求核的に付加することで、この反応は進行する。(還元的アミノ化反応においてはヒドリドが求核種であった。これと同じように反応機構が描ける。)
(解答例)
(24.61-24.70 は、現在準備中です。)