23.01-23.10
23.01, 01
「アルドール縮合」ではなく、「アルドール反応」の生成物を書く。反応機構等は、23.2節を参照すること。
第5版においては、(b) が 2-butanone である。
(解答例)
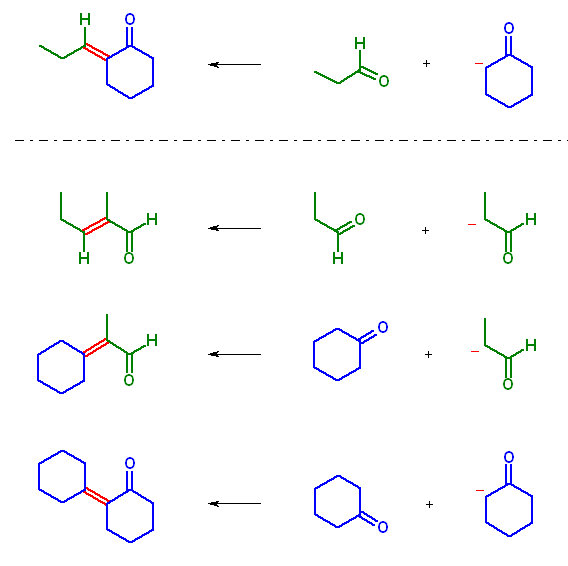
この問いでは、α 水素が1種類しかないアルデヒド、ケトンについての反応であるため、考えられる生成物はそれぞれ1種類のみである。
反応は、1) 一方のカルボニル化合物の α 水素が塩基により引き抜かれ、エノラートを生成。
2) 生じたエノラート(の炭素)により、もう一方のカルボニル化合物に求核付加。
3) 溶媒(アルコール)などから、プロトンを引き抜き、アルドール(β-ケトアルコール)を与える。
の順に進行する。以下、反応と生成物を示す。
(a) 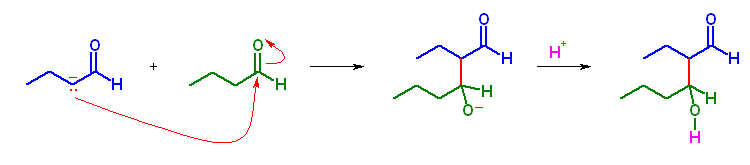
(b) 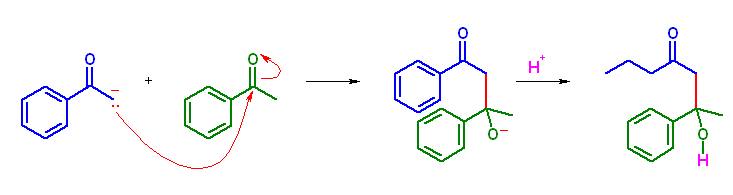
(c) 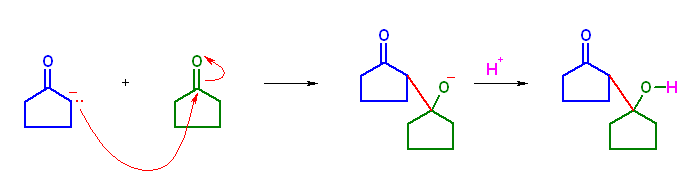
第5版、(b) 2-butanone
2-butanone は、カルボニル基に対し、α 水素が2種類あるので、エノラートも2種類生じる。そのため、生成するアルドールにも2種類の構造が考えられる。
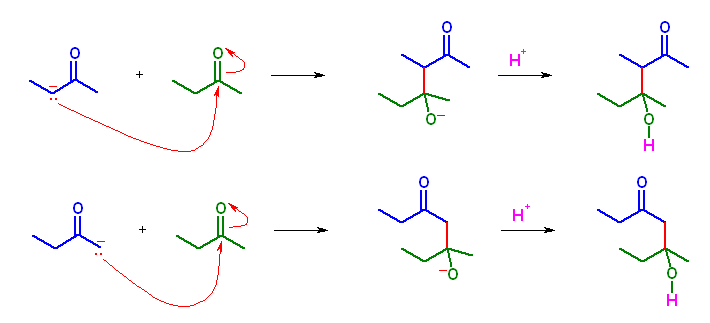
23.02, 02
まず、アセトン2分子のアルドール反応から、4-ヒドロキシ-4-メチル-2-ペンタノンを生じる反応を書いてみること。この反応の逆の過程を考えると、どの結合が変化しているのかがわかりやすい。
(解答例)
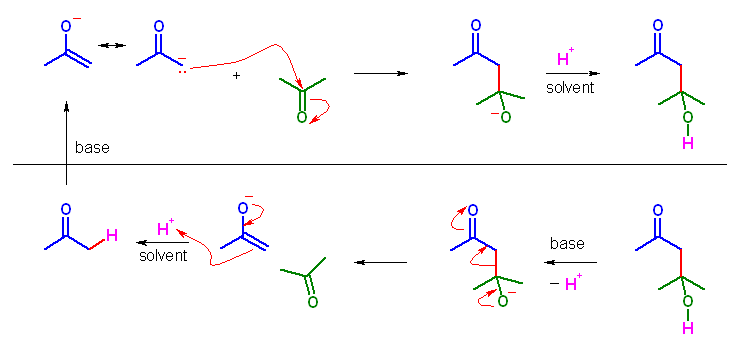
上段は、アセトンより生じるエノラートがもう1分子のアセトンと反応して、4-ヒドロキシ-4-メチル-2-ペンタノンを生じる反応。下段は、4-ヒドロキシ-4-メチル-2-ペンタノンのレトロアルドール反応(逆アルドール反応)により、2分子のアセトンを生じる反応。
ここに示した機構からも判るように、アルドール反応は、塩基触媒の存在下、可逆反応である。
23.03, 03
アルドールよりの脱水の起きる位置は、カルボニルと共役したエノンを与えるが、これは形式的に、もとのカルボニル化合物と同じパターンの位置に二重結合が入ることを意味している。
(解答例)
(a) 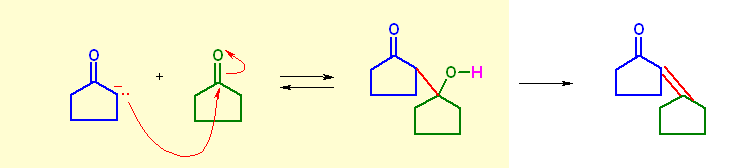
(b) 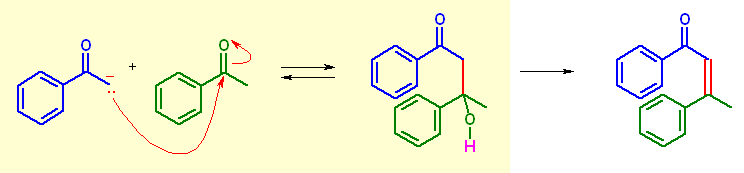
(c) 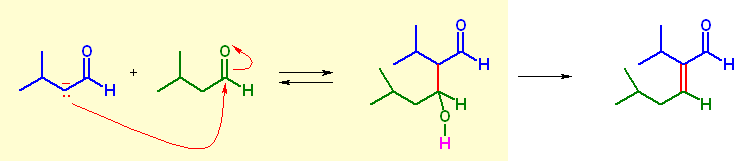
アルドール反応(アルドールの生成)は、塩基触媒の存在下、可逆反応である。アルデヒドのような基質では、この平衡が生成物側に傾くが、ケトンからはじめる場合は、この平衡が出発物よりに傾く。しかし、その先の脱水は可逆的ではあるが、生成物側(脱水側)に大きく傾くので、「アルドール縮合」としてみた場合は、生成物側に傾く形になる。上図では「生成物側に大きく偏った平衡」を非可逆のように一方向の矢印のみで表している。
アルドール縮合が塩基触媒で可逆であるということは、エノンに対して水酸化物イオンが付加してアルドールを形成する過程があるということを意味している。
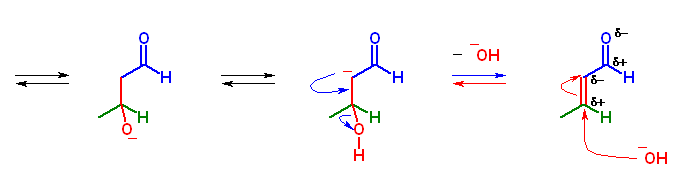
この求核攻撃は、カルボニルに共役した C=C 二重結合が、カルボニルの分極の影響を受けて、カルボニル α 炭素が δ- に、カルボニル β 炭素が δ+ に分極していることにより生じることが可能となる。
23.04, 04
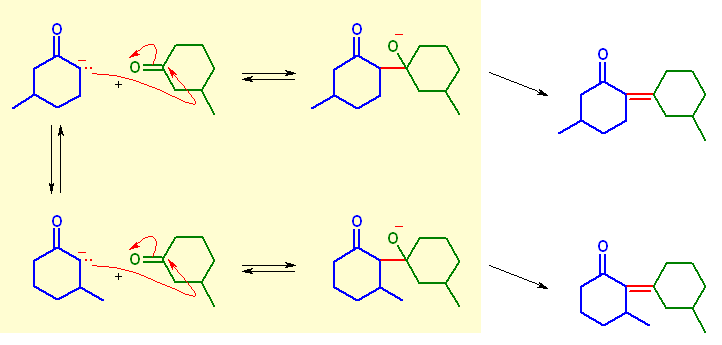
3-メチルシクロヘキサノン は、2種類のカルボニル基の α 水素を持つ。
(解答例)
23.05, 05
問い 23.03 の反応機構を見て、パターンを探してみること。選択肢に与えられた化合物名を構造に直し、そのパターンを持つかどうかを調べればよい。
第5版には、(a) として次の選択肢あり。(第5版での (b), (c) は、第6版の (a), (b) )
3-hydroxy-2,2,3-trimethylbutanal
(解答例)
アルドール反応およびアルドール縮合で生じるのは、β-ヒドロキシカルボニル化合物、および、α,β不飽和カルボニル化合物(共役エノン)である。
(a) 2-hydroxy-2-methylpentanal は、アルドール反応では生じない。
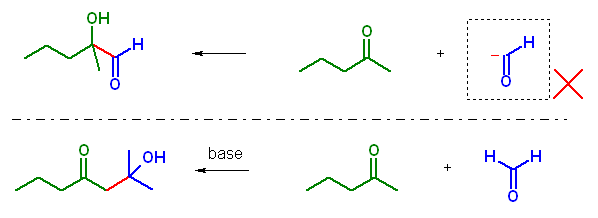
上図上段のように、2-hydroxy-2-methylpentanal の赤で示した結合がカルボニルに対する求核攻撃で生じると考えるなら、ホルムアルデヒド H2CO の共役塩基が求核種でなければならないが、通常、このようなアニオンは生じない。ホルムアルデヒドの水素は、カルボニル基に対する α 位ではなく酸性度も小さい。もし、2-pentanone と ホルムアルデヒドの反応を塩基性の条件にすると、上図下段のような生成物をはじめ、2-pentanone が2種類の異なる α 水素を持つことに由来する構造異性体や、2-pentanone 同士のアルドール生成物などが生じることになる。
(b) 5-ethyl-4-methylhept-4-en-3-one は、 pnetan-3-one 同士のアルドール縮合によって生じる。
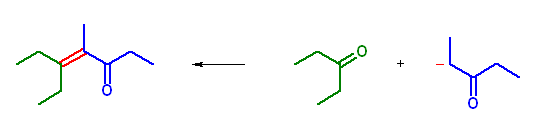
5版 (a) 3-hydroxy-2,2,3-trimethylbutanal は、2-methylpropanal のエノラートがアセトンに求核付加して生じるアルドール反応の生成物である。
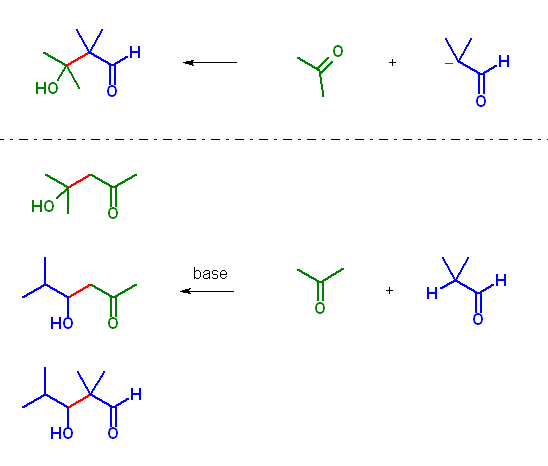
ただし、アルデヒドとケトンでは、求核攻撃を受けやすいのはアルデヒドである。また、エノラートとしてのカルバニオンの安定性は、アルキル置換基が少ないほうが安定である。(カルボカチオンは級数が高いほうが安定であった。カルバニオンは級数が低い方が安定である。)これらのことを考え合わせると、反応の条件にも依るが、2種のカルボニル化合物を混合した中に塩基を加えただけでは、4種のアルドール反応(塩基性条件下では可逆で生じる)の平衡生成物となるが、表題の化合物が主生成物とはなりにくい。
実際問題として、もし2種の異なるカルボニル化合物を用いたアルドール反応を計画する場合は、
1) 一方のカルボニル化合物に α 水素が無いものを選ぶ(そのため、1種類しかエノラートが生じない)
2) または、酸性度の違いなどの条件から、α 水素が1種類ではない場合でも、ただ1種類しかエノラートを生じない系を選ぶ
3) エノラートの求核攻撃を受けるアルデヒドは大過剰に用いる
などの条件を設定してやる必要がある。(23.6節参照)
23.06, 06
アルドール反応(またはアルドール縮合)で反応する2つの分子が異なる場合や、反応箇所が複数ある場合等、その生成物が混合物になる場合には、それらを分離しなければならない。工業的に安価な方法であることを考えると、2つの分子が同じで、かつ α 水素が1種類しかなく、したがって単一の生成物を与えることが前提条件となる。
(解答例)
ethanal (acetaldehyde) のアルドール縮合にて、but-2-enal を得ることができる。ヒドリド還元(NaBH
4) によりアルデヒド基を水酸基まで還元し、次いで、パラジウム触媒を用いた接触水素添加反応で炭素=炭素二重結合を還元すればよい。
なお、acetaldehyde は、ethyne (acetylene) の水和によって得ることができる。
23.07,
エノンの部分がアルドール縮合により生じたと考えることができる。
(解答例)
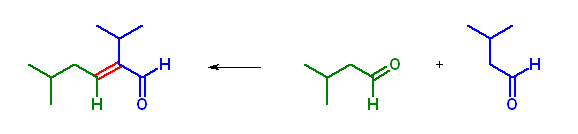
3-methylbutanal 同士のアルドール縮合により、目的物である 2-isopropyl-5-methylhex-2-enal を与える。
23.08, 07
3つともエノンの形になっているから、形式的には混合アルドール反応により生成する。ここでは、単に「混合物の1つとして与える」以上のものはどれであるのかまで考えて解答せよ。
(解答例)
(a) acetone から生じるエノラートが benzaldehyde に対して求核攻撃する組み合わせの混合アルドール反応により生成する。ここで、benzaldehyde は、カルボニル基 α 水素をもたないからエノラートを生じない。また、ケトンよりもアルデヒドは求核攻撃を受けやすい。以上の理由により、この組み合わせの混合アルドール反応では、目的化合物が優先すると考えられる。
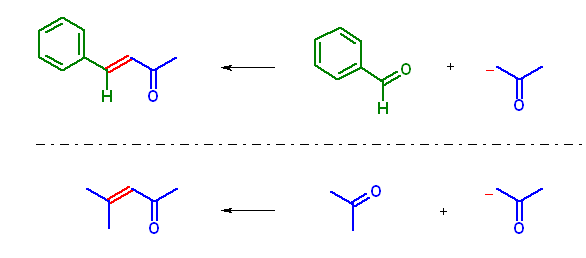
(b) acetone から生じるエノラートが acetophenone に対して求核攻撃する組み合わせの混合アルドール反応により生成する。この組み合わせでは、acetophenone もカルボニル基 α 水素をもつので、エノラートを生じる上、どちらもケトンであるから求核攻撃を同定度にうける。したがって、4種類の反応生成物が同程度生じると考えられる系である。
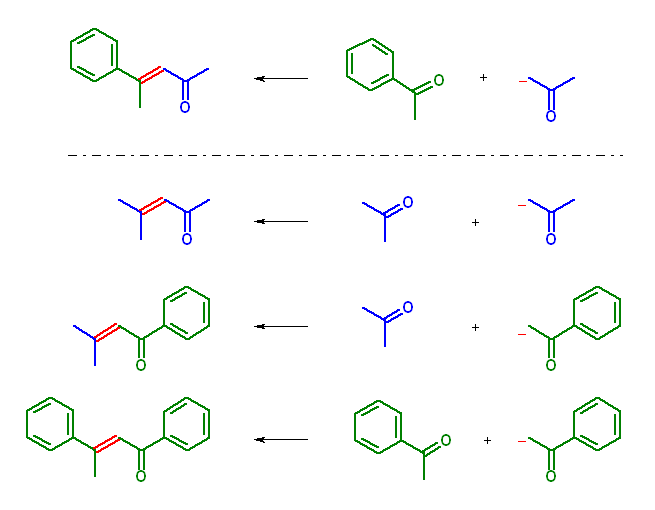
(c) cyclohexanone から生じるエノラートが propanal に対して求核攻撃する組み合わせの混合アルドール反応により生成する。この組み合わせでは、propanal もカルボニル基 α 水素をもつので、エノラートを生じる。ケトンよりはアルデヒドの方が求核攻撃を受けやすいと考えられるが、アルデヒドの方がケトンよりも α 水素の酸性度が高いこともあるので、おそらくアルデヒド同士の反応混合物が主となり、全部で4種類の混合物を与えると考えられる系である。
23.09, 08
ちょっと問題文が変な気がします。もし僕が書き換えるなら次のようにします。:2,4-pentanedione のような 1,3-diketone は、塩基で処理しても分子内のアルドール縮合生成物を与えない。この理由を説明せよ。
図 23.4 も参照すること。
(解答例)
- 1,3-diketone は、2種類の α 水素を持つが、一方(2つのカルボニル基に挟まれた活性メチレンの位置:下図中緑色で示した)の水素は、pKa が 9 前後で、それに対し、もう一方の水素は、(下図中青色で示した水素は、ひとつのカルボニル基としか相互作用できないから、アセトンと同程度の)pKa が 19 前後であり、これらの2種類の α 水素の酸性度にかなりの差がある。これは、とりもなおさず、共役塩基として生じる2種類のエノラートの安定性にかなりの差があることを示している。
- 1,3-diketone が分子内のアルドール縮合をする場合、経路は1つしか考えられない(下図、上より右下への反応)。エノールのアニオン炭素による隣接位のカルボニル基に対しての求核攻撃(下図、左側)は、形式的にエノラートの極限構造式間の変換にすぎず、環状構造を持つような生成物は与えないからである。
- 分子内のアルドール縮合の結果、生じる生成物は4員環で、大きな結合角歪みをもつ。
- アルドール縮合は、塩基触媒存在下、全過程とも可逆である。
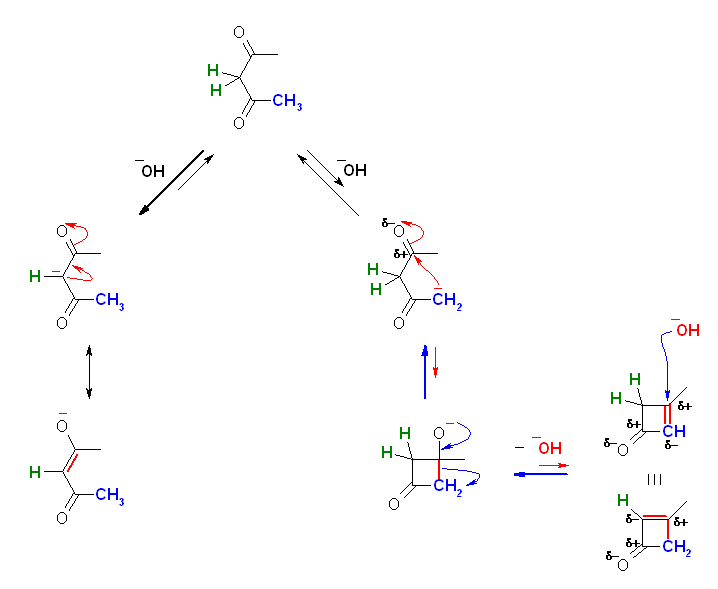
結果として、反応機構上、平衡の一部としてわずかに4員環の分子内アルドール縮合生成物を与えることが可能であるが、この生成物( 3-methylcyclobut-2-en-1-one )は、大きな結合角歪みを持つため不安定であるから、すぐに水酸化物イオンによる開環をうけて逆反応で戻ってしまう経路がある(問い 23.03 の(発展)の反応機構も参照せよ)。一方、同じ平衡にある活性メチレンの位置で生じるエノラートは非常に安定である。結果として、平衡は上図左端のエノラート側に傾くことになる。
23.10, 09
ジケトン化合物であるから、分子内のアルドール反応を考えてみよ。もし、結合角歪みの大きなものでなければ、分子間反応に優先して進行する。
(解答例)
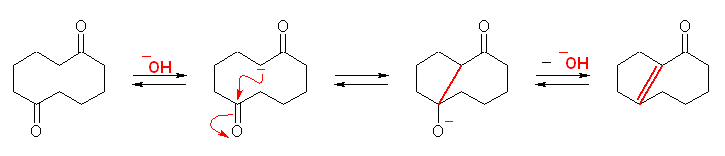
もちろん、下図は上図と全く同じものである。
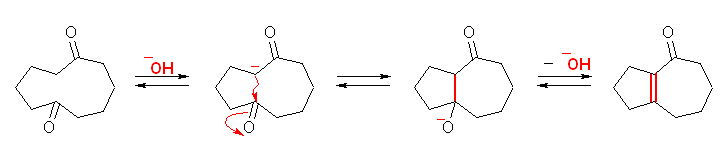
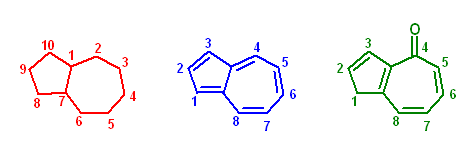
得られる生成物は、bicyclo[5.3.0]dec-1(7)-en-2-one (または、付加命名法を用いて、2,3,5,6,7,8-hexahydro-1H-azulen-4-one )である。
命名に関して、ビシクロアルカンとしての番号は下図左(赤字)、アズレンとしての番号は下図中(青字)となる。命名と比較せよ。なお緑(下図右)では、 1H-azulen-4-one の構造を示した。
23.11-23.20
23.11, 10
例題 23.3 などを参照せよ。
(解答例)
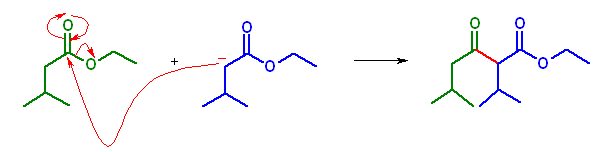
(a) ethyl 2-isopropyl-5-methyl-3-oxohexanoate
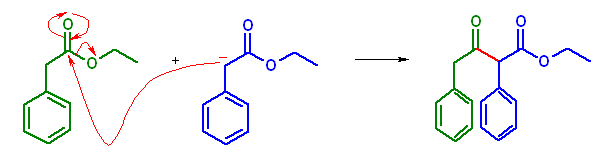
(b) ethyl 3-oxo-2,4-diphenylbutanoate
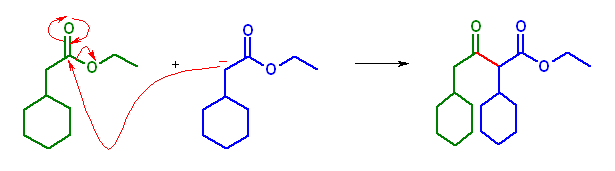
(c) ethyl 2,4-dicyclohexyl-3-oxobutanoate
23.12, 11
図 23.5 を参照せよ。
(解答例)
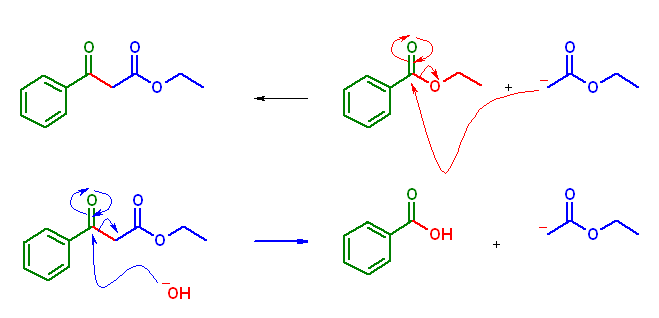
上段の Claisen 縮合により ethyl 3-oxo-3-phenylpropanoate を生成する反応と同じように、下段の逆 Claisen 反応も、カルボニル求核置換反応で進行する。水酸化物イオンがカルボニル基に求核攻撃し、脱離基の脱離によってカルボン酸を与える。
この逆 Claisen 反応での脱離基は、酢酸エチルの共役塩基のエノラートである。酢酸エチルのカルボニル α水素の酸性度は、教科書p872、表22.1 より pKa が 25であり、アルコールよりもかなり酸性度が小さいことから、エステルのケン化における脱離基、-OR より脱離しにくいものと考えられるが、上図では示していないが、更に脱離したアニオンがカルボキシ基の酸性水素を引き抜くため、この反応は生成物側に平衡がずれることが可能となる。(以上、エステルのケン化(塩基性の加水分解)の反応機構、並びにケン化が非可逆となる理由と同じである。)
23.13, 12
例題 23.4 と同様に考えよ。シュウ酸エステルは、α水素を持たない。
(解答例)
methyl 2-(3,3-dimethyl-2-oxocyclohexyl)-2-oxoacetate
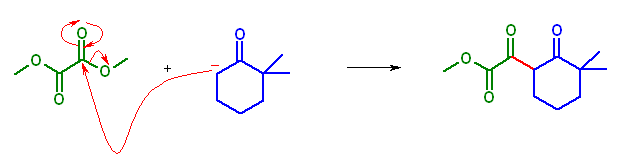
23.14, 13
Dieckmann 環化は、単に Claisen 縮合が分子内で起きるだけだから、反応機構を追えばすぐに生成物が書けるはずである。
(解答例)
ethyl 5-methyl-2-oxocyclohexanecarboxylate
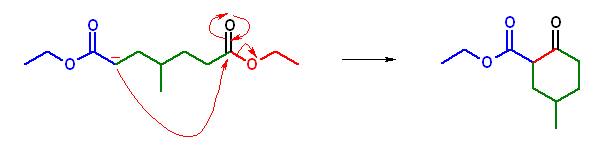
出発物質(diethyl 4-methylheptanedioate)の構造が2つのエステル基に関して対称なので、生成物は唯一種類である。
(注意)「問題の解き方」では、出発物質の命名に、diethyl 4-methylcycloheptanedioate としているが、当然、間違い。まあ、もしこの程度の間違いを間違いと気付かないようであれば、あなたはうっかりさんなのか勉強不足なのかどちらかでしょう。
23.15, 14
問い 23.14 も参照すること。
(解答例)
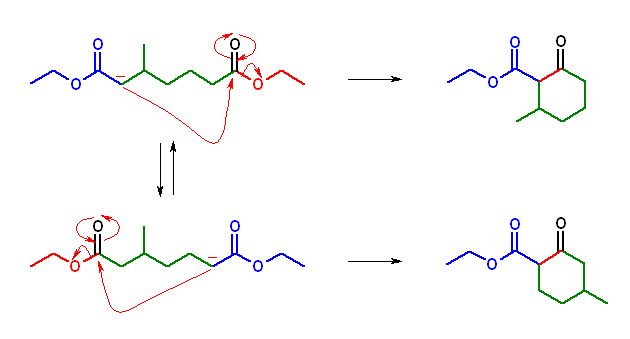
出発物質(diethyl 3-methylheptanedioate)の構造が2つのエステル基に関して非対称なので、いずれのエステル基の α 水素が引き抜かれるかによって2種類のエノラートが存在する。それぞれ、下図で表したように、一方からは、ethyl 2-methyl-6-oxocyclohexanecarboxylate を、もう一方からは、ethyl 4-methyl-2-oxocyclohexanecarboxylate を生じる。(これら2つは、メチル基の位置異性体である。)
23.16, 15
「α,β 不飽和受容体」(共役エノン)は、問い 23.03 の(発展)にも記したように、C=C 二重結合がカルボニル基(など)の影響で分極し、1,3-ジカルボニル化合物(活性メチレン化合物)より生じたエノラートを求核種とした付加反応(Michael 付加反応)を生じる。
(解答例)
2,4-pentanedione から生じるエノラートが求核種とし、選択肢に与えられたα,β 不飽和受容体に付加する。
(a) 3-(3-oxocyclohexyl)pentane-2,4-dione
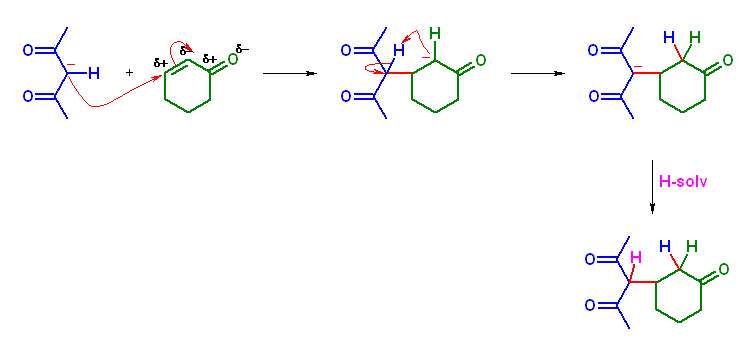
(b) 4-acetyl-5-oxohexanenitrile
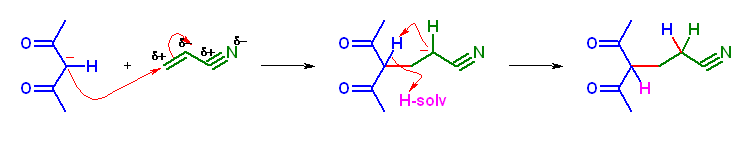
(c) ethyl 4-acetyl-3-methyl-5-oxohexanoate
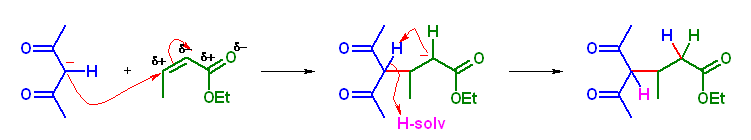
上の反応機構では、はじめに Michael 付加受容体のカルボニル基(など)の α 位に生じるカルバニオン(エノラート)が、分子内の、より酸性度の高い活性メチレン水素を引き抜くものとして反応機構を書いている。しかし、これは最終的に溶媒等より水素を引き抜いて中性の生成物を与えるまでそれぞれの水素が上記機構で書いたような位置に固定されていることを意味するのではない。
23.17, 16
問い 23.16 と同様に考えよ。
(解答例)
(a) diethyl 2-(3-oxobutyl)malonate, 系統名 diethyl 2-(3-oxobutyl)propanedioate
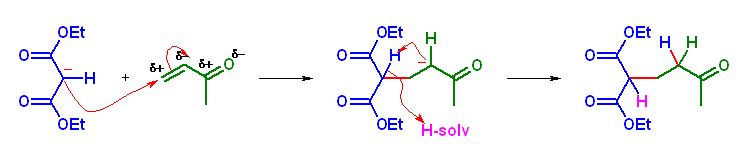
(b) ethyl 2-oxo-1-(3-oxobutyl)cyclopentanecarboxylate
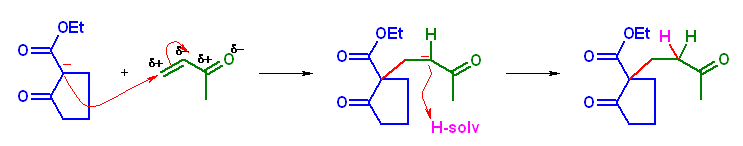
(c) 5-nitropentan-2-one
23.18,
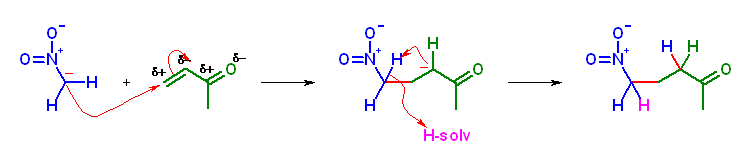
Nitro 基の α 位水素は酸性度が高いため、その共役塩基は、Michael 付加反応の求核種になる。では、Michael 付加の受容体はというと、カルボニル基に共役した二重結合で、その結合位置は β位になる。
(解答例)
nitroethane の共役塩基を求核種とし、pent-1-en-3-one を受容体とした Michael 付加反応により、6-nitroheptan-3-one を得ることができる。
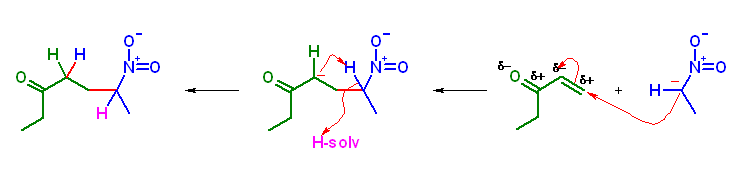
23.19, 17
図 23.8 を参照せよ。
(解答例)
(a) ethyl 3-(2-oxocyclopentyl)propanoate
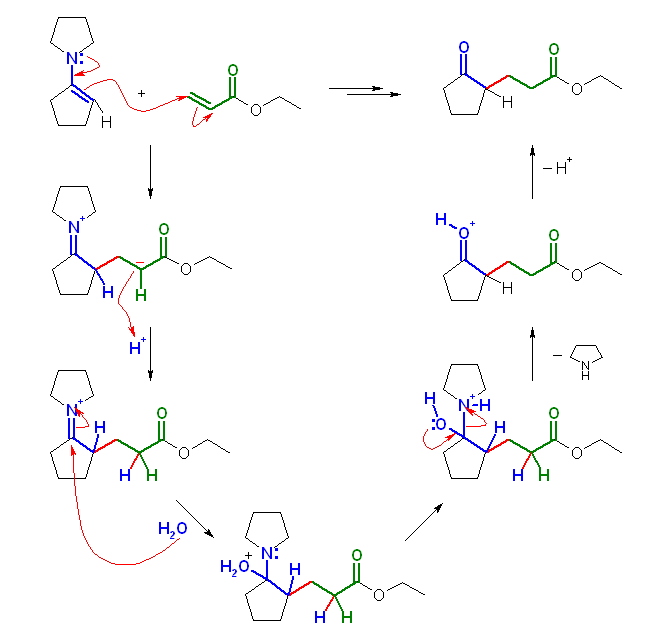
(b) 3-(2-oxocyclopentyl)propanal
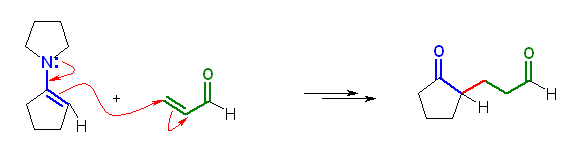
(c) 2-(1-methyl-3-oxobutyl)cyclopentanone
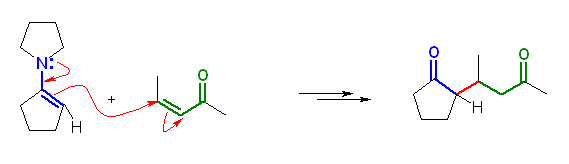
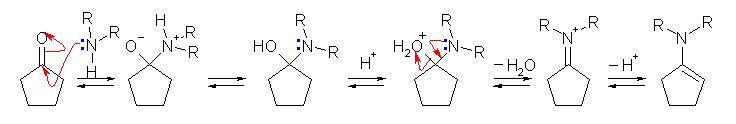
エナミンの生成の反応機構は、教科書 19.9 節を参照のこと。反応機構を再掲しておく。
23.20, 18
23.19 と同様に考える。
(解答例)
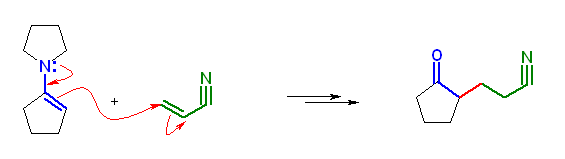
(a) cyclopentanone から生じさせたエナミンと acrylonitrile (系統名 prop-2-enenitrile ) の反応
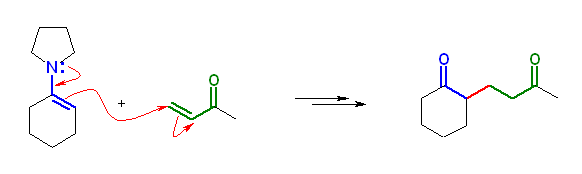
(b) cyclohexanone から生じさせたエナミンと but-3-en-2-one の反応
23.21-23.30
23.21, 19
β-ジケトンからのエノラートが求核種として Michael 付加するところから反応が始まる。
(解答例)
まず、 Michael 付加により 2-methyl-2-(3-oxobutyl)cyclopentane-1,3-dione を与える。
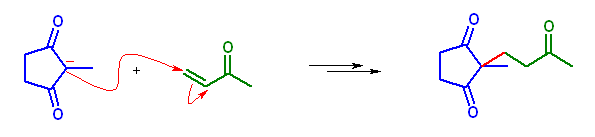
この Michael 付加体は、3種類の カルボニル α 水素を持つ。それぞれに形式的に可能な分子内 Aldol 縮合反応を書くと、次図のようになる。
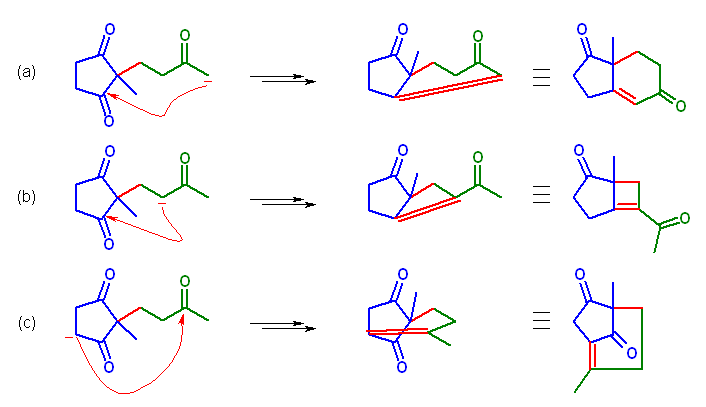
(a) では、6-methylbicyclo[4.3.0]non-1-ene-3,7-dione を与える。
(b) では、6-acetyl-1-methylbicyclo[3.2.0]hept-5-en-2-one を与える。
(c) では、2,5-dimethylbicyclo[3.2.1]oct-1-ene-6,8-dione を与える。
注意すべきことは、アルドール縮合は可逆な反応であるから、これらは互いに平衡下にある。したがって、これらのうち、最も安定な生成物が主生成物として生じることになる。
(b) の生成物は、cyclobutene 環の結合角歪みが大きいために、(a) より不安定であることが予測される。
(c) の生成物は、(a) の生成物と同様に、新しく生じた環は6員環である。しかし、次の3次元模型で確認できるように、次の2つの点より、(a) に比べて不安定である。
・bicyclo[3.2.1]octene 骨格は、環の歪みのため、炭素=炭素二重結合の周囲の立体が平面になれない。
・同様に環の歪みのため、カルボニルと炭素=炭素二重結合が同一平面内にない(そのため、共役にならない)。
したがって、得られるのは (a) で示した 6-methylbicyclo[4.3.0]non-1-ene-3,7-dione である。
(c) で得られる化合物 の3次元模型
23.22, 20
第1段階が Michael 付加で、第2段階がアルドール縮合である。アルドール縮合で生じた箇所は共役エノンの構造であることを考慮すると、Michael 付加体の構造が類推される。
(解答例)
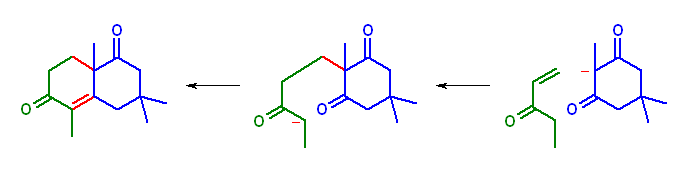
2,5,5-trimethylcyclohexane-1,3-dione から生じるエノラートを求核種として、pent-1-en-3-one に対して Michael 付加することにより、中間体(付加体)として、2,5,5-trimethyl-2-(3-oxopentyl)cyclohexane-1,3-dione を与える。更に分子内アルドール縮合によって、目的物である 1,4,4,7-tetramethylbicyclo[4,4,0]dec-6-ene-2,8-dione を与える。
1,4,4,7-tetramethylbicyclo[4,4,0]dec-6-ene-2,8-dione を、naphthalene を元にした付加命名法で命名すると、3,3,5,8a-tetramethyl-3,4,8,8a-tetrahydro-2H,7H-naphthalene-1,6-dione となる。
23.23, 21
エノンはアルドール縮合(「反応のまとめ」では、アルドール反応と、アルドール生成物の脱水に分けて書かれている)によって与えられる。
(解答例)
(a) pentan-3-one 同士のアルドール縮合
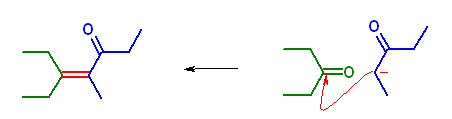
(b) 3-methylbutanal 同士のアルドール縮合
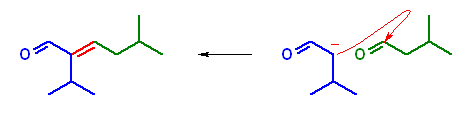
23.24, 22
問題文は、Claisen 縮合をさしている。なお、与えられた構造は「中間体である」と明記されていることから注意してみると、1つの酸素は結合が1本で、-1の形式電荷を持つ。
(解答例)
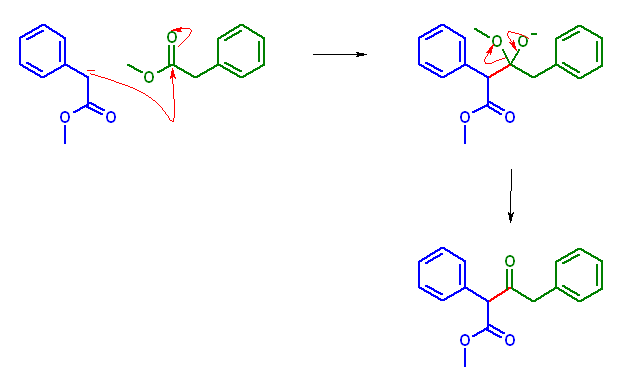
反応物は methyl phenylacetate
中間体(上図、右上)からの脱離基はメトキシドイオン CH3O-
生成物は methyl 3-oxo-2,4-diphenylbutanoate
23.25, 23
23.23 などと同じように考える。
(解答例)
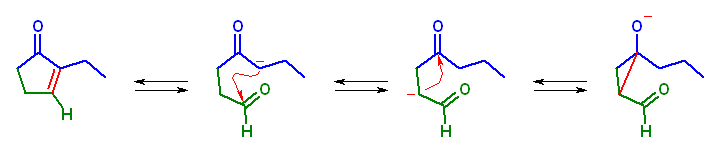
4-oxoheptanal の分子内アルドール反応。
アルドール反応(アルドール縮合)は、塩基触媒の存在下、平衡下にある。α 水素は2種類あるが、3員環を生成する反応は結合角の歪みが大きいため、上図、左のように5員環生成物 2-ethylcyclopent-2-en-1-one を与える。
23.26, 24
問い 23.22 と同様に考える。
(解答例)
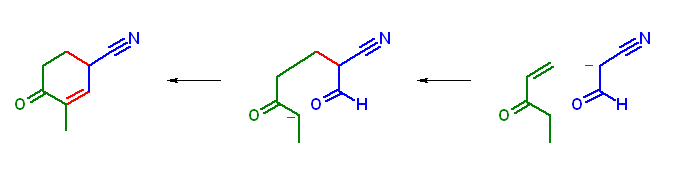
Michael 付加は、3-oxopropanenitrile より生じるエノラートを求核種とし、pent-1-en-3-one に対する付加が進行する。シアノ基は、カルボニル基と同様の効果を持つので、3-oxopropanenitrile は、β-ジケトン等と同様に酸性度が高い。
23.27, 25
アルドール反応には、酸性のカルボニル α 水素が引き抜かれてエノラートが生じる必要がある。また、このエノラートにより、カルボニル基が求核攻撃を受ける必要がある。
(解答例)
アルドール反応は、アルデヒドの場合は生成物に平衡が傾くが、ケトンでは出発物側に平衡が傾いている。しかし、その後の脱水までを含めたアルドール縮合では、ケトンでも十分に生成物側に平衡が傾く。したがって、問いの文が「アルドール縮合」と指定しているから、アルデヒド、ケトンの区別はここでは考えなくてもよい。
(a) trimethylacetaldehyde (系統名 2,2-dimethylpropanal)
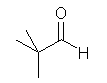
(c) benzophenone (系統名 1,1-diphenylmethanone)
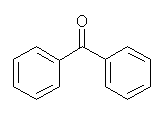
の2つは、カルボニル α 水素を持たない。そのため、アルドール反応しない。
(f) 3-phenylprop-2-enal
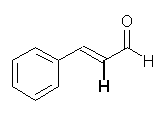
は、形式的にはカルボニル α 水素をもつものの、その水素がカルボニル基と共役した C=C 二重結合に結合した sp2 水素であるため、カルボニル基の π 系と直交しており、したがって安定なエノラートを生成しない。(酸性水素ではない。)そのため、アルドール反応しない。
(b) bicyclobutyliden-2-one (別名 2-cyclobutylidencyclobutanone ) を与える。
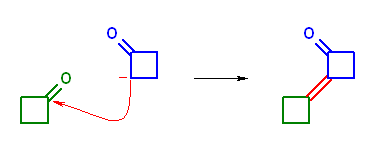
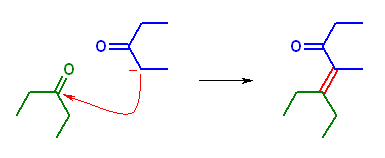
(d) 5-ethyl-4-methylhept-4-en-3-one を与える。
(e) 2-octyldodec-2-enal を与える。
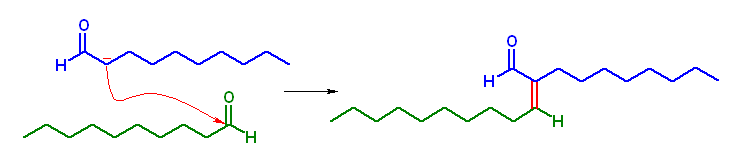
23.28, 26
(a) は異なる2分子からの交差アルドールで、(b), (c) は分子内のアルドールで得られる。(d) はアルドール縮合によって生成することが可能なところが2箇所あることに注意。
(解答例)
(a) benzaldehyde と acetophenone を反応させる。
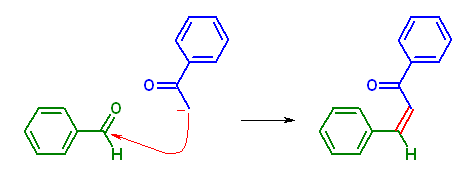
アルデヒドの方がケトンより求核攻撃を受けやすい。benzaldehyde は α 水素を持たないから、交差アルドール反応により生じる上記生成物 (1,3-diphenylprop-2-en-1-one) が主となると考えられる。
(b) 5-oxohexanal を分子内で反応させる。
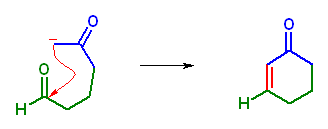
カルボニル α 水素は、上図以外に2箇所あるが、これらはいずれも分子内アルドール縮合(塩基触媒下、可逆)により結合角歪みの大きな4員環の構造を与えるから、平衡の結果、最も安定な上記生成物 (cyclohex-2-en-1-one) が得られる。
(c) [2-(2-oxoethyl)phenyl]acetaldehyde (別名 o-phenylenebis(acetaldehyde))を反応させる。
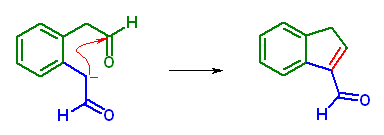
生成物は、3H-indene-1-carbaldehyde である。
(d) 1,3-diphenylpropan-2-one から生じるエノラートを求核種とし、1,2-diphenylethane-1,2-dione (慣用名 benzil )に対して反応させる。
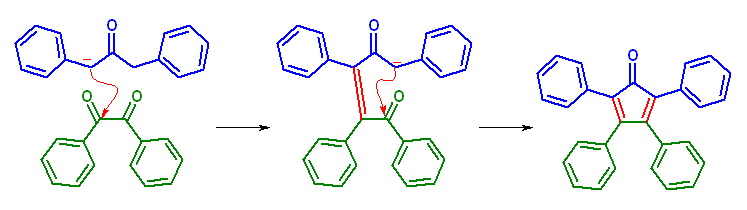
23.29, 27
2つのアルデヒド基に対して対称な構造なので、生成物は1種類のみを考えればよい。
(解答例)
アルデヒドなので、アルドール反応の平衡の結果、十分な量のアルドール型の環化生成物が得られる。更に加熱等により脱水して(アルドール縮合)エノンにしてもよい。
分子内のアルドール縮合により、 cyclopent-1-enecarbaldehyde が得られる。
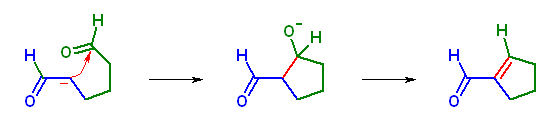
23.30, 28
カルボニル α 水素が複数種類あることに注意して考えること。
アルドール縮合反応は、塩基触媒の存在下、可逆となるから、生じる生成物が複数ある場合には、それらの間での平衡が成り立つ。その結果、より安定な生成物の方が多く生じる。安定性に極端に差がない場合には、両方の生成物が(異なる比で、ではあるが)生成することになる。
(解答例)
4種類のカルボニル α 水素に由来したエノラートが存在しており、それぞれがカルボニル基に対する分子内の求核攻撃をすることが可能である。(下図)
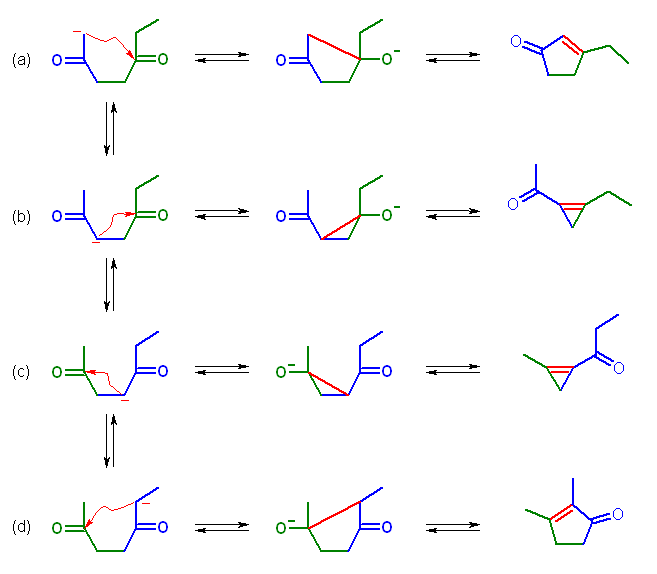
エノラート (b) および (c) から、アルドール縮合で生じる化合物は、結合角歪みの大きな3員環を持つため、不安定であると考えられるから、主な生成物ではない。
エノラート (a) および (d) について着目すると、カルバニオンは級数の小さい方が安定であることを考慮すると、(a) の方が安定である。
しかし、生成物の構造から考えると、(a) より生じるエノンに比べ、 (d) より生じるエノンの方が安定である。 これは、エノンのアルケンに着目したとき、アルケンの周囲のアルキル基の数は、3-ethylcyclopent-2-en-1-one では3置換、2,3-dimethylcyclopent-2-en-1-one では4置換だからである。
完全に生成物の間に平衡が成立する系であるから、途中の中間体のエノラートの安定性よりも生成物の安定性が生成物の量比を決定すると考えられるから、エノラート (d) より生じる 2,3-dimethylcyclopent-2-en-1-one が主生成物、エノラート (a) より生じる 3-ethylcyclopent-2-en-1-one が副生成物となると予想される。
問い 23.31 の文章に示された、主生成物の 1H-NMR スペクトルについての情報も、2本のメチル基の存在を示唆しており、上の構造からの予測と一致している。
23.31-23.40
23.31, 29
特にヒントは無い。
(解答例)
この 1H-NMR スペクトルに関する記述は、
・若干環境が異なるメチル基が2本あり、他の水素とスピン結合していない。
・アルケンに結合した水素(ビニルプロトン)が存在しない。
ことを意味する。したがって、主生成物は、 2,3-dimethylcyclopent-2-en-1-one である。(問い 23.30 の解答例を参照)
23.32, 30
問い 23.30 の解答例の解説を参照のこと。
(解答例)
塩基触媒の存在下、アルドール縮合は可逆であるから、アルドール縮合生成物はエノラートを再生(逆アルドール反応)する過程がある。(問い 23.03 の「発展」の項等も参照のこと)
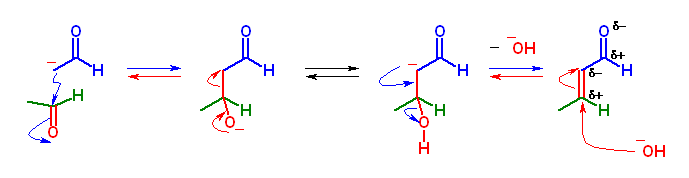
そのため、もとのカルボニル化合物より可能であるアルドール縮合生成物は、互いに平衡になる。平衡下の生成物の安定性が生成物の量比を決定するから、3-ethylcyclopent-2-en-1-one は、2,3-dimethylcyclopent-2-en-1-one との間に平衡となるが、その平衡は 2,3-dimethylcyclopent-2-en-1-one 側に傾く。
23.33, 31
アルドール反応は、カルボニル化合物に対する求核付加反応であるから、エステルの加水分解の機構が、塩基性と酸性条件下でどのように描かれたのかを思い出してみるとよいだろう。
なお、酸性条件下での反応機構を書く場合には、-OH や、カルバニオンのようなイオン種は介在させてはならない。
(解答例)
酸性条件下では、
求核攻撃を受けるのは、プロトン化されたカルボニル基。プロトン(ルイス酸)の配位により、カルボニル基の分極が増すため、弱い求核種でも攻撃できるようになる。
求核種は、酸性条件下、平衡で存在しているエノール。
上段は塩基触媒、下段に酸触媒の反応機構をまとめた。
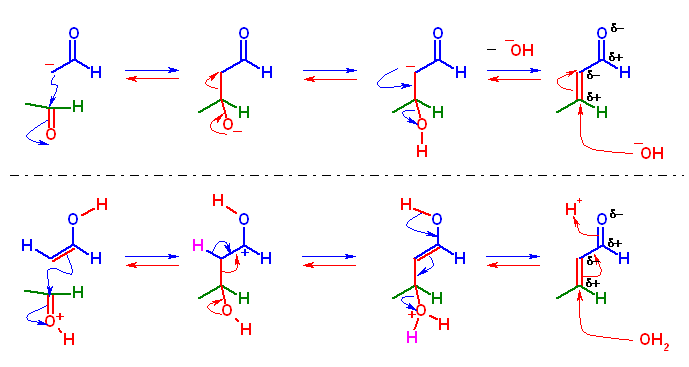
上下、それぞれの対応を確認しておくこと。
23.34, 32
教科書 23.2 節、教科書 23.4 節を参照すること。
(解答例)
2,2,6-trimethylcyclohexanone は、α 水素を1つしか持たないので、アルドール反応によりアルドールを与えるが、その後に脱水して共役エノンを与えることができない。
アルデヒドの場合は、アルドールを収率よく与えることができるが、ケトンの場合はこの平衡は出発物質よりに偏っており、その後の脱水で共役エノンを生じて、始めて平衡が生成物側に傾く。したがって、ケトンであり脱水の不可能な 2,2,6-trimethylcyclohexanone では、アルドール生成物を単離することができない。
23.35, 33
シンナムアルデヒド cinnamaldehyde の系統名は、3-Phenyl-propenal である。構造を書き、どの位置がアルドール反応で生じているのかを見出すこと。
(解答例)
benzaldehyde と acetaldehyde の交差アルドール縮合を用いる。
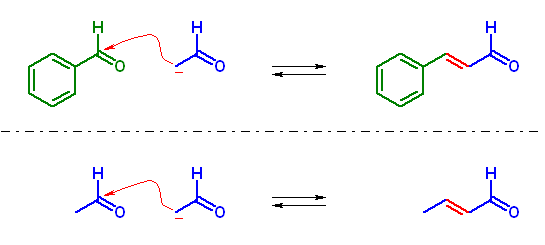
benzaldehyde は、α 水素を持たないため、反応系中にあるエノラートは acetaldehyde 由来のもののみである。上記図の下段のような、acetaldehyde の自己縮合反応も生じる可能性がある。塩基性触媒存在下、反応は可逆であるので、すべてのアルドール縮合生成物は互いに変換可能な平衡下にあり、反応生成物の安定性でその量比が決まる。cinnamaldehyde は、単なる共役エノンより、更にフェニル基とも共役しているため、より安定性の高い生成物であると考えられるから、交差アルドール縮合反応が優先的に起きる可能性がある。
問題文の「ケイ皮」は、漢字で書くと「桂皮」。漢方の関連で「クスノキ科の常緑高木、ケイの樹皮を桂皮という」とあるが、肉桂(ニッケイ、ニッキ)の樹皮をはがし、乾燥させ、粉末にしたスパイスがシナモンパウダー。つまり、シンナムアルデヒド(対応するカルボン酸は、シンナミックアシッド)は、シナモンと共通の語幹である。
23.36, 34
問い 23.27 (f) などを参照すること。
(解答例)
2つある α 水素は、いずれもカルボニル基の π 系とは直交しており、安定なエノラートを生じないため、アルドール反応における求核種となることができない。
23.37, 35
(a) のみ、Claisen 縮合、他は、アルドール縮合。
(解答例)
(a) ethyl 2-ethyl-3-oxohexanoate が得られる。
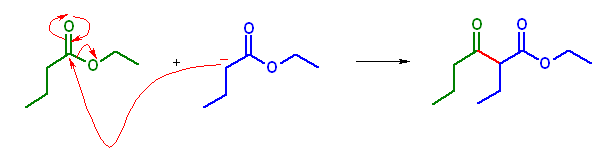
(b) bicycloheptyliden-2-one (別名 2-cycloheptylidenecycloheptanone)が得られる。
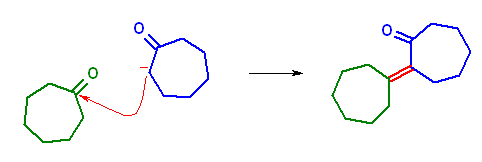
(c) 主生成物として、3-ethyl-2-methylcyclohex-2-enone が得られる。異なる位置の α 水素が抜けて生じたエノラートからは、ピンクの矢印のような求核攻撃により、1-(2-ethylcyclobut-1-enyl)propan-1-one を生じるが、これら2つの生成物は(逆アルドールを経由した)平衡下にあるため、結合角歪みの大きい後者は主には生じない。
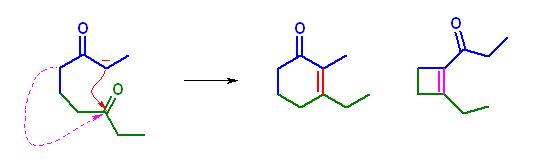
(d) 2-benzyl-5-phenylpent-2-enalが得られる。
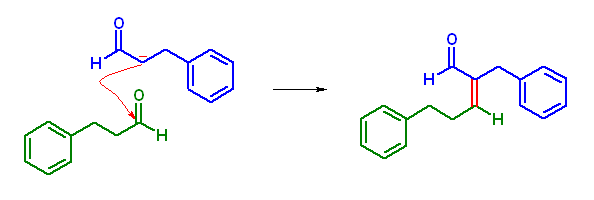
23.38, 36
交差 Claisen 反応では、目的の交差生成物以外の生成物があり得る。この目的外のものをどのように抑えるのかが、実質上の反応の工夫で必要な点である。
(解答例)
シクロペンタノンに塩基を加えてエノラートを生じさせたときに、周囲にギ酸エステルがないと、(ギ酸エステルを系に混合する前に、はじめからある程度高濃度で存在している)別のシクロペンタノン分子との反応が競争してしまうため。
ギ酸エステルは、カルボニル α 水素を持たないため、塩基と混合してもエノラートを生じない。そのため、交差 Claisen 反応において有用な求核攻撃の受容分子として用いられる。すなわち、ギ酸エステルは、どの段階で系中に加えても、ギ酸エステルのエノラートに由来するような副生成物を考える必要はない。
23.39, 37
Claisen 縮合だから、エステルが求核攻撃をうけたあと脱離基が脱離する(すなわち、カルボニル求核置換反応の形式になる)。そのような組み合わせを考える。交差 Claisen の条件では、自己縮合体、交差生成物とも考えなければならない。
なお、Claisen 縮合も、アルドール縮合等と同様に可逆である。
なお、「問題の解き方」(第6版、第7版とも。確認はしていませんが、おそらく第5版も。)の、23.39(d) について書かれた解説に関連して、重要なコメントがあります。(以下の解答例中に示しました。)「問題の解き方」を参考にしている人は、必ず、一読しておいてください。
(解答例)
Claisen 縮合も、アルドール縮合等と同様に可逆であるから、複数の構造の生成物が書ける場合、それらは逆Claisen反応を経由して互いに変換可能で、平衡下にある。したがって、安定性によって生成物の量比が決定される。ただし、塩基性の条件下である場合には、その生成物は(以下、図では中性の分子を示しているが) β-ケトエステルの活性メチレンの位置で酸性水素が引き抜かれたエノラートである。エノラートが安定であるということは、エノラートの共役酸(中性分子、β-ケトエステル)の酸性度が高い(より小さな pKa をもつ)ということと等価である。
(a) 両エステルとも α 水素を持つ。したがって、2×2=4通りの生成物がある。
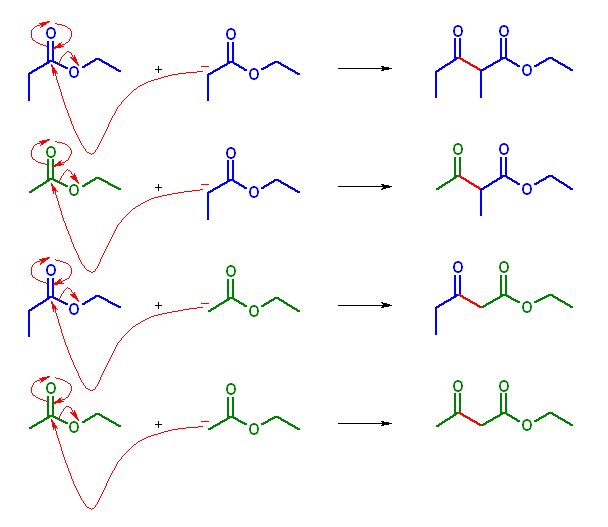
生成物は、上より
ethyl 2-methyl-3-oxopentanoate
ethyl 2-methyl-3-oxobutanoate
ethyl 3-oxopentanoate
ethyl 3-oxobutanoate
これら4種の生成物は、ほぼ等しい酸性度を持つと考えられるから、いずれもほぼ等量ずつ生じると予測される。
(b) 安息香酸エステルは α 水素を持たないから、求核種はフェニル酢酸のエステルから生じるエノラートに限定され、したがって、2通りの生成物が考えられる。
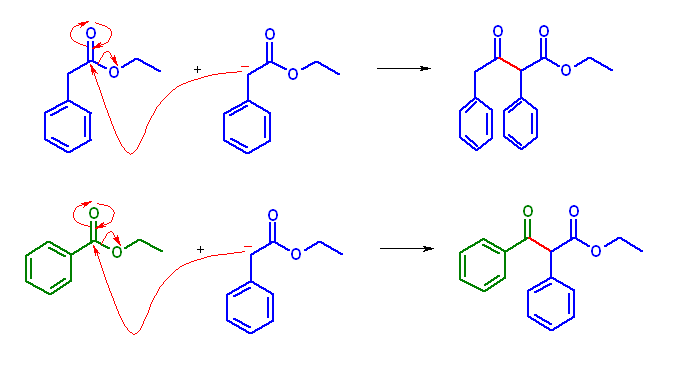
生成物は、上より
ethyl 3-oxo-2,4-diphenylbutanoate
ethyl 3-oxo-2,3-diphenylpropanoate
これら2つの生成物は、交差 Claisen 生成物の方が、カルボニル基にフェニル基が共役している分、わずかに安定であると考えられ、主生成物となると予測される。
(c) 炭酸エステルは α 水素を持たないから、シクロヘキサノンから生じるエノラートに限定される。シクロヘキサノンはエステルではないから、Claisen 縮合生成物は与えない。
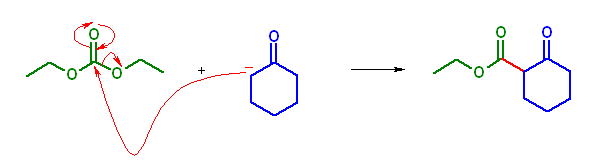
生成物は、ethyl 2-oxocyclohexanecarboxylate である。
なお、アルドールより脱水までが生じるような条件では、シクロヘキサノン同士の縮合生成物が生じる可能性もある。アルドールからの脱水が進行しないような条件では、ケトン同士のアルドール付加体は平衡位置の関係より、ほとんど生じない。
(d) 酢酸エステルは、α 水素を持ち、同時に Claisen 反応の求核種の受容体として働く。そのため、次図のように、自己縮合する。一方、ベンズアルデヒドは、α 水素を持たないため、エノラート(求核種)を生じない。また、エステルではないから、Claisen 縮合生成物は与えない。
一般に、ともに α 水素を持つエステルとアルデヒドとで比較すると、アルデヒドの α 水素の方が酸性度が高い(教科書 p872、表22.1)ので、両者を混合した場合に、エステル由来のエノラートが反応に関与することは考えなくて良いのであるが、このケースでは、アルデヒドが α 水素を持たないことから、エステル由来のエノラートが反応に関与する。
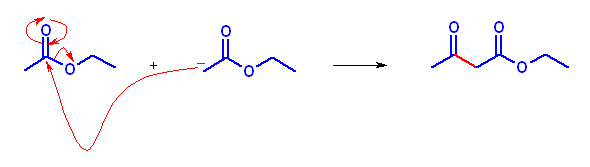
生成物は、ethyl 3-oxobutanoate である。
(c) と同様にアルドール反応を考える場合、ベンズアルデヒドは、α 水素を持たないため自己縮合した生成物は与えない。そのため、酢酸エステル由来のエノラートが求核種として働いて、次のような交差アルドール反応を生じると予測される。しかし、上のような Claisen 縮合と競争して生じることが可能かどうかについては、現時点で、判断の材料が無いように思われる。
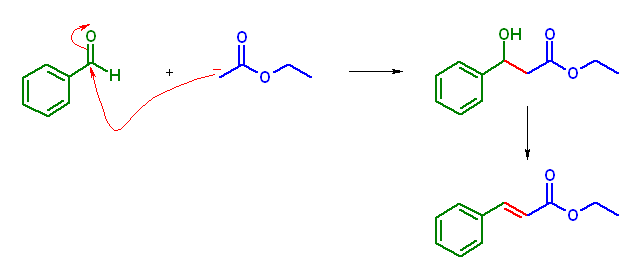
「問題の解き方」に示された問 23.39(d) の解答例について
解答例では、酢酸エステルの自己 Claisen 縮合による ethyl 3-oxobutanoate および、脱離する EtOH の他、主生成物に、「交差 Claisen 縮合生成物」として、次図の ethyl 3-oxo-3-phenylpropanoate を生じると示している。
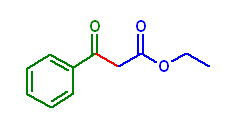
反応機構上、アルデヒドのカルボニル基に求核攻撃が起きた後、ヒドリド H- の脱離が生じない限り、このような「交差 Claisen 縮合生成物」は、生じることができない。「アルデヒドのカルボニル基に求核攻撃が起きた後のヒドリド H- の脱離」は、カニッツァロ反応のように特殊な場合においてのみ、例外的に生じる。これは、近傍に強いヒドリド受容体(カニッツァロ反応の場合は、別のアルデヒド分子)がある場合に限られる。
カニッツァロ反応(α 水素を持たないアルデヒドを強塩基と加熱、など)の反応機構を示しておく。
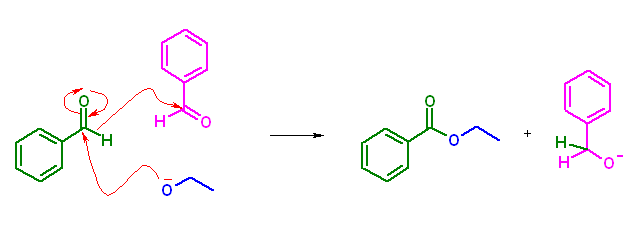
形式上は、絶対に無いとは言い切れないが、もしこれを想定しているのなら、縮合生成物以外の副生成物として、 EtOH 以外に、ベンジルアルコール PhCH2OH も挙げていなければ整合性が取れない。
よって、この解答例は本来の想定されたものというより、出題ミス(または、解答ミス)に類するものと思う。「問題の解き方」に与えられた解答を満たすようにするためには、「benzaldehyde と ethyl acetate」を「ethyl benzoate と ethyl acetate」に変えてやらなければならない。
23.40, 38
β-ケトエステルは、Claisen 縮合によって得ることができた。この Claisen 縮合は、塩基触媒存在下、可逆である。
(解答例)
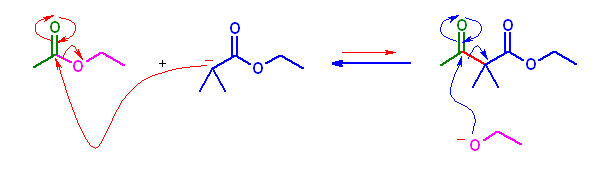
ethyl 2,2-dimethyl-3-oxobutanate (教科書では、ジメチルアセト酢酸エチル)は、次図のように、ethyl 2-methylpropanoate からのエノラートが ethyl acetate に求核攻撃して生じる交差 Claisen 縮合体である。この、3位のカルボニル基にエトキシドイオンが求核的に攻撃すると、カルボニル求核置換反応の形式によりエノラートが脱離する(逆 Claisen反応、次図中、青の曲がった矢印で示した。)。
23.41-23.50
23.41, 39
教科書 23.8 節を参考に、Claisen 縮合の反応の平衡が、生成物側に傾く理由についてもういちど整理してみよう。
(解答例)
ethyl 3-oxobutanate (アセト酢酸エチル)は、次図のように、ethyl acetate からのエノラートが、もう一分子の ethyl acetate に求核攻撃して生じる Claisen 縮合体である。問い 23.40 と同様に、3位のカルボニル基にエトキシドイオンが求核的に攻撃すると、カルボニル求核置換反応の形式によりエノラートが脱離する(逆 Claisen反応)ことが可能である。
しかし、ethyl 3-oxobutanate は β-ケトエステルであることから酸性度の高い水素を持っている。この活性メチレンの pKa は、表 22.1 を参照すると、約 11 であり、エタノール(pKa は約16)よりずっと強い酸である。酸-塩基反応では、より強い酸が塩を形成し、より弱い酸(この系ではエタノール)が遊離するから、ethyl 3-oxobutanate は、エトキシドイオンと速やかに反応し、エノラートと遊離のエタノールを生成することが分かる。
そのため、23.40 のケースと比較して、(Claisen縮合体が酸性水素を持つことにより、エノラートを形成してしまうので)逆Claisen反応が進行しにくくなっているものと予測される。
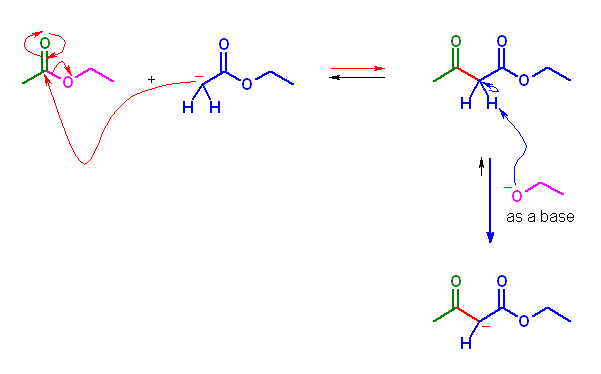
上の機構図、右列に描かれた酸-塩基平衡は、塩基性条件下では下向きに傾く。このことが、Claisen 縮合の全体としての平衡が生成物よりに傾くことの理由になっている。(教科書 23.8 節を参照。)
ところで、平衡下の物質間の量比はボルツマン分布に従うので、量比 NB/NA = exp(-ΔE/RT ) と表される。この式から明らかなように、2つの状態の間のエネルギー差 ΔE が同じであれば、温度が低いほど量比は開き、温度の高い極限では、エネルギー差 ΔE にかかわりなく両状態の存在量が等しくなる。すなわち、上の機構図において、温度が高いほうが(同じ塩基性の条件下であっても)エノラートを形成していない(したがって、3位のカルボニル基にエトキシドイオンが求核的に攻撃して2分子の Ethyl acetate を生じうるような )形態の ethyl 3-oxobutanate (アセト酢酸エチル)の分子の割合が多くなると考えられる。
23.42, 40
Michael 付加は、教科書 23.11 節を参照すること。
基本は活性メチレン化合物が共役エノンに付加するから、R-CH2CH2C(=O)-R' のユニットに着目すると、どの位置で Michael 付加が生じているのかが判断できる。
ただし、(b) は、(a), (c),(e) のような形に帰着するための工夫が必要となる。
ニトロ基は、その α 位での酸性度が高く Michael 付加の求核種にもなるが、ニトロアルケンは、求電子的 Michael 付加受容体となる。したがって、(d) ~ (f) は、それぞれ、2通りに書くことができる。
(解答例)
解答例の反応機構では、Michael付加の求核種を青で、求電子性 Michael 付加受容体を緑で示した。なお、求核種は「求核性供与体」として名称を示した分子のエノラートである。
(a) 生成物: ethyl 2-acetyl-5-oxo-5-phenyl-pentanoate
求核性供与体: ethyl 3-oxo-butanoate
求電子性受容体: 1-phenylprop-2-en-1-one
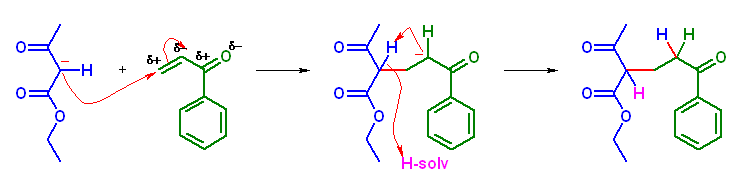
(b) 生成物: heptane-2,6-dione
脱炭酸前 Michael 付加生成物: ethyl 2-acetyl-5-oxohexanoate
求核性供与体: ethyl 3-oxobutanoate
求電子性受容体: but-3-en-2-one
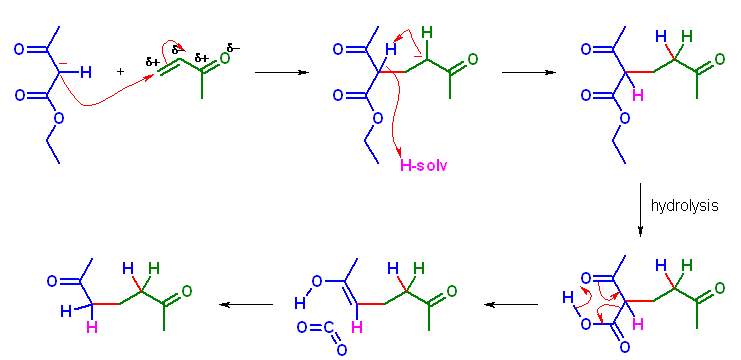
(c) 生成物: diethyl 2-(2-cyanoethyl)malonate (系統名: diethyl 2-(2-cyanoethyl)propanedioate )
求核性供与体:diethyl malonate (系統名: diethyl propanedioate )
求電子性受容体:acrylonitrile (系統名: prop-2-enenitrile )
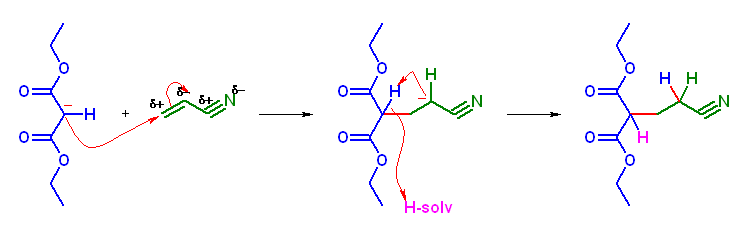
(d) 生成物: ethyl 4-nitropentanoate
脱炭酸前 Michael 付加生成物: diethyl 2-(2-nitropropyl)malonate (系統名: diethyl 2-(2-nitropropyl)propanedioate )
求核性供与体: diethyl malonate (系統名: diethyl propanedioate )
求電子性受容体:2-nitropropene
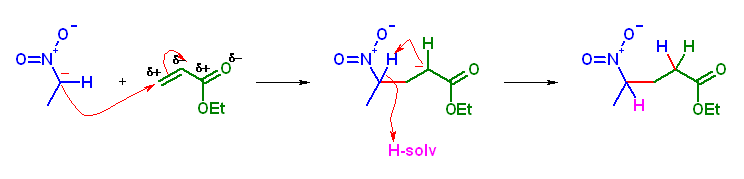
生成物: ethyl 4-nitropentanoate
求核性供与体: nitroethane
求電子性受容体: ethyl acrylate (系統名: ethyl prop-2-enoate )
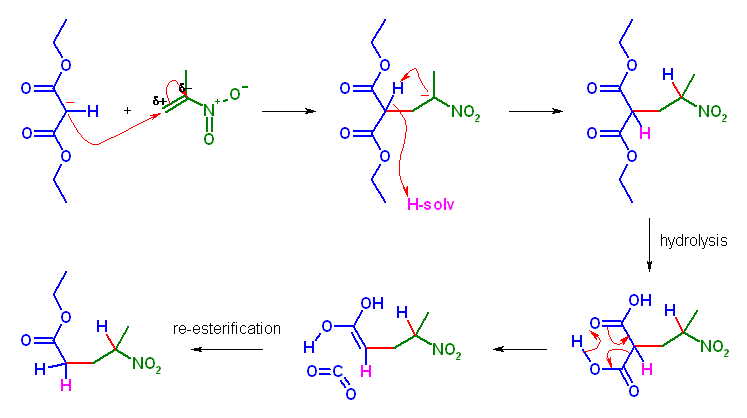
(e) 生成物: diethyl 2-(2-nitroethyl)malonate (系統名: diethyl 2-(2-nitroethyl)propanedioate )
求核性供与体: nitromethane
求電子性受容体: diethyl 2-methylenemalonate (系統名: diethyl 2-methylidenepropanedioate
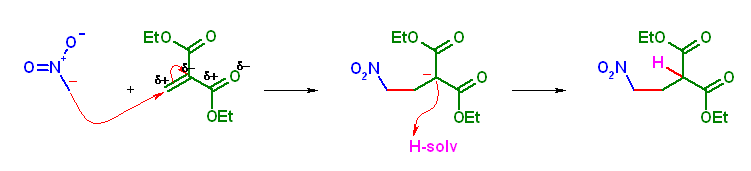
生成物: diethyl 2-(2-nitroethyl)malonate (系統名: diethyl 2-(2-nitroethyl)propanedioate )
求核性供与体: diethyl malonate (系統名: diethyl propanedioate )
求電子性受容体: nitroethene
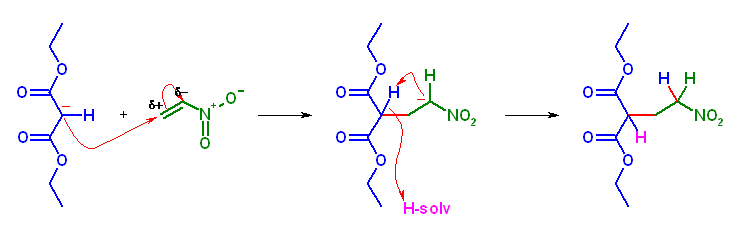
(f) 生成物: 3-(nitromethyl)cyclohexanone
求核性供与体: nitromethane
求電子性受容体: cyclohex-2-enone
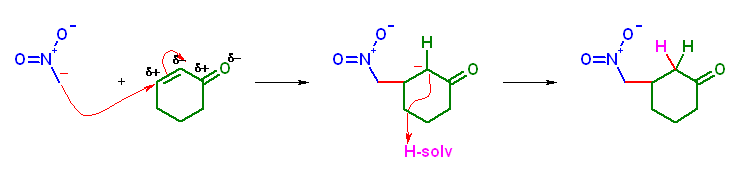
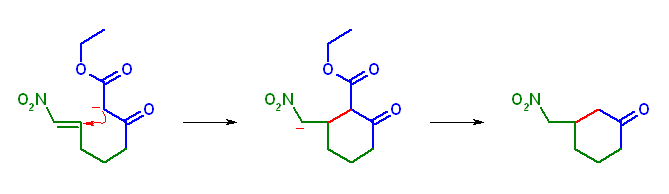
生成物: 3-(nitromethyl)cyclohexanone
脱炭酸前 Michael 付加生成物: ethyl 2-nitromethyl-6-oxocyclohexanecarboxylate
出発物(分子内反応): ethyl 8-nitro-3-oxooct-7-enoate
23.43, 41
Robinson 環化、教科書 23.13 節を参照のこと。また、問い 23.22 も参照すること。
(解答例)
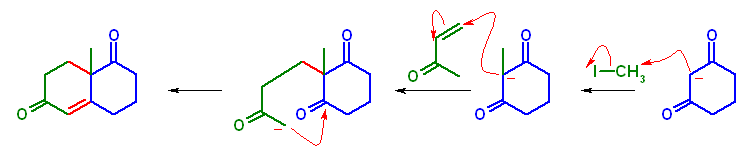
1) 1,3-cyclohexanedione の活性メチレンの位置で、まずモノメチル化する。反応条件は、NaOEt, then CH3I
2) 再度、塩基を加えてエノラートとしたのち、but-3-en-2-one に対するMichael 付加を行う。
3) 最後に、分子内 aldol 縮合させることにより、目的の Wieland-Miescher ケトンを与える。
23.44, 42
描かれている反応が、どういう反応なのかをアサインし、本来はどうなるべきなのかを考えること。
(解答例)
1. そもそも反応が進行しない/しにくい。
2. 反応は進行するけれど、単一生成物を与えない。
などが、目的の物質が高収率では得られない主な理由として考えられる。
(a)
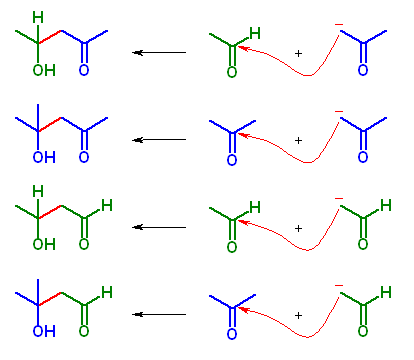
アセトンとアセトアルデヒドの交差アルドール反応を用いているので、生成物は複数(アセトン、アセトアルデヒトの両方ともが α 水素を持つので、原理的には2×2=4通り)あり、それらの間が平衡となるため、特定の交差生成物のみを主生成物として得ることは難しいと予測される。目的としているのは、アセトンからのエノラートがアセトアルデヒドに求核攻撃して生じるアルドール。
教科書 p897 の記述によると、アルドール付加体の安定性は、立体的要因で変化するとされている。また、一般に、アルデヒドのアルドールは生成物側に有利であるが、ケトンのアルドールは生成物側に不利である。
(b)
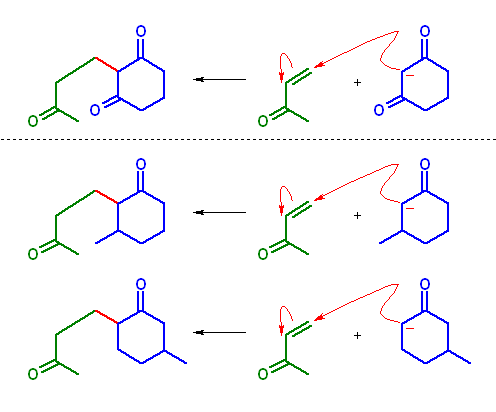
Michael 付加における求核種は、上図、破線より上のように、より安定な 1,3-ジカルボニル化合物からのエノラートを用いるのが一般的である。破線より下に示したような、モノケトンからのエノラートでは、Michael 付加生成物の収率が低いらしい。
また、この反応が進行するにしても、シクロヘキサノンの3位にあるメチル基※がカルボニル基 α 位を非等価にしているから、2種類のエノラートが考えられ、したがって、生成物が混合物になると考えられる。
(c)
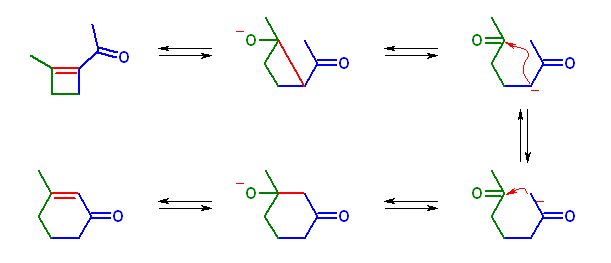
カルボニル基の内側と外側に2種類の α 水素があるから、原理的に2種類のアルドール縮合生成物が考えられる。塩基触媒の存在下に逆アルドール反応が進行するから、これらの生成物の間には平衡が存在する。ここでは、4員環生成物を目的としているが、結合角の歪みがあるために相対的に不安定であり、より安定な6員環生成物を主生成物として与える。問い 23.30 の解説も参照すること。
※註: 同様に2種類ある 2-methylcyclohexanone からのエノラートは、熱力学支配と速度論支配を使いわけることによって、反応条件により生成しわけることが可能である。
以下の外部リンク先によると、LDA, -78℃ では、反応速度論支配となり、立体的にすいている方の(6位の) α 水素が引き抜かれてエノラートを生じる。これに対し、Ph3CLi を塩基として用い、加熱条件下ではより安定なエノラート(アルケン部分が多置換であるように)を生成するために2位の α 水素が引き抜かれてエノラートを生じる。
(外部リンク http://www.chem-station.com/odoos/data/on-ol-6.htm )
その他、アルドール反応の機構や、位置、立体の制御に関しては膨大な知見の蓄積がある。
23.45, 43
以下を参考に、試薬等の条件を調べること。
a),b) 二重結合は、アルコールからの脱水で生じることができる。
c) 酸化開裂により、カルボン酸を与え、
d) エステル化する。
e),f) 分子内の Claisen 反応(Dieckmann 環化)
g),h) β-ケトエステルのアルキル化と脱炭酸
(解答例)
a) 1) LiAlH4 or NaBH4,
2) H3O+
b) POCl3, pyridine
c),d) 1) OsO4,
2) HIO4,
3) CrO3, H3O+,
4) SOCl2,
5) EtOH
e) NaOEt/EtOH
f) H3O+
g) 1) NaOEt/EtOH,
2) CH3Br
h) 1) NaOH-H2O,
2) H3O+, heat
(解説) c,d) のところが標準的な解答より少し遠回りしているかもしれない。標準的には、KMnO4-H3O+, then EtOH, H+ といったところか。
上のように遠回りをしたのは、過マンガン酸カリウムやオゾンを用いた直接酸化だと分解反応まで生じてしまい、収率が下がるからである。四酸化オスミウムで 1,2-ジオール化合物とし、過ヨウ素酸で酸化開裂する。得られるアルデヒドを酸性クロム酸でカルボン酸まで酸化したあと、エステル化する。ここでは、あえて、Fischer のエステル化合成の条件とせず、塩化チオニルによって酸塩化物としたのち、エタノールと反応させるように書いた。
23.46, 44
ノーヒント。
(解答例)
(a) 2,6-dibenzylidenecyclohexanone
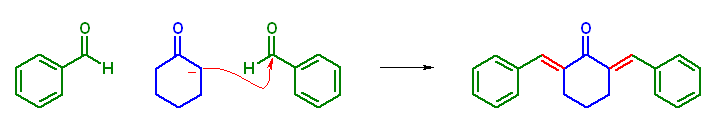
cyclohexanone と、2分子の benzaldehyde で、アルドール縮合させる。benzaldehyde は、α 水素を持たないから目的の構造の分子が主に生成する。
(b) 3-(2-oxocyclohexyl)propanenitrile
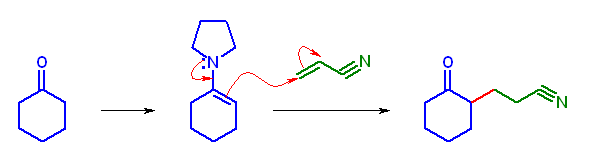
acrylonitrile に対しての Michael 付加を行う。Michael 付加は、モノケトンのエノラートでは十分に反応しないので、pyrrolidine などを用いてエナミンとしてから反応させる。
(c) 2-allylcyclohexanone
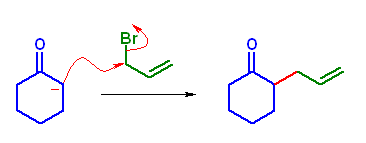
allylbromide (系統名 3-bromopropene) に対して、エノラートを求核種として、SN2 反応させる。
23.47, 45
(a) ホルムアルデヒド CH2O は、α 水素を持たない。
(b) Michael 付加は、α,β-不飽和化合物に対して、安定なエノラートよりの求核攻撃で生じる。
(解答例)
(a) ethyl 2-methylidene-3-oxo-butanoate
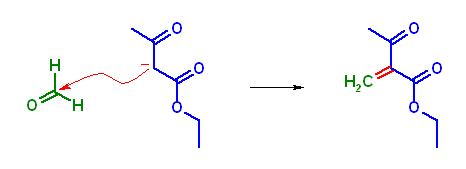
ホルムアルデヒドは、カルボニル炭素の廻りの立体障害もなく、また、電子的にも π 系に対する電子供与基(アルキル基)を一切持たないことの2つの影響により、最も求核攻撃を受けやすい分子のひとつである。
(b) diethyl 2,4-diacetylpentanedioate
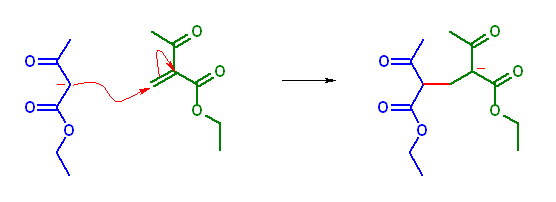
23.48, 46
どうでも良いですが、問い 23.47 と分離して別の問題にする意味があるんですかねえ。
(解答例)
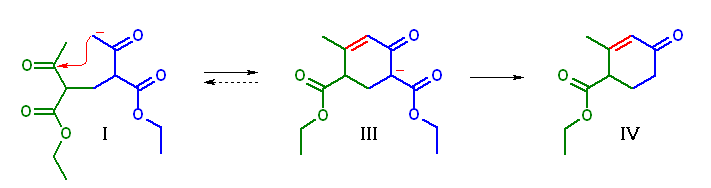
I は、diethyl 2,4-diacetylpentanedioate から生じるエノラートのうちの1つ。「置換シクロヘキセノン」を生じる反応とすると、上図に示したアルドール縮合となる。
III を加水分解、脱炭酸することにより、Hagemann のエステル IV を得ることができる。
解答としては、上記の通りで十分とは思うが、I の構造をよく見ると、アルドール反応以外に、Claisen 縮合も可能である。また、そもそも、β-ケトエステルの構造を持つので、diethyl 2,4-diacetylpentanedioate の中の最も酸性の高い水素は、I で示したアニオンの位置とは異なっている。
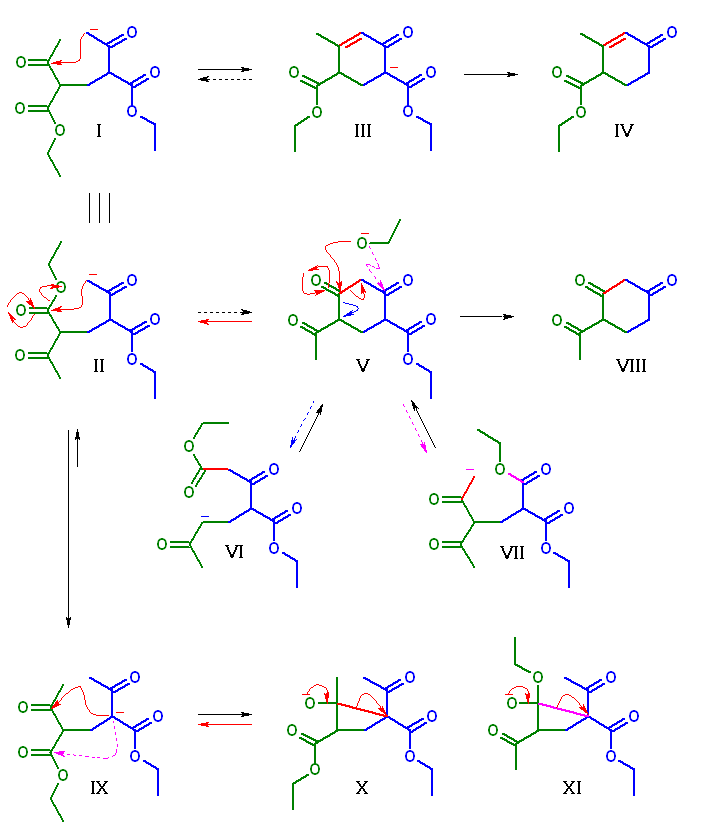
I と II は同じものを書き直したもの。I に書かれた曲がった矢印では、Aldol 縮合により III を与えるが、II に書かれた曲がった矢印では Claisen 縮合により V を与える。
III は、アルドール縮合の結果として生じるエノン構造を持つ生成物(アルドールに比べてエノンは共役が広がることからより安定となるため、アルドール反応では生成物に不利な反応基質でも、その後の脱水により生成物に有利となったことを思い出すこと。)であり、また、同時に β-ケトエステルでもある。(そのため、塩基性の溶液中では酸性水素が引き抜かれ、エノラートとなっている。Claisen 縮合も、平衡ではあるが、β-ケトエステルの酸性水素が引き抜かれることで平衡が生成物側に偏ったことを思い出すこと。問い 23.41 の解説も参照。)III, V は逆アルドール反応、逆Claisen反応によって平衡下にあると考えられるが、上記のような理由により、III が優先して生じているのではないかと予測する。
また、逆Claisen反応(エトキシドイオンの求核攻撃による V の開環反応)について考えると、問い 23.41 と同様、酸性水素が引き抜かれるために反応性は高くないと考えられるが、形式的に V から II を再生する過程以外に、VI や VII になる経路も考えられ、場合によっては主生成物以外の副生成物の原因になるかもしれない。
更に、I、II のエノラートは、より安定なエノラート IX に比べると存在する量はずっと少ないはずである。しかしながら IX からのアルドール反応や Claisen 縮合による生成物が優先するのではなく、I 由来で反応は進行する。これは、IX 自身が β-ケトエステルのエノラートで安定であり、同時に、この位置からの求核攻撃では、角度歪みが大きく、したがってより不安定である4員環生成物しか生じないことにより、平衡反応が出発物質側に大きく偏ることが理由として挙げられる。この IX 由来の反応では、いずれも X や XI のような構造の中間体を経由するものの、すぐに安定なイオン(β-ケトエステルのエノラート:青の部分)を脱離する反応により IX を再生してしまうという理解の仕方もできる。
23.49, 47
エナミンのピロリジン環は、窒素の孤立電子対が共役した二重結合の π結合と平行になるために、二重結合をほぼ同じ面内にあるような構造をとろうとすると考えられる。この条件で分子模型を組んでみること。
(解答例)
エナミンのピロリジン環は、窒素の孤立電子対が共役した二重結合の π結合と平行になるために、二重結合をほぼ同じ面内にあるような構造をとろうとすると考えられる。
一方で、エナミンのメチル基は、二重結合に結合している場合には、ペリフェラル方向しか向くことができないために、ピロリジン環との間に立体障害が生じ、不安定となる。これに対し、二重結合に結合していない場合には、アキシアル方向に向くことができるので、ピロリジン環との間の立体反発が無い。
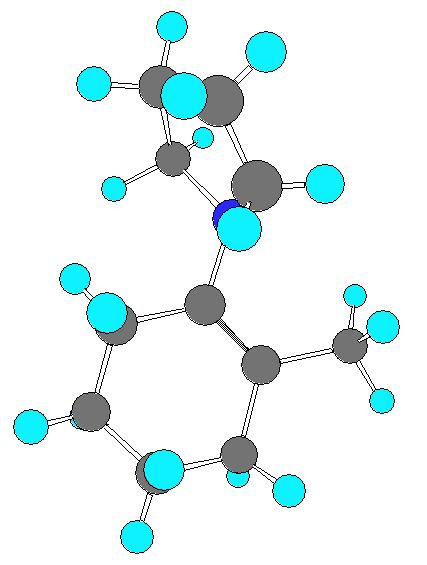
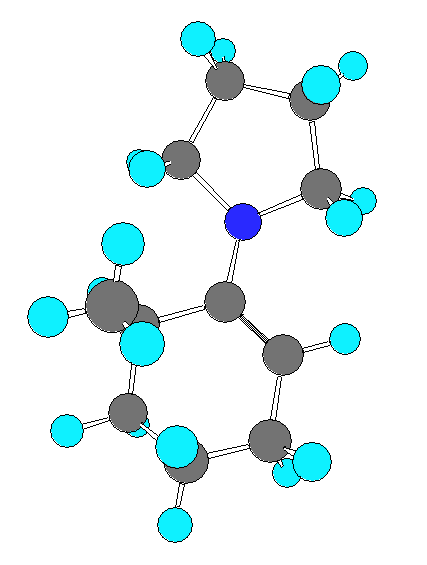
(左:メチル基との反発により、ピロリジン窒素が二重結合の π電子と平行になれない。
右:メチル基はアキシアル方向を向く。ピロリジン環との反発は小さい。)
23.50, 48
問い 23.22 など、Robinson 環化反応との類似で考えよ。ただし、Robinson 環化の第一段階である Michael 付加は、モノケトンのエノラートからはほとんど進行しない。
(解答例)
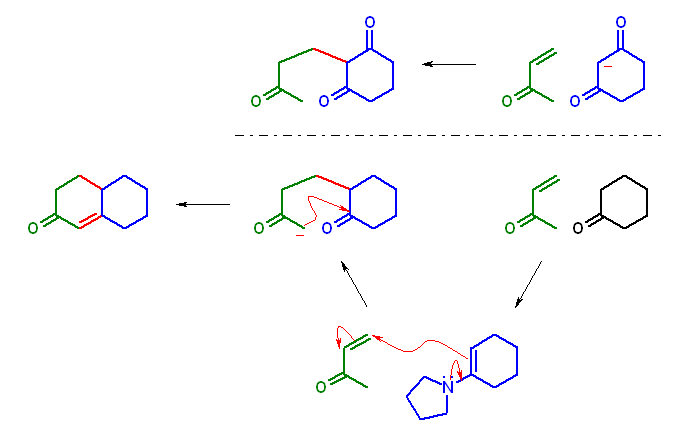
α, β-不飽和ケトンへの共役付加(Michael付加)は、モノケトンのエノラートからはほとんど進行しないので、エナミンを形成してから反応させる。エナミンは、形式的にはエノラートと同じ反応生成物を与えるので、エノラートのシントンとして用いられる。※
cyclohexanone と pyrrolidine から誘導されたエナミン、1-cyclohex-1-enylpyrrolidine と、but-3-en-2-one との反応によって得られる Michael 付加体、2-(3-oxobutyl)cyclohexanone は、はじめ側鎖の2位に負電荷を持つが、末端4位から酸性水素を引き抜く形で(どちらもカルボニル α 位なので、同程度に酸性で、アニオンの負電荷は、側鎖2位と側鎖4位の両者の平衡(←共鳴ではない)にあると考えられる。)生じた末端のエノラートが、続いて分子内アルドール反応を行うことで目的生成物
bicyclo[4.4.0]dec-1-en-3-one (付加命名法においては、4,4a,5,6,7,8-Hexahydro-3H-naphthalen-2-one ※2)
を与える。
側鎖2位の炭素からの求核攻撃が起きないのは、塩基触媒存在下で逆反応があるために生成物同士が平衡になるアルドール反応においては、より安定な生成物を優先して与えるからである。(側鎖2位の炭素からの求核攻撃では、結合角歪みの大きな4員環生成物となる。)
註※:エナミンの形成、および反応とその後の加水分解の機構の詳細については、問い 23.19(a) の解答例および「発展」の項等を参照すること。
註※2:問い 23.10 も参照すること。
23.51-23.62
23.51, 49
問い 23.50 を参照すること。(b) に関しては、問い 23.49 のヒントになる。
(解答例)
α, β-不飽和ケトンへの共役付加(Michael付加)は、モノケトンのエノラートからはほとんど進行しないので、エナミンを形成してから反応させる。
(a)
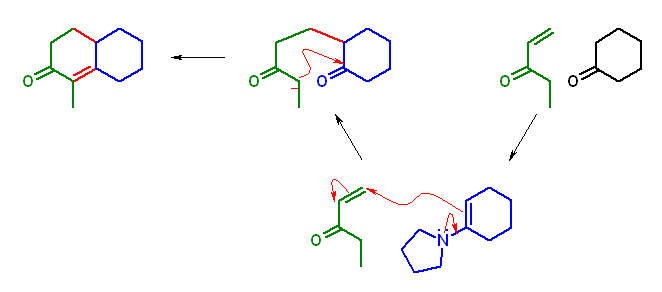
cyclohexanone から誘導したエナミン 1-(cyclohex-1-enyl)pyrrolidine により、α, β-不飽和ケトン pent-1-en-3-one に共役付加させ、その Michael 付加体 2-(3-oxopentyl)cyclohexanone からの分子内アルドール縮合により、目的生成物 2-methylbicyclo[4.4.0]dec-1-en-3-one (付加命名法:1-methyl-4,4a,5,6,7,8-hexahydro-3H-naphthalen-2-one)を得る。
(b)
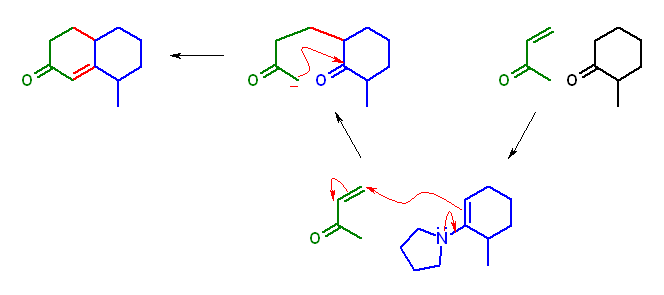
2-methylcyclohexanone から誘導したエナミン 1-(6-methylcyclohex-1-enyl)pyrrolidine により、α, β-不飽和ケトン but-3-en-2-one に共役付加させ、その Michael 付加体 2-methyl-6-(3-oxobutyl)cyclohexanone からの分子内アルドール縮合により、目的生成物 10-methylbicyclo[4.4.0]dec-1-en-3-one (付加命名法:8-methyl-4,4a,5,6,7,8-hexahydro-3H-naphthalen-2-one)を得る。
ここで用いるケトンはカルボニル基に対して非対称であるが、問い 23.49 に示したような理由により、エナミンは目的のものが主に生じる。
(c)
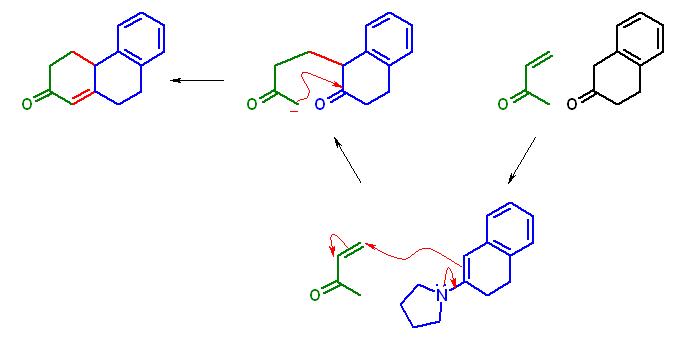
3,4-dihydro-1H-naphthalen-2-one から誘導したエナミン 1-(3,4-dihydronaphthalen-2-yl)pyrrolidine により、α, β-不飽和ケトン but-3-en-2-one に共役付加させ、その Michael 付加体 1-(3-oxobutyl)-3,4-dihydro-1H-naphthalen-2-one からの分子内アルドール縮合により、目的生成物 4,4a,9,10-tetrahydro-3H-phenanthren-2-one を得る。
ここで用いるケトンはカルボニル基に対して非対称であるが、構造的に考えられるもう一方のエナミンと比較して、上の機構に描かれたものの方が、フェニル基との共役によってより安定であるため、熱力学的支配の条件においては、主生成物とすることが可能であると考えられる。
23.52, 50
たとえカルボニルの α 位であってもビニル水素は酸性ではないから、この出発物質2種の組み合わせい対して塩基を加えたときに引き抜かれるべき水素はひとつしかない。
また、エノン ene + one と同様に、イノン yne + one も Michael 付加の受容体となる。
(解答例)
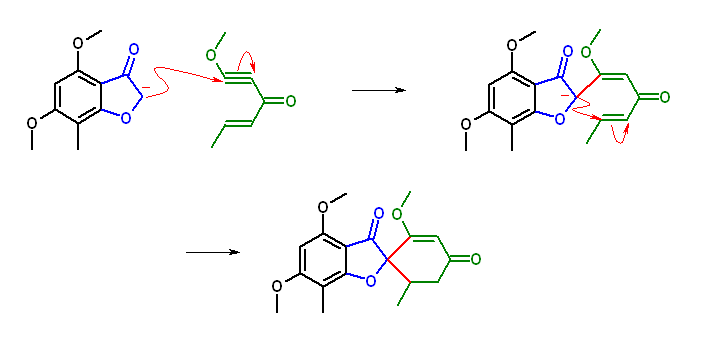
原著論文にあたったわけではないので、詳細は不明。しかし、上図のような2回の Michael 付加が生じることで目的の構造を与える。ただし、実際のところは、
エノンへの Michael 付加とイノンへの Michael 付加のどちらが先に生じるのか、
エノンへの Michael 付加により生じるメチル基の立体をどうやって制御するのか
などは、この教科書内での情報では説明できない。
23.53,
出発物と生成物の構造を見比べればよい。
(解答例)
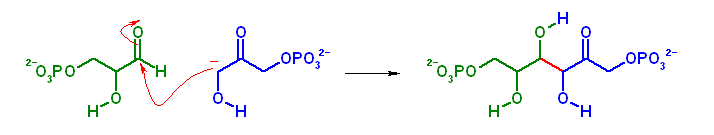
上図のように、形式的には Aldol 反応により、付加体を生じている。
均一溶液中では、求核体となっているジヒドロキシアセトンリン酸(青色の分子)中に、カルボニル α 水素より酸性度の高い水酸基水素があるので、このような反応は通常は考えられない。生体内では、酵素等によって反応場が与えられるから、位置特異的、あるいは立体特異的な反応が可能となる。
23.54, 51
マロン酸ジエステルは、酸性度の高い水素を持つ。
アルドール縮合の変形と見ることもできるし、マロン酸エステル合成の変形とみることもできる。
(解答例)
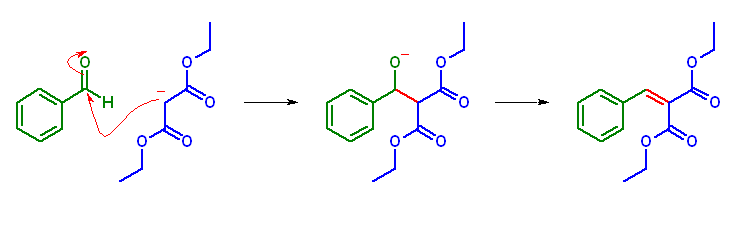
マロン酸ジエチルより生じたエノラートが、アルデヒドに対して求核付加したのち、アルドール縮合と同様に脱水する。diethyl 2-benzylidenepropanedioate (別名 2-benzylidenemalonic acid diethyl ester) は、マロン酸エステル合成のときと同様に、加水分解により β-カルボニル酸の構造となるから、容易に脱炭酸する。
23.55, 52
問い 23.35、23.39(d) も参照してください。
(解答例)
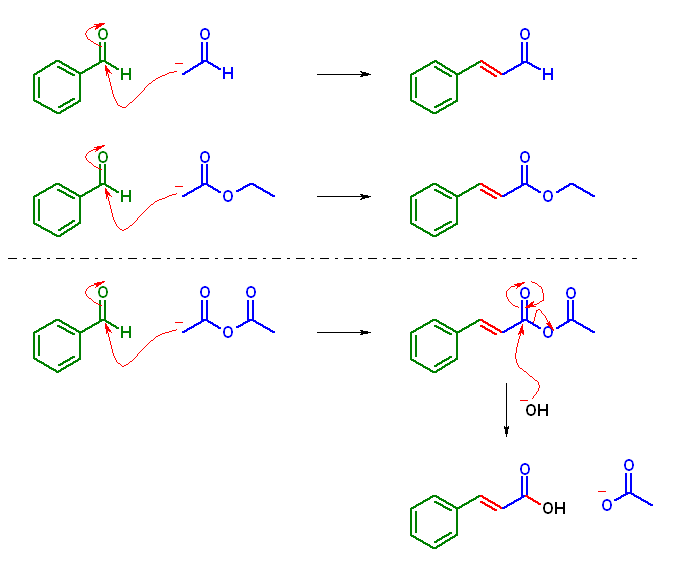
ベンズアルデヒドは、問い 23.35、問い23.39(d) にも示されるように、アセトアルデヒド、酢酸エステルとの交差アルドール縮合によってシンナムアルデヒド、ケイ皮酸エステルを与える。
これと同様に、無水酢酸 acetic anhydride との交差アルドール縮合によって、酢酸ケイ皮酸無水物 acetic cinnamic anhydride を与える。これを加水分解することにより、ケイ皮酸 cinnamic acid (系統名:3-phenylprop-2-enoic acid) が得られる。
いうまでも無いが、無水酢酸は、カルボニル α 水素を持つ。ただし、この酸性水素を引き抜くための塩基として、CH3CO2- を用いていることに注意せよ。これは、塩基はかならず求核種としても働くので、もし EtO- を塩基として用いた場合、酸無水物と1対1で反応して 酢酸エチル ethyl acetate を与えてしまうからである。(酢酸エチルからエノラートを発生させる際に、水酸化ナトリウムなどを用いることができなかったのと同じ理屈である。)
このことを考え合わせると、求核種に酸ハロゲン化物からのエノラートを用いることがほとんどない(例外は、HVZ 反応 : 教科書 22.4 節)ことの理由が判るはずである。
酸無水物の命名については、教科書 p811 などを参照してください。
・日本語では acid の語がなくても「…酸無水物」と訳す。「無水…酸」と訳すのは4種類、無水酢酸、無水コハク酸、無水マレイン酸、無水フタル酸に限る。
・混合無水物は、異なる2種類の酸から誘導される無水物、すなわち非対称な無水物である。 IUPACでは酸名の形容詞を必要なだけアルファベット順に並べる。
引用は、外部リンク:http://homepage1.nifty.com/nomenclator/text/anhydrid.htm
23.56, 53
これも、通常通りに考えれば説明できる。
(解答例)
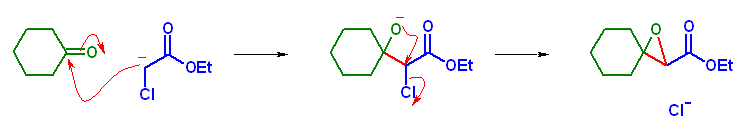
クロロ酢酸エステルより生じたエノラートが、カルボニル化合物に求核付加すると、アルドール型の付加反応によりアルコキシドを生じる。このアルコキシドが、塩素の結合した炭素に対し、分子内の求核攻撃を行うことにより、オキシラン環(エポキシ環)が形成される。
なお、この生成物は、ethyl 1-oxaspiro[2.5]octane-2-carboxylate である。 oxa は、炭素を酸素で置換したもの。したがって、spiro[2.5]octane の1位のメチレンが酸素になった化合物をさす。※
もし、環状ケトンからの生成物でなければ、スピロ構造をもたず、したがってエポキシ環をオキシランとして命名することができる。たとえば、アセトアルデヒドとクロロ酢酸エチルによる Darzens 反応での生成物は、 ethyl 3-methyloxirane-2-carboxylate となる。
註※:スピロアルカンの命名については、
・接頭辞 spiro- スピロ を用いる。
・各スピロ原子を結ぶ鎖を構成する骨格原子の数をピリオド(コンマではない)で区切って並べ、角カッコで囲んで表示する。
・番号付けは、小さい環のスピロ原子の隣の原子から始め、この環を回ってスピロ原子に至り、次いで第2の環を一周する。
引用は、外部リンク:http://homepage1.nifty.com/nomenclator/text/sp_alk.htm
二環系においては、橋の長い順に回ったことと対照的なので注意すること。
すなわち、二環系の番号付けでは、第一の橋頭を1位とし、最長の橋を経て、第二の橋頭へ至り、さらに主環を回る。最後に主橋(二環系では最短の橋)に、第一の橋頭の隣から番号を付ける。
引用は、外部リンク:http://homepage1.nifty.com/nomenclator/text/baeyer.htm
23.57, 54
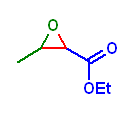
とにかく、出発物と目的生成物の構造を見比べて、同じ場所はどこなのか、反応したのはどこなのかを探す必要がある。たとえば反応していない置換基としてイソプロペニル基がある。
一般に、このような問題は、逆合成の考え方の方が速く正解にたどり着けるだろう。まず、目的生成物を与えるようなアルドール反応を考えること。
次いで、Michael 反応において、求核種となる箇所、および受容体となる箇所を探すこと。
(解答例)
分子内アルドールにより目的生成物を与えているのだから、最終生成物中の水酸基の炭素が、求核攻撃をうけた位置である。求核種はもうひとつのカルボニルの α位のエノラート炭素。そう考えると、次の反応がかける。
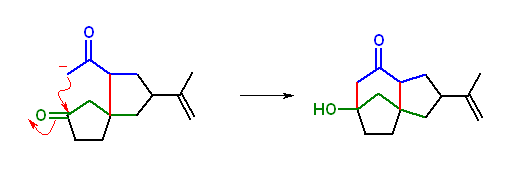
次に、この spiro[4.4]nonane の誘導体を与えるような Michael 付加を考えればよい。
Michael 付加は共役エノンに対しての求核攻撃により生じる。また、求核種は、ケトンに由来するエノラートである。
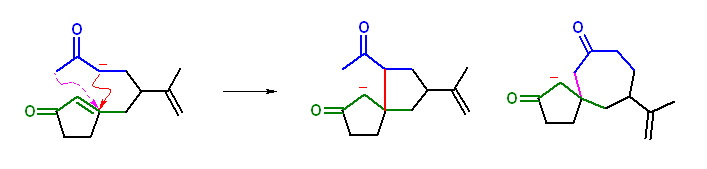
通常は、モノケトンのエノラートは(不安定であるために、平衡で生じている量が少なく)Michael 付加体をほとんど与えないが、分子内反応では、わずかにしか生じないエノラートでも速やかに反応できるので、Michael 付加体を与えると解釈できる。
なお、このとき、ピンクの矢印で示したような攻撃があると7員環を与えるが、分子内反応で効率よく生じるのは、5員環、または6員環であることが多い。
8-hydroxy-3-isopropenyltricyclo[6.2.1.01,5]undecan-6-one の3次元模型
結構複雑な形ではあるが、上の3次元模型を見るとわかるように、分子内に歪みなどがほとんどない。
23.58, 55
ギルマン試薬による求核付加がはじめに生じている。ギルマン試薬は、Grignard 試薬など他の有機金属試薬と同じようにアルキルアニオンの等価体として反応する。共役付加以外には、酸塩化物のように特に反応性の高いカルボニル化合物とは反応してケトンを与えるが、ケトン、エステルなどとは反応しなかったことを思い出そう。
(解答例)
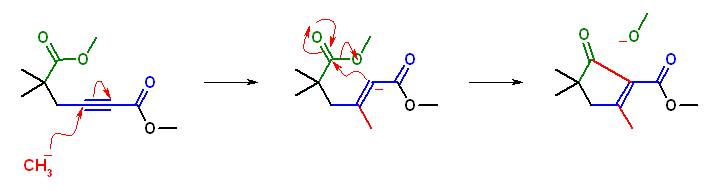
ここでは、(CH3)2CuLi を CH3- として書いている。エステルのカルボニル基に共役した三重結合に共役付加し、生じるビニルアニオンがすぐに分子内で Claisen 縮合によりエステルと反応する。
生成物の名称は、 methyl 2,4,4-trimethyl-5-oxocyclopent-1-enecarboxylate
23.59, 56
逆合成の方法で考えるのがよい。
とはいえ、この反応における出発物質は、実は酸性水素が1種類しかないから、はじめの段階の反応がどこで生じているのかもすぐに判るはずである。
(解答例)
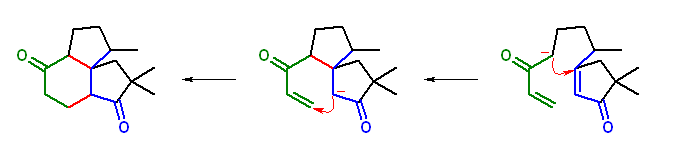
上図では、逆合成の方法で、最終生成物を与えるような Michael 付加を考え、次いでその中間体を与えるような Michael 付加を考えた。しかし、ヒントにも述べたように、この出発分子においては、酸性であるような α 水素は1箇所しかない。(ビニル水素は酸性ではないから。)
生成物の名称は、
3,3,12-trimethyltricyclo[7.3.0.01,5]dodecane-4,8-dione
23.60, 57
出発物と生成物を比較して、新たにできた結合と切れた結合より判断せよ。
(解答例)
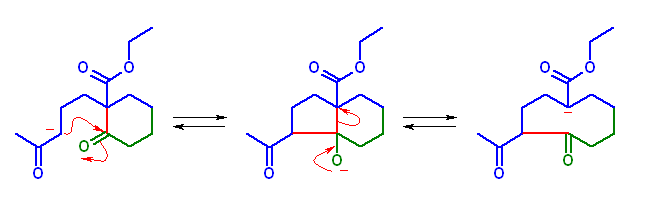
逆アルドール反応で9員環となるような反応が起きるのは、脱離するアニオンがエステル基の付け根にあり、エノラートとして安定であるからである。
生成物の名称は、ethyl 4-acetyl-5-oxocyclononanecarboxylate
23.61, 58
反応式をよく見比べること。
(解答例)
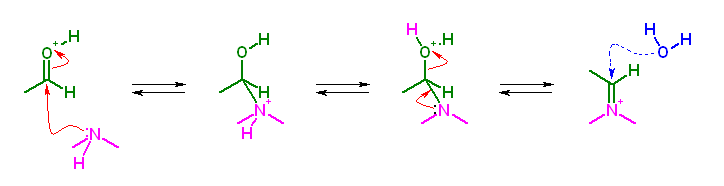
カルボニル化合物とアミンより酸触媒でイミンを生じる反応は、プロトン化されたカルボニル基(ルイス酸の配位により分極が強められて、より求核攻撃を受けやすくなる)に対して、フリーベースのアミンが求核攻撃する。(そのため、酸性が高すぎると、アミンがプロトン化されてしまい、反応が進行しなくなる。)
なお、イミニウムイオンは、
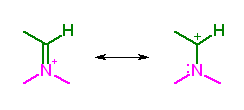
のような共鳴を持つから、(プロトン化されたカルボニル基と同様に)求核攻撃を非常に受けやすい。
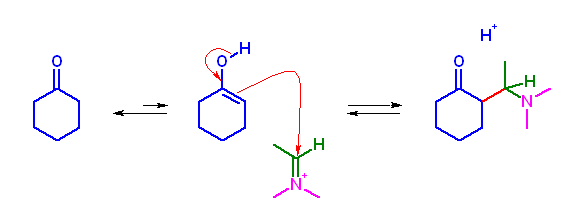
ケトンより酸触媒の存在下に生じるエノールが、イミニウムイオンに対して求核付加することで、Mannich 反応が進行する。
23.62, 59
反応式をよく見比べること。問い 23.61 からも判るように、カルボニル化合物に対し、β-アミノ化合物を生成物として与える。α-位には、イミニウムイオンを形成するのに使用したアルデヒド由来の炭素が来ている。
(解答例)
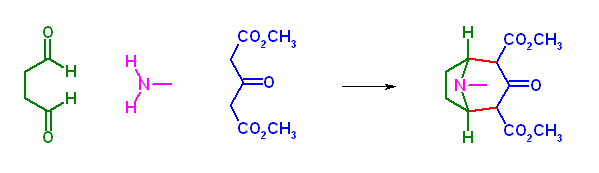
アミンは methyl amine、アルデヒドは butanedial を用いる。
なお、分子内で2箇所の Mannich 反応が生じているが、1箇所でのみ反応をさせた形式で反応機構図を示した。
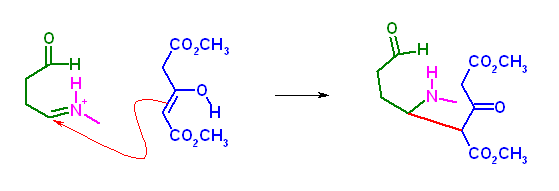
この後、同様に分子内の Mannich 反応によって、目的の dimethyl 8-methyl-3-oxo-8-azabicyclo[3.2.1]octane-2,4-dicarboxylate を得ることができる。
なお、β-ケトエステルの構造なので、加水分解によって容易に脱炭酸ができる。また、カルボニル基はヒドリド還元で水酸基に変換した後、安息香酸のエステルとすることが可能である。(もちろん、位置特異的、立体特異的に進行させるような工夫が必要である。)