21.01-21.10 (1-10)
21.01, 01
命名において、スペースを入れるべき場所と、そうではない場所に注意すること。
(b) シクロヘキサン環とカルボン酸誘導体では、カルボン酸誘導体の方が命名における優先順位が高いから、シクロヘキシル基の結合したカルボン酸の誘導体として命名する。
解答書(6版、英語)の (g), (i) にミスあり。以下、解答例中、赤で示した部分が正しい。
(解答例)
(a) 4-methylpentanoyl chloride
(b) cyclohexylacetamide, or cyclohexylethanamide
6版 (c) isopropyl 2-methylpropionate, or isopropyl 2-methylpropanoate
(d) benzoic anhydride, or benzenecarboxylic anhydride
(e) isopropyl cyclopentanecarboxylate
(f) cyclopentyl 2-methylpropionate, or cyclopentyl 2-methylpropanoate
6版 (g) N-methyl-4-pentenamide
6版 (h) methyl (R)-2-bromopropionate, or methyl (R)-2-bromopropanoate
(i) 2,3-dimethyl-2-butenoyl chloride
5版
(c) 2-methylbutyronitrile, or 2-methylbutanenitrile
(g) 4-pentenamide
(h) 2-ethylbutyronitrile, or 2-ethylbutanenitrile
21.02, 02
解答書(6版、英語)の (e) の分子の命名にミスあり。エステルだから、「ethyl」と「3-oxo~」の間はハイフンではなく、スペース。
(解答例)
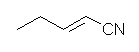
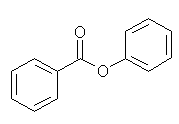
(a) 5版:2-pentenenitrile, 6版:phenyl benzoate
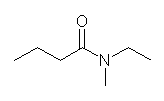
(b) N-ethyl-N-methylbutanamide
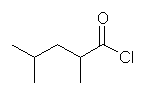
(c) 2,4-dimethylpentanoyl chloride
(d) methyl 1-methylcyclohexanecarboxylate
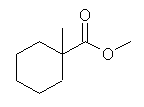
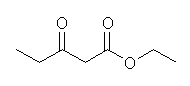
(e) ethyl 3-oxopentanoate
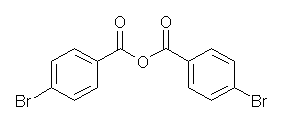
(f) bis(4-bromobenzoic) anhydride
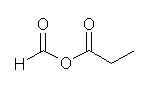
(g) formic propanoic anhydride
(h) cis-2-methylcyclohexanecarbonyl chloride
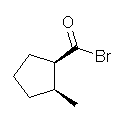
21.03, 03
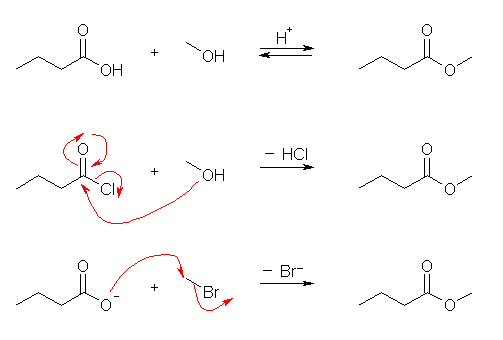
求核種は、メトキシドイオン。脱離基は塩化物イオン。
(解答例)
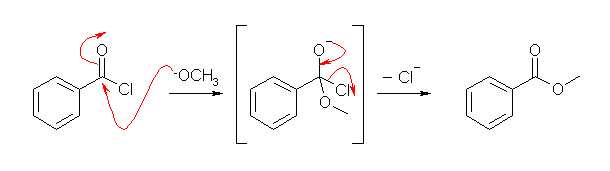
上機構の中央に示したような、4面体中間体を経由するから、求核アシル置換反応ではかならず曲がった矢印を計4本書かなければならない。(カルボニル酸素上への矢印と、カルボニル酸素からカルボニル炭素上へ(カルボニル酸素-炭素二重結合上へ)の矢印を省略することはできない。)
21.04, 04
(a) は、図 21.2 を参照すること。(b) は、この応用である。脱離基が脱離しやすいほど反応性が高い。脱離しやすい脱離基とは、強酸の共役塩基のかたちをしているものである。
(解答例)
脱離基の共役酸を強酸から弱酸になる順に並べると次のようになる。
(a) HCl > HOCH3 > NH3
(b) HOCH(CF3)2 > HOCH2CCl3 > HOCH3
カルボン酸は、電子吸引性の置換基が結合すると共役塩基(カルボキシラート)が安定になるため、その酸性度が上がる。
従って、求核アシル置換反応の反応性の高いほうから低いほうへ並べる。
(a) CH3COCl > CH3CO2CH3 > CH3CONH2
(b) CH3CO2CH(CF3)2 > CH3CO2CH2CCl3 > CH3CO2CH3
21.05, 05
この問いにおいては、求核アシル置換反応の脱離基は同じである。従って、求核アシル置換反応の反応機構における後半部分は同じである。つまり、前半部分に差が生じていることになる。
アルデヒドやケトンにくらべて、カルボニル基に電子供与性基の結合したエステルやカルボン酸誘導体でカルボニル求核反応の反応性が低かったことを思い出すこと。
(解答例)
トリフルオロ酢酸のエステルにおいては、トリフルオロメチル基は強い電子吸引性基である。このことによって、カルボニル基の炭素の正の部分電荷はより大きくなる。したがって、求核反応自体の反応性が高くなる。
21.06, 06
求核種はなにか、脱離基はなにか、を確認し、教科書 図 21.2 を参照すること。
(解答例)
(a) 求核種は -OH、脱離基は -OCH3。エステルの加水分解である。加水分解による生成物は CH3CO2H だが、水酸化ナトリウム存在下に中和されてナトリウム塩 CH3CO2Na を生じる。副生成物として生じるのは、脱離したメトキシドイオン -OCH3 が溶媒である水から H+ を受け取って生じるメタノール CH3OH である。
(b) 求核種は孤立電子対を持つ NH3、脱離基は Cl-。酸塩化物のアミノリシスである。中性の部分が付加して負のイオンが脱離するから、求核アシル置換により直接生じるのは正の電荷をもつ CH3CONH3+ であるが、速やかに H+ を失い、CH3CONH2 を与える。形式的には、副生成物として脱離するのは HCl であるが、反応条件として過剰に加えられているアンモニアと塩をつくり、塩化アンモニウム NH4Cl を与える。
(c) 求核種は -OCH3、脱離基は -OCOCH3。酸無水物のアルコーリシスによるエステルの生成反応である。脱離基であるアセテートイオンがナトリウム塩を生成し、副生成物として CH3COCH3Na を与える。
21.07, 07
教科書、図 21.1 の求核アシル置換反応の反応機構を参照すること。教科書の問いに与えた図の、形式電荷の位置、多重結合の有無等を判別するため、それぞれの原子の結合の数等を確認しながら構造式に書き起こしてみること。
カルボン酸(誘導体ではなく、カルボン酸そのもの)に対して、負の電荷をもつ求核種は塩基としてもはたらき得るから、酸性度の高い水素を引き抜いてカルボキシラート RCO2- を生じてしまう。カルボキシラートは負電荷を帯びているから、負電荷をもつ求核種からの求核攻撃は受けない。(酸性条件のエステルの加水分解は全過程が可逆であったのに対し、塩基性条件でのエステルの加水分解が不可逆であった理由を思い出すこと。)
(解答例)
出発物質のカルボン酸誘導体は、メチルエステル、求核種は水酸化物イオン -OH、4面体中間体からの脱離基は -OCH3 で、この加水分解により生じる生成物はカルボン酸。ただし、アルカリ性条件であるから、カルボキシラート(カルボン酸塩)となる。
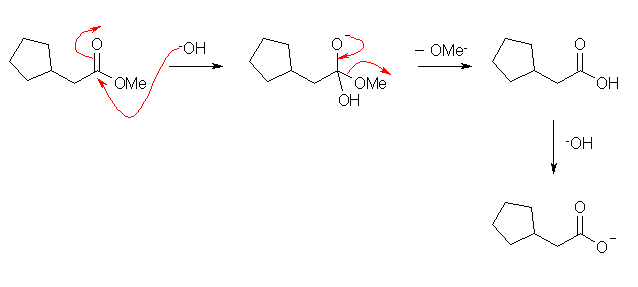
21.08, 08
エステルの合成法にはいくつかの方法がある。代表的なものとして、最低限、授業でやった以下のようなものを整理しておくこと。
1) Fischer のエステル化法。
2) カルボン酸誘導体のアルコーリシスによる方法。
3) カルボキシラートを求核種とする方法。
(解答例)
1) Fischer のエステル化法では、過剰のアルコール中にカルボン酸と酸触媒を加え、加熱還流させる。酸触媒としては、硫酸や塩酸などの強酸を用いる。安価で、溶媒として用いることができるような液体であるアルコールに適した方法である。反応機構は、教科書、図 21.5 を参照すること。
2) アルコーリシスによりエステルを生じることが可能なカルボン酸誘導体は、酸ハロゲン化物、または酸無水物である。ただし、酸無水物では脱離基部分の方がカルボン酸塩となってしまい、エステルにならないから、半分が無駄になってしまう。また、エステルのアルコーリシスによるエステルの生成も例外的には可能である。脱離するアルコールの沸点が低いなどの理由により系から除くことが可能な場合、脱離するアルコールにハロゲンなどの電子吸引性基がついて酸性度の高い(したがって、他のアルコールよりも脱離しやすい)場合などである。
3) 1級または2級のハロゲン化アルキルに対し、カルボキシラートが求核置換するとエステルを生じる。
(a)
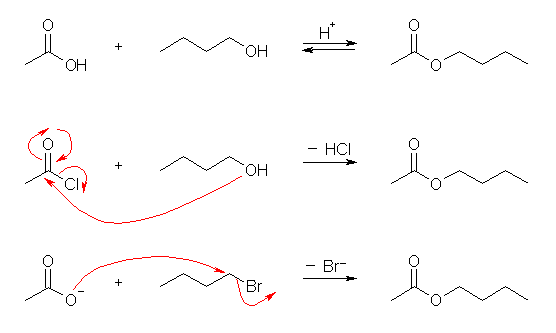
(b)
21.09, 09
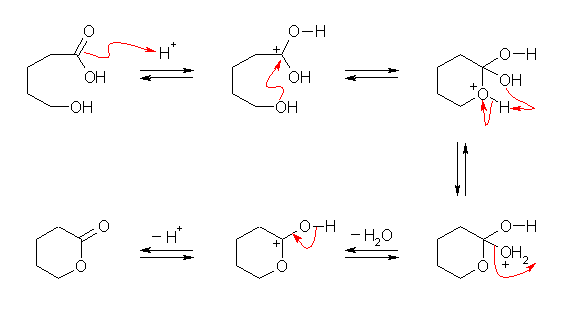
5-ヒドロキシペンタン酸は、分子内に水酸基とカルボキシ基を同時に持つから、酸触媒で処理することにより分子内エステル化反応が進行し、環状エステル(ラクトン)を与える。
(解答例)
21.10, 10
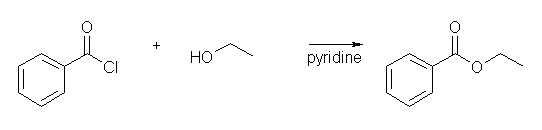
エステルと対応したカルボン酸塩化物に、アルコールを加える。ただし、生じる塩酸をトラップする目的で、求核性の小さな塩基(ピリジンやトリエチルアミンなど。(アミンを用いる場合は3級のアミンに限る。)を加える。1級、2級のアミンを加えるとアミドが生じてしまうので使えない(アルコールより、一般にアミンの方が求核性が高かったことを思い出すこと。)
(解答例)
(a) propionyl chloride (or, propanoyl chloride) + methanol → methyl propionate (or methyl propanoate)
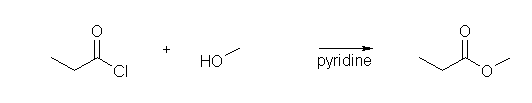
(b) acetyl chloride (or, ethanoyl chloride) + ethanol → ethyl acetate (or ethyl ethanoate)
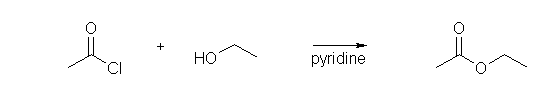
(c) benzoyl chloride (or, benzenecarbonyl chloride) + ethanol → ethyl benzoate (or ethyl benzenecarboxylate)
21.11-21.20 (11-21)
21.11, 11
教科書の関連箇所の記述(Fischer のエステル化法を含めたカルボン酸の求核アシル置換反応については、教科書 21.3 節。酸ハロゲン化物のアルコーリシスについては、教科書 21.4 節)をよく読むこと。
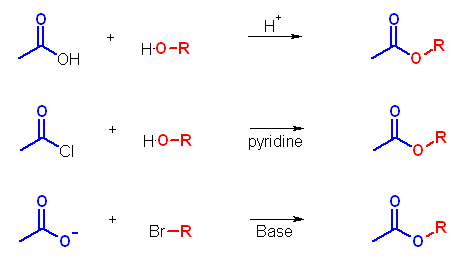
Fischer のエステル化法も、酸塩化物とアルコールの反応も、どちらもアルコールの酸素がカルボニル炭素へ求核攻撃する。従って、カルボニル炭素上で求核アシル置換反応が生じ、上図のようにエステル中の酸素はアルコール由来となる。
これに対し、ハロゲン化アルキルへのカルボキシラートによる求核攻撃での反応では、求核置換反応はハロゲン化アルキルの炭素上で起きる。生成物中のエステル酸素は、カルボン酸由来となる。
(解答例)
Fischer のエステル化法も、酸塩化物とアルコールの反応も、いずれもカルボニル基上での求核アシル置換反応で、4面体型の中間体を経由して起きる。3配位の sp2 混成炭素と比較して、4面体型の sp3 混成炭素の方が、その炭素上で隣接した結合同士の距離が短くなるから、立体的に混み合ったアルコールでは、エステル生成の反応において中間体が不安定化をうける。このため、第2級アルコールを用いたエステル化は、第1級アルコールを用いたときよりも相対的に反応が遅くなる。
シクロヘキサノールは第2級のアルコールであるから、求核反応の中心となる酸素の付近は、第1級のアルコールと比較して立体的に混み合っている。Fischer のエステル化法も、酸塩化物とアルコールの反応も、いずれも第1級のアルコールを用いた場合より遅くなる。もともと、Fischer のエステル化法はアルコール溶液中での加熱が必要な反応で、室温では遅くしか進行しない。酸塩化物とアルコールの反応は室温で十分に反応が進行するほど速い反応である。従って、(相対的に遅くなることが予測される)第2級アルコールとの反応は、より反応性の高い酸ハロゲン化物との反応を用いるほうがよい。
21.12, 12
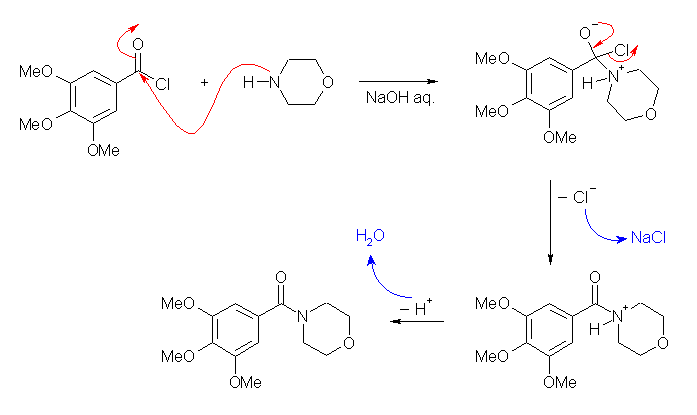
アミノリシスも、アルコーリシスも、加水分解と同様の反応機構で進行する。教科書の 21.4 節、酸ハロゲン化物の加水分解の部分の記述および反応機構を参照すること。アルコーリシスにおいては酸素の、アミノリシスにおいては窒素の、それぞれ孤立電子対が求核反応に関与する。
(解答例)
21.13, 13
原料として用いる酸塩化物およびアミンは何であるかを、判断すること。反応の条件は、問い 21.12 において、トリメトジン trimetozine を合成する際と同じでよい。
教科書 21.4 節、酸塩化物のアミノリシスの記述にあるように、生じる塩酸のトラップのために塩基を加える必要がある。(求核種であるアミンが塩酸との塩(塩化アンモニウム塩)を作ると、求核性を失い、反応が進行しない。)このためには、アミンを酸塩化物に対して2モル等量加えるか、あるいは水酸化ナトリウムのような塩基を加える。ただし、反応で生じる塩酸のトラップのために水酸化ナトリウムを用いる場合、水酸化物イオン自体も高い求核性をもつから、「酸塩化物 + 水酸化ナトリウム」の組み合わせの中にアミンを加える方法では、加水分解による副生成物がかなりの量生じると予想される。これを避けるためには、「アミン + 水酸化ナトリウム」の組み合わせの中に酸塩化物を加えるなどすればよい。
(解答例)
水酸化ナトリウムなどの塩基存在下(または2等量のアミンを用いて)以下の組み合わせで反応させる。
(a) propionyl chloride (or, propanoyl chloride) + methylamine → N-methylpropanamide
(b) benzoyl chloride (or, benzenecarbonyl chloride) + diethylamine → N,N-diethylbenzamide (or, N,N-diethylbenzenecarboxamide)
(c) propionyl chloride (or, propanoyl chloride) + ammonia → propanamide
特に (c) のようにアンモニアを用いるような場合、アンモニア水を過剰に用いるのが普通である。(常温で気体であるアンモニアは安価であると同時に、水溶液として用いてもアンモニアの揮発性が高く、そもそも正確に秤量することが難しい。)また、(a) のメチルアミンも常温で気体であるから、メチルアミン水溶液を過剰に用いるのが一般的である。常温で気体のアミンは、気体として、あるいは水溶液として正確に秤量することは難しいが、その塩酸塩(一般に常温で固体なので、正確な秤量が容易である)を水酸化ナトリウム溶液中に加えて、系中でアミンを発生させる方法をとることもできる。
21.14, 14
教科書 21.4 節中、酸塩化物と有機金属試薬の反応についてよく読み、反応機構を参照すること。また、非対称なケトンの合成においては、カルボニル基の左右の置換基のいずれを酸塩化物とするかにより2通りの可能性がある。
(解答例)
(a)
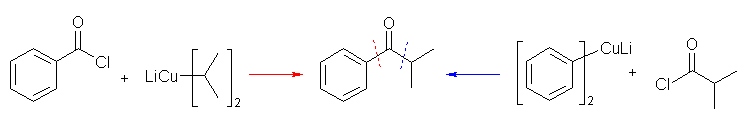
(b)
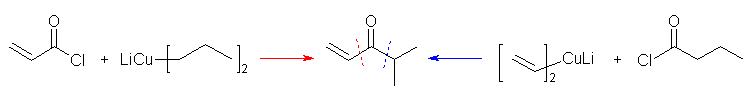
なお、これらの反応は有機銅(I)酸リチウムの代わりに、他の有機金属試薬(たとえば Grignard 試薬)を用いた場合、生じたケトンが更に反応してしまうことに注意する。
21.15, 16
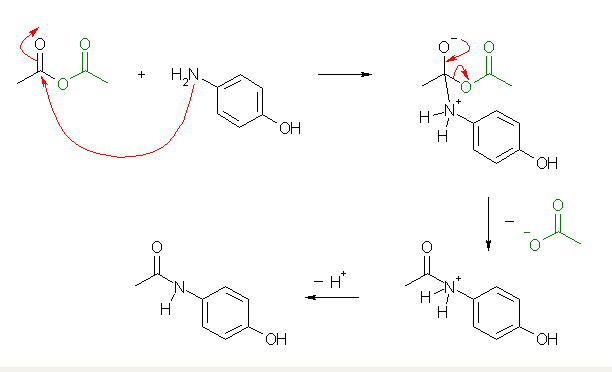
酸無水物における求核アシル置換反応については、教科書 21.5 節をよく読むこと。求核アシル置換反応において、脱離基がやや大きいため酸塩化物やエステルなどと異なる構造のように思いがちだが、次図のように、他のカルボン酸誘導体と同じであるものとして捉えること。
p-ヒドロキシアニリンは、分子内に水酸基とアミノ基をもつ。酸素、窒素ともに孤立電子対をもちから求核性を示すが、水酸基よりアミノ基の方が求核性が高い。
(解答例)
21.16, 15
問い 21.15 の解答例で示したように、酸無水物の求核アシル置換反応においても脱離基も含めて電子の流れを考えて反応機構を書けば、この問題も同じよう解くことができる。
(解答例)
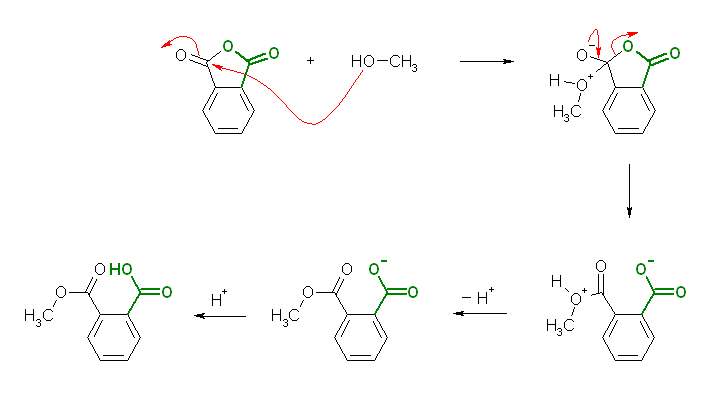
この問いの文にいわく「この無水物のほかの”半分”」、つまり、求核アシル置換反応における脱離基はカルボキラートで、酸性条件ではカルボキシ基となる。ここで生じたカルボン酸は、アルコールが存在するだけではエステル化は進行しないから、環状の酸無水物のアルコーリシスでは、ジカルボン酸のモノエステルが生じる。(ジエステルは生じない。)
21.17
アミンと酸無水物の反応を完結させるために、塩基を加えなければならない理由を問うこの問題で、過剰の塩基が存在しないときに何が起きるかを考えるためには、酸無水物のアミノリシスの反応機構を書いてみること。
酸ハロゲン化物のアミノリシスについての問い、21.3 のヒントも参照すること。
(解答例)
反応の進行により、酸塩化物の求核アシル置換反応では塩酸が生じたように、酸無水物の求核アシル置換反応ではカルボン酸を生じる。アミノリシスでは、反応を完結させるためには、反応の進行とともに生じる酸をトラップするため、過剰のアミン、またはもう1当量の NaOH などのような塩基を加える必要がある。
アミノリシスにおける求核種、すなわちアミンは、酸が存在すると塩を生成し、求核性を失い、反応が進行しなくなる。つまり、酸無水物と同量のアミンを加えても、1/2 当量が反応した時点で残りのアミンは塩を生成してしまうから、全体の半分しか反応が進行できない。
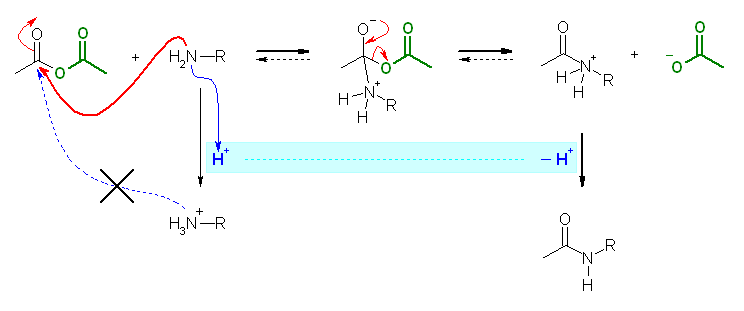
4面体中間体(上段、中央)からの脱離の段階では、アミンが抜けると出発物質である酸無水物を与え、カルボキシラートが抜けることによりプロトン化アミドを与える。カルボン酸誘導体の求核アシル置換反応の反応性を思い出すこと。反応は主に右向きに進行する。
なお、酸のトラップのために加える塩基として NaOH を用いる場合、はじめに酸無水物と NaOH を混合してしまうと副反応として加水分解がおきてしまう。
21.17, 18
ケン化(エステルのアルカリによる加水分解)の反応機構については、教科書、図 21.9 を参照し、各段階についてよく吟味すること。すべての過程が可逆であれば反応全体も可逆となるはずであるが、一箇所でも不可逆な過程がふくまれれば、全体としても不可逆になる。
(解答例)
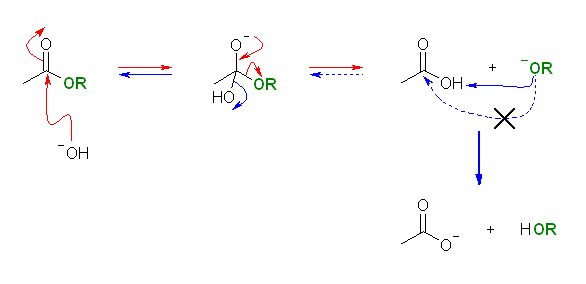
エステルに水酸化物イオンが求核的に付加すると、4面体型中間体(上段、中央)を生じる。この中間体から水酸化物イオンが脱離(青、左向き矢印)すると出発物質であるエステルを再生する。アルコキシドイオン -OR が脱離(赤、右向き矢印)するとカルボン酸を生じる。
カルボン酸のカルボニル基にアルコキシドイオンが求核付加すれば、4面体型中間体にもどるが、反応系は塩基性であるから、これに優先して酸-塩基反応(下向きの矢印)によりカルボキシラート(と中和による水)を生じる。(アルカリとして加えてある水酸化物イオン以外に、アルコキシドイオンも求核種であると同時に塩基性をあわせもつから、アルコキシドイオンも酸-塩基反応に関与し、アルコールを与える。水とアルコールの pKa の差はさほど大きくないが、アルコールの方が若干酸性度が小さければ、存在量に差がなければ水酸化物イオンよりアルコキシドイオンの方が塩基として先に反応すると考えてもよい。ただし、反応系中にアルカリとして過剰の水酸化物イオンを加えている場合は、水酸買う物イオンが酸-塩基反応に関与すると考えるべきである。)
これによって生じたカルボキシラートは、負電荷を帯びているから、これ以上求核攻撃を受けない。また、塩基性の水溶液中には有意な量の H+ は存在しないから、カルボン酸の形に戻る分子もほとんどない。
最後の酸-塩基反応は、カルボン酸の酸解離平衡として捉えることで理解してよい。
AH ←→ A- + H+
酸解離平衡で生じた H+ は、水酸化物イオンまたはアルコキシドイオンとの中和反応で消費されるから、平衡は右へずれ、カルボン酸の大部分がカルボキシラート A- の形で存在することになる。
21.18, 19
エステルに対し、還元剤として1モル当量の DIBAH を用い、-78℃で反応させると、ヒドリドによる攻撃が1段階おきて生じるアルデヒド中間体を生成物として単離することができる。温度が高い場合や LiAlH4 を還元剤として用いる場合では、このアルデヒド中間体は単離できず、もう1段階のヒドリド還元が進行して第1級のアルコールを生じる。
教科書 21.6節中の「還元:エステルのアルコールへの変換」のセクションには、LiAlH4 を還元剤として用いる場合のエステルの還元機構が示されているから、これを参照して、還元剤として1モル当量の DIBAH を用いたときの反応機構を書いてみること。
(解答例)
まずここでは、単純化した反応機構を示す。
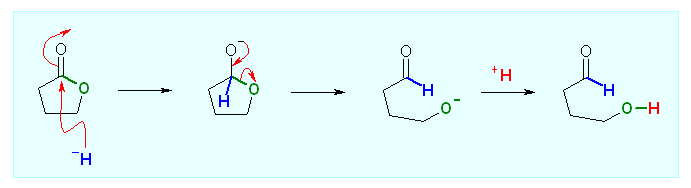
1当量のヒドリドによる求核アシル置換反応で、アルデヒド中間体を生じ、これが反応処理の加水分解で生成物の 4-hydroxybutanal を与える。
LiAlH4 などを還元剤として用いる場合は、系中で生じるアルデヒドも2段階目のヒドリドによる求核的な攻撃をうけると、次図のようにアルコールまでヒドリド還元される。
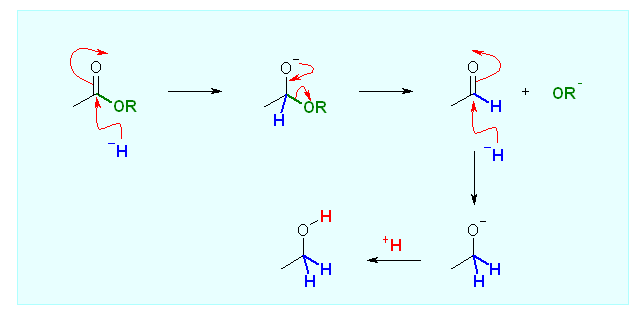
以下、単純化しないで反応機構を書いてみる。
まず、LiAlH4 は、Li+ AlH4- のように解離する塩である。これを用いたエステルのヒドリド還元では、カルボニル基に Li+ イオンがルイス酸として配位する。ルイス酸の配位は、カルボニルの分極を大きくするから、求核攻撃を受けやすくする。その結果、(イオン間のクーロン相互作用により、カルボニル酸素やリチウムイオンの近傍に弱く束縛されている) AlH4- イオンの中のヒドリドが、このカルボニル基に求核的に付加して、4面体型の中間体(下図、上段中央)を生じる。Li+ と RO- が脱離してアルデヒド中間体となるが、そのカルボニル基に AlH3 がルイス酸として配位しながら、ヒドリドの求核付加が起きる。この反応では、アルミニウムトリアルコキシドを生じるから、その加水分解により、アルコールと水酸化アルミニウムを与える反応となる。
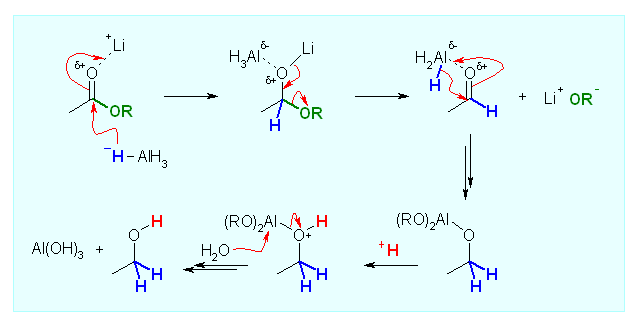
同様に、1モル当量の DIBAH を用い、-78℃ で反応させたときの反応機構を書くので、上の LiAlH4 を用いた場合と比較しておくこと。
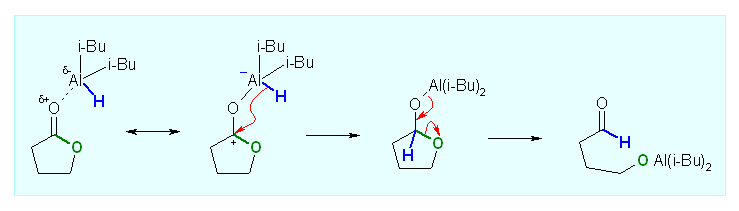
LiAlH4 のときとは異なり、はじめにカルボニル酸素に配位するのは、Li+ ではなく、それ自身がルイス酸性をもつ DIBAH である。カルボニル基へのルイス酸の配位によって分極が大きくなるので、カルボニル炭素に DIBAH 中のヒドリドが求核的に付加する。この反応機構の図では、あらためてルイス酸の配位がカルボニルの分極を助けることを示すため、共鳴構造を書いている。( LiAlH4 を用いたときに、Li+ の配位が起きたときも、同様の共鳴を書くことが可能である。)
DIBAH は、アルミニウム上にヒドリドを1つしか持っていないので、2段階目のヒドリド還元は生じない。(1モル当量の DIBAH しか加えていない場合は、特に低温で反応をおこなったとき、系中のすべての DIBAH はエステルに配位するから、遊離したヒドリド供与体が存在せず、従ってアルデヒド中間体はこれ以上還元されない。)
エステルよりもアルデヒドの方がヒドリド還元を受けやすかったことを思い出すこと。それにも係らず、1当量の DIBAH ではエステルからアルデヒドを得ることができるのは、従って、まとめると、
・はじめにすべての DIBAH がエステル分子との間で1対1の錯体を作り、
・次いで錯体内での反応で、エステルがアルデヒドに還元されるが、
・その錯体内にはヒドリドを1つしか持たないため、2段階目の反応が起きない
ためである。
21.19, 20
エステルのヒドリド還元では、2種のアルコールを生じる。(メチルエステル(など)のような単純なエステルでは、その一方はメタノール(など)のようなアルコールであり、意図した生成物として意識されないことも多い。しかしながら、ここでは学習のために2種ともを挙げるようにすること。
(解答例)
(a) methyl 2-methylpentanoate → 2-methyl-1-pentanol + methanol
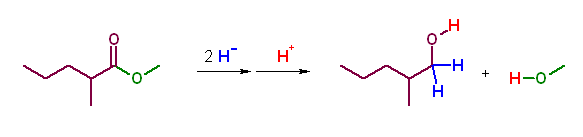
(b) phenyl benzoate → benzyl alcohol + phenol
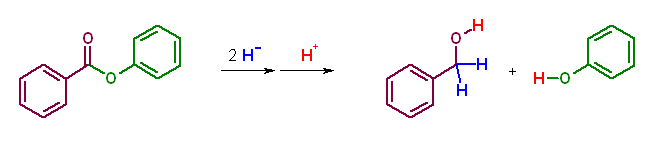
21.20, 21
エステルと Grignard 試薬の反応では、LiAlH4 を用いたヒドリド還元で2つのヒドリドが反応したのと同様に、2分子の Grignard 試薬が反応する。従って、生成物の3級アルコールのうち、水酸基の結合した炭素上に同じ置換基が2つある場合、その部分が Grignard 試薬由来であると判断できる。
(解答例)
次に示したエステル中の OR の部分は、脱離してアルコール ROH となってしまうから、どのような構造でもかまわない。(合成上は、R としてメチルなどを使う。これは、エステルの調製上の都合(Fischer エステル合成を用いる場合、安価なメタノールを用いることができるなど)のほか、グリニヤル反応で副生成物として生じるメタノールが沸点も低く容易に系から除いてしまえるからである。)
(a) 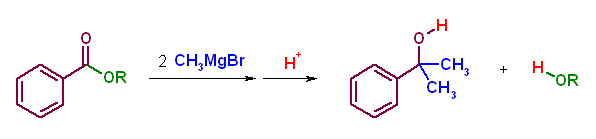
(b) 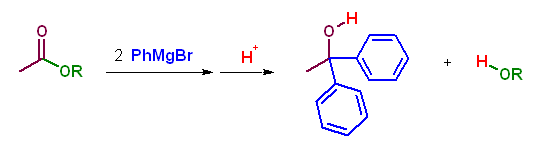
(c) 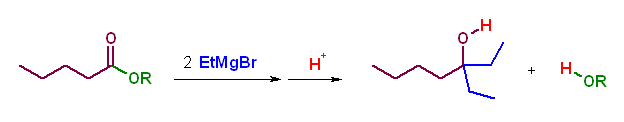
21.21-21.30 (22-34)
21.21, 22
教科書 21.7 節をよく読むこと。
N-ethylbenzamide の構造は次の通り。
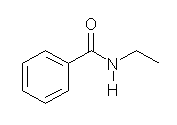
(解答例)
(a) 加水分解すればよい。水溶液中で加熱する。酸、塩基のいずれも触媒として用いることができる。
(b) 酸アミドはヒドリド還元でアミンを与える。酸アミドをカルボン酸やエステルに変換してから還元する必要がある。(a) の条件で加水分解して得た安息香酸を還元する。カルボン酸なので、BH3 での還元が適している。
(c) N-ethylbenzamide を LiAlH4 を用いて還元する。
21.22, 23
逆合成で考えること。
(解答例)
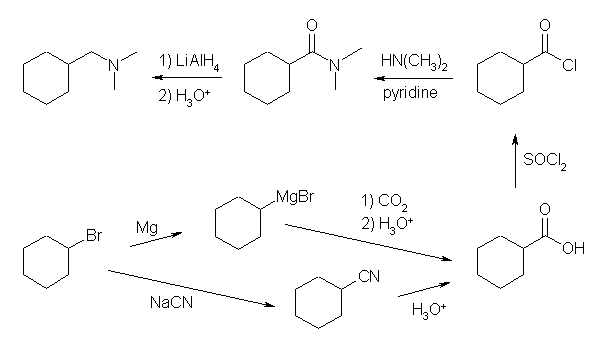
LiAlH4 による還元で (N,N-dimethylaminomethyl)cyclohexane を与えるのは、N,N-dimethylcyclohexanecarboxamide である。酸アミドは、酸塩化物のアミノリシスで合成できる。酸塩化物 cyclohexanecarbonyl chloride は、カルボン酸 cyclohexanecarboxylic acid の塩化チオニルによる処理で合成可能である。このカルボン酸の合成ルートとして、グリニヤル試薬と二酸化炭素の処理、ニトリル cyclohexanecarbonitrile の加水分解の2通りが考えられるが、環状の第2級のハロゲン化アルキルからの合成となるから、立体障害をうけやすい求核置換反応によるニトリルの合成を含む経路より、グリニヤル試薬経由の方がすぐれている。
21.24
「酸触媒によるニトリルの加水分解の反応機構を、電子の流れを示す曲がった矢印を使って書く」
教科書第5版 21.8 節(教科書第6版では 20.6 節)を参照すること。シアノ基 -C≡N は、カルボニルと同様に電気陰性度の異なる原子が多重結合で結合された構造である。したがって、カルボニル基 >C=O と同様に分極しており、同じ形式で求核攻撃を受けることが可能である。
従ってニトリルの加水分解は酸アミドの加水分解と類似の機構で進行し、酸によっても塩基によっても触媒される。
(解答例)
ここでは、ニトリルの加水分解の反応について、酸触媒、塩基触媒の両方の機構を示した。酸触媒での反応機構中には -OH を考えることはできない。(有意な量の存在がないため。)酸性条件下ではプロトン化をうけて分極の大きくなったカルボニル基に(中性、塩基性では十分な求核種としては働かない)水分子が求核攻撃をする。また、塩基触媒での反応機構では、H+ を考えてはいけない。H+ 付加と同等な段階を考える場合、水を付加させてから -OH を脱離させるなどする。
下の2つの反応機構について、酸触媒、塩基触媒の両者の対応に気をつけてよく見ること。それぞれの段階の大部分は、両者の間で対応している。また、どちらもニトリルから酸アミドを経由してカルボン酸に至る過程と考えることができることに注意すること。また、加水分解の途中の過程は可逆な段階もあるが、全体としては不可逆である。これは最終段階をみたら判るが、酸性条件下ではアミドの加水分解で生じたアンモニアはアンモニウムイオンとなってしまい、求核性を失う。塩基性条件下では加水分解で生じたカルボン酸がカルボキシラートとなってしまい求核攻撃を受けにくくなる。
酸触媒
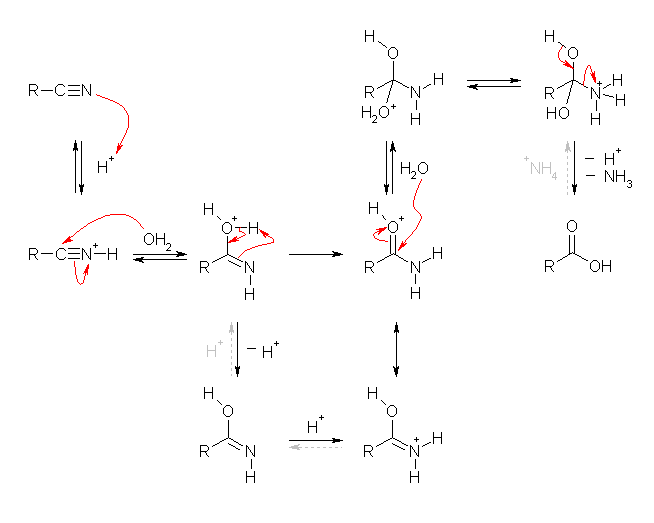
塩基触媒
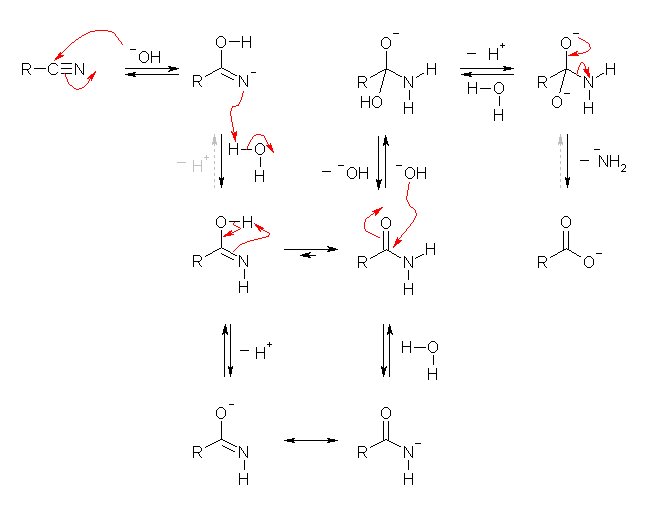
21.25
第6版の 20.12 と同じ問題である。
(a), (b) (第5版では (a) と (c)) は、ケトンを生じる。(第5版の (b) ではアルデヒドを生じる。)教科書 20.9 節(第5版では、教科書 21.8 節)を参照すること。
ニトリルは、グリニヤル試薬との反応でケトンに変換することができる。非対称なケトンである (b) (第5版では (c))は、反応に2通りの原料およびグリニヤル試薬の組み合わせが考えられる。
ニトリルは、LiAlH4 のようなヒドリド試薬で還元すると、第1級アミンを与える。これは、シアノ基に対するヒドリド H- の求核付加反応である。
シアノ基に対してヒドリド H- の求核付加がおこると、シアノ基に対するグリニヤル試薬の求核付加で生じるのと同じ、イミンアニオン中間体を生成する。イミンアニオンを加水分解するとカルボニル化合物を生成するのだが、LiAlH4 を用いた場合では、ヒドリドによる第2段階目の求核攻撃も起こり、第1級アミンまで還元されるのである。(以下、第5版のみの記述。)より弱い還元剤である DIBAH (DiIsobutyl Alminum Hydride) を用い、極低温(-78℃など)で反応を行うと、ヒドリドの第2の付加は起こらず、水を付加させることによりイミン中間体をアルデヒドに加水分解することができる。これは、エステルの DIBAH によるアルデヒドへの還元(教科書 21.6 節:第5版、第6版とも)と類似の反応である。
(解答例)
(a) propanenitrile に、ethylmagnesium bromide を作用させる。生じるイミンアニオン中間体を加水分解すると、3-pentanone を得る。
(b) 2通りの合成ルートが考えられる。(第5版 (c)) benzonitrile と methylmagunesium bromide を作用させる。または、acetonitrile に phenylmagnesium bromide を作用させる。生じるイミンアニオン中間体を加水分解すると acetophenone を得る。
第5版 (b) 2-methylpropanal
2-methylpropanenitrile を、DIBAH (DiIsobutyl Alminum Hydride) を用い、極低温(-78℃など)で反応させる。生じたイミンアニオン中間体を加水分解すると 2-methylpropanal を得る。
21.26
第6版の 20.13 と同じ問題である。
ハロゲン化アルキルは、グリニヤル試薬にすることができる。ニトリルとグリニヤル試薬からカルボニル化合物をつくることが可能である。前問を参照のこと。
(解答例)
2通りの合成ルートを考えることができる。その1。benzylbromide をグリニヤル試薬にした後、propanenitrile に作用させ、加水分解する。その2。benzylbromide を NaCN で処理して phenylacetonitrile とし、これに対し ethylmagnesium bromide を作用させ、加水分解する。
21.23, 27
(a) アルコールを塩基で処理すると、求核性の高いアルコキシドが生じる。
(b) Fischer エステル合成の反応条件である。
(c) 酸塩化物のアミノリシスである。
(解答例)
(a) アルコキシドが求核種としてはたらき、臭化アルキルの臭素の結合した炭素上で求核置換反応する。RO- + BrR' → ROR' + Br- の反応式で考える。アルコールからアルコキシドを生じさせるために、水酸基に対して等モル当量の塩基が必要である。(触媒ではない。)
同じ反応ではあるが、ROH + BrR' → ROR' + HBr と書いてもよい。ただし、実際には中性のアルコール分子はハロゲン化アルキルに対して求核置換していくほど求核性は高くない。
ポリマー: Br(CH2CH2CH2OCH2CH2CH2O)nH
ただし、黒字の部分が 1,3-dibromopropane 由来の部分。
(b) Fischer エステル合成は、プロトン化をうけたカルボン酸 ( -C+(OH)2 ) に対するアルコール水酸基の求核付加に始まる一連の反応である。
ポリマー: H(OCH2CH2OC(=O)CH2CH2CH2CH2CH2CH2C(=O))nOH
ただし、黒字の部分が ethylene glycol (1,2-ethanediol) 由来の部分。
(c) 酸塩化物のアミノリシスではアミドを生じる。また、生じるアミド結合1つにつき塩酸1分子を生じるから、これをトラップするのに塩基(酸塩化物に対して等モル当量)が必要である。
この反応で生じるのは、ナイロン 66 である。
ポリマー: H(NHCH2CH2CH2CH2CH2CH2NHC(=O)CH2CH2CH2CH2C(=O))nOH
ただし、黒字の部分が hexamethylenediamine (1,6-diaminohexane) 由来の部分。
21.24, 28
同じポリアミド樹脂であるナイロン 66 の構造式等を参照すること。
(解答例)
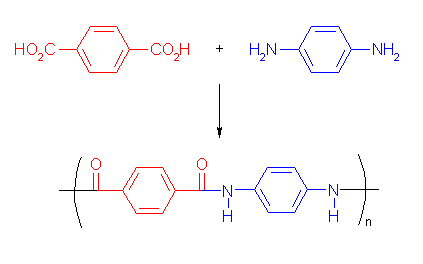
21.25, 29
ジカルボン酸とジアミンから生じるポリアミドや、ジカルボン酸とジオールから生じるポリエステルは、ナイロン 66 やケブラー、ポリエチレンテレフタラート (PET) などのように直線状に伸びた構造をもつ。
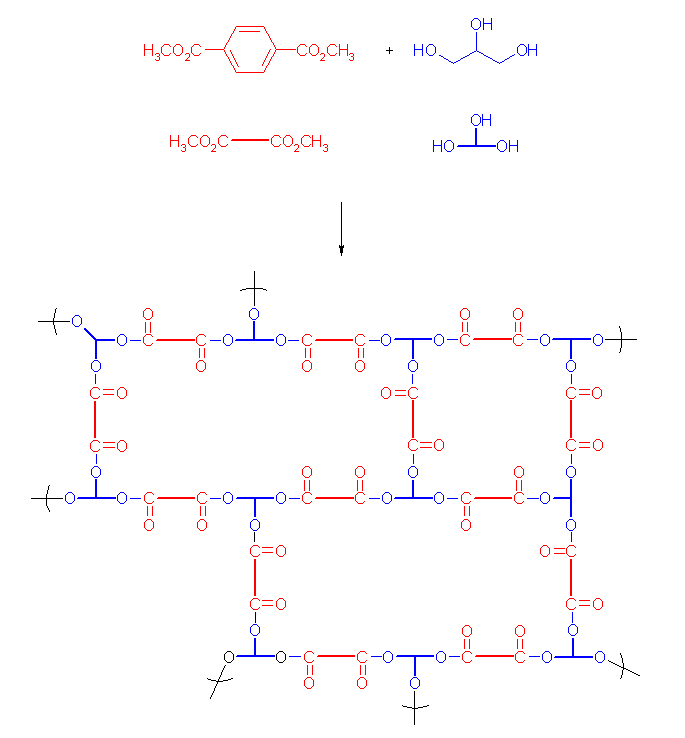
カルボン酸エステルとアルコールからのエステル交換の反応は、形式的にはエステルのアルコーリシスである。酸触媒存在下、カルボン酸とエステルは互いに可逆であったことを思い出すこと。同じ反応機構でエステルと別のエステルとの間の可逆的な変換も可能となる。2種のエステルが平衡にあるとき、メタノールのように沸点の低いアルコールが系外に除かれてしまうと、平衡移動の原理(ル・シャトリエの原理)により、メチルエステルからグリセロール(のような高沸点アルコール)のエステル側に平衡を移すことが可能である。
(解答例)
ジカルボン酸とトリオールを3対2で縮合させると、次の図に模式的に示したように直線とはならず、分岐する。その分岐から網目構造を形成する。図では二次元的な網目のように描いているが、3次元的にひろがったネットワーク状になる。(模式図では分子を直線的に描いているが、おそらく実際の形はもっと不規則であると予測される。)
このような網目構造をとることによって、ポリマーはより硬いものとなると予想される。(金網のようにワイアを編込んだものと、その金網の材料となっているワイアを束ねただけのものをイメージしてみること。)
(21.26-21.27 (第5版 21.30-31)は、分光学の問題なので省略しました。)
21.28, 32
命名にあたって、かならず構造式を書いてみること。青→窒素、赤→酸素。(a), (b) ともにカルボン酸誘導体として命名する。
(解答例)
あたえられた図を構造式に書き直すと次の通り。
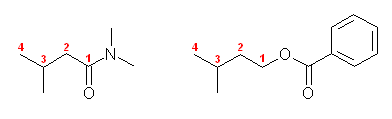
(a) N,N-dimethyl-3-methylbutanamide
(b) 3-methylbutyl benzoate
21.29, 33
(a), (b) の構造式は次のようになっている。
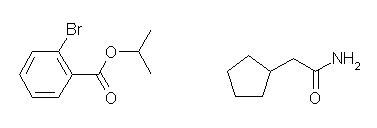
(a) isopropyl 2-bromobenzoate
(b) cyclopentylacetamide
(解答例)
(a) エステルは Fischer 法、または酸ハロゲン化物や酸無水物のアルコーリシスで合成が可能である。イソプロピルエステルを Fischer 法で合成するためには、第2級のアルコールであるイソプロパノールを必要とする。第2級アルコールでは立体的な要因のため反応が遅くなるからもともと反応の速い酸ハロゲン化物のアルコーリシスの方が好ましいと考えられる。問題 21.11 のヒントおよび解答例を参照すること。(なお、Fischer 法も誤りではない。2-bromopropane に対して 2-bromobenzoate による求核置換でも可。)
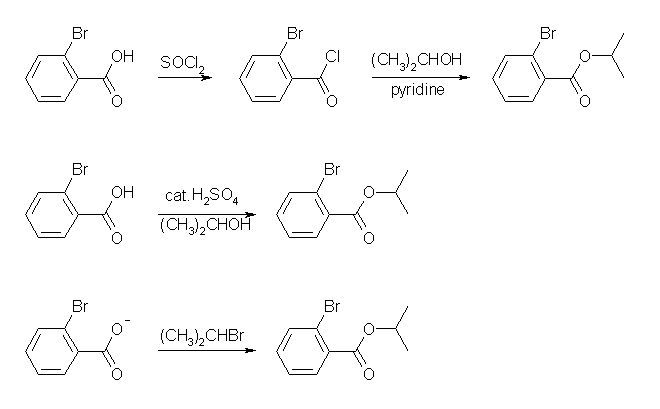
(b) 酸アミドは、エステル、酸無水物や酸ハロゲン化物のアミノリシスで合成が可能である。
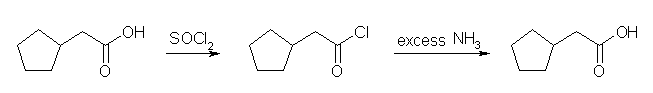
21.30, 34
4面体中間体の構造は次のようである。
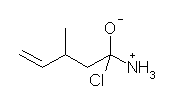
窒素が中性のアミノ基ではないことに注意すること。
(解答例)
4面体アルコキシドイオン中間体の中心炭素にはアルキル基、酸素のほかに、塩素と窒素が結合しているから、まず、酸ハロゲン化物に対する求核付加を考えると、NH3 と NH2- の2種の求核種が考慮すべき候補となる。アンモニアによる反応は一般的な酸塩化物のアミノリシスであり、示されている構造の中間体を与える。アミドイオンによる反応では、中間体の中心炭素に結合した窒素はアンモニオ基 -NH3+ ではなくアミノ基 -NH2 となるはずである。なお、求核種としてのこれらアミンまたはアミドイオンは、プロトンと共存させることは難しい。(求核種はルイス塩基でもあるから。)
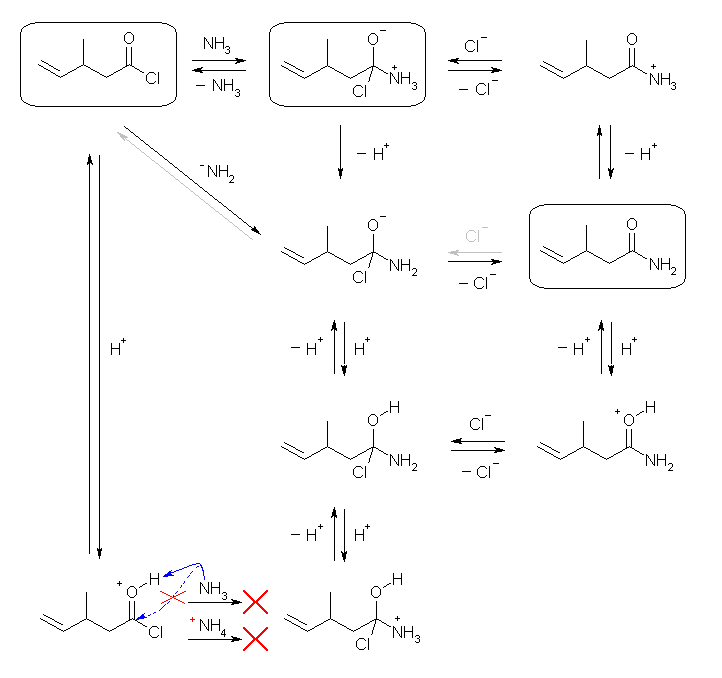
酸アミドに塩化物イオンが反応してこの中間体を形成することはない。これは、まず、酸アミドのカルボニル基は、孤立電子をもち共鳴的に電子を与える窒素と結合しているから求核攻撃をうけにくく(教科書、図21.2 などを参照し、カルボン酸誘導体の求核アシル置換反応の反応しやすさの順序を思い出すこと)、さらに塩化物イオンは求核性が小さいためである。
また、仮にこの反応が生じたとしても、この反応で生じることのできる中間体(酸塩化物にアミドイオンが求核付加したものと同じ構造)は、分子内にアミノ基(pKb は一般に5前後)より塩基性の高いアルコキシドを持っているから、アミノ基に対する選択的なプロトン化により問題文に図で与えられているような中間体を生成することは難しい。
出発物は 3-methyl-4-pentenoyl chloride
生成物は 3-methyl-7-methylpentanamide
求核試薬はアンモニア。脱離基は塩化物イオン Cl+
21.31-21.40 (35-49)
21.31
「求核」アシル置換反応は、正の(部分)電荷をもつ位置に対しておきる。従って、より大きく正に分極している方が反応性が高い。
(解答例)
静電ポテンシャルマップでカルボニル炭素上の電子密度がより低い(色としてはより青い)方が求核アシル置換反応に対して活性が高い。
もとよりカルボニル基は分極が大きい。このカルボニル炭素への結合のグループが電子供与的(孤立電子対をもつ窒素や酸素)である酸アミドやエステルは、そうではないもの(アルキル基や水素をもつケトン、アルデヒド)に比べて求核反応に対する活性は低い。ヒドリド還元でアルデヒドやケトンは NaBH4 で還元することができたのに対し、エステルやアミドの還元には LiAlH4 が必要であったことなどを思い出すこと。
アジド基は下に示すような共鳴で表される。共鳴構造式は実在する構造を表すものではないから、共鳴構造式だけをみて実在の分子の電荷密度を議論することはできない(その目的のために静電ポテンシャルマップを表す)のだが、アミノ基 -NH2 よりもアシルアミノ基 -NHCOR の方が弱い電子供与性であるように、同じ窒素でもそこに電子吸引性置換基が結合することにより電子供与性は小さくなる。(正の形式電荷を持つ窒素は電子吸引性である。)
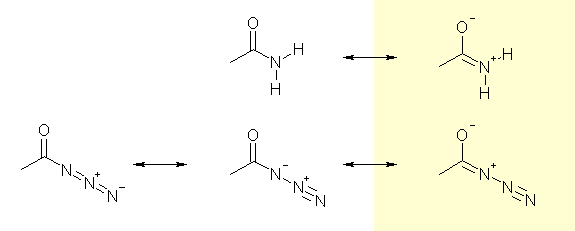
上図、背景に色を重ねた部分が孤立電子対からカルボニルへの電子供与がおきていることを表す共鳴構造になる。アミドではこれが2つのうち1つであるのに対し、酸アジドではこれが3つのうち1つで、電子供与の寄与が小さいと読むこともできる。
21.32, 35
(d) などは、フェニル基のない部分を主鎖として命名する。
(c) ジカルボン酸のエステルとして命名する。
(f) において、カルボン酸誘導体やニトリルはシクロアルケンの二重結合に優先して1位の番号がふられる。
(解答例)
(a) 4-methylbenzenecarboxamide, or 4-methylbenzamide
第6版:(b) 4-ethylhex-2-enoyl chloride
(c) dimethyl butanedioate, or dimethyl succinate
(d) isopropyl 3-phenylpropanoate, or isopropyl 3-phenylpropionate
(e) N-methyl-3-bromobutanamide
第6版:(f) methyl cyclopent-1-enecarboxylate
(g) phenyl benzenecarboxylate, or phenyl benzoate
(h) benzencarboxylic 2-methylpropanoic anhydride, or benzoic 2-methylpropionic anhydride
第5版:
(b) 4-ethylhex-2-enenitrile
(f) 1-cyclopentenecarbonitrile
21.33, 36
名前より、主鎖と側鎖の構造を読み取ればよい。
(解答例)
(a) p-bromophenylacetamide
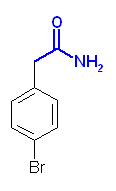
第6版: (b) m-benzoylbenzamide
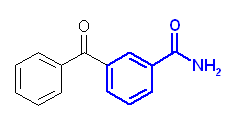
第5版: (b) m-benzoylbenzonitrile
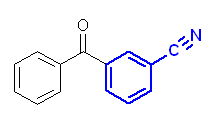
(c) 2,2-dimethylhexanamide
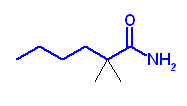
(d) cyclohexyl cyclohexanecarboxylate
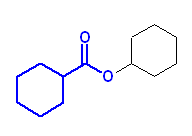
第6版: (e) ethyl cyclobut-2-enecarboxylate
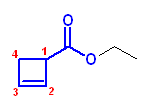
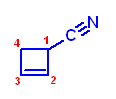
第5版: (e) cyclobut-2-enecarbonitrile
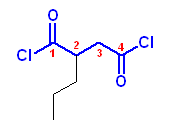
(f) 2-propylbutanedioyl chloride
21.34, 37
まず、分子式より不飽和度を計算し、分子内にある二重結合や環構造の数を調べること。
該当する条件の内で相当複雑な分子を書くこともでき、それぞれに名前のつけ方があるが、まずは単純な構造で自分で名前の付けられるものを書くとよい。
(c) は、第5版のみの問い。第6版で学習している場合も同様に解いてみるとよい。C5H7N の分子式を持つニトリルを示す。
(解答例)
(a) C6H9ClO の不飽和度は2。
酸塩化物の部分以外に環構造を持つもの (主鎖部分の見極めに気をつけること)
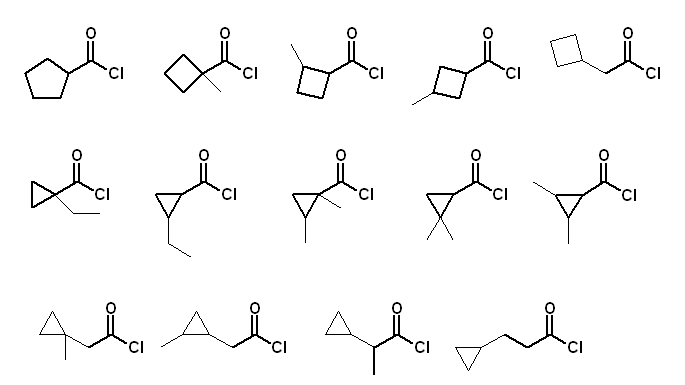
(上段、左より) cyclopentanecarbonyl chloride, 1-methylcyclobtanecarbonyl chloride, 2-methylcyclobtanecarbonyl chloride, 3-methylcyclobtanecarbonyl chloride, cyclobutylacetyl chloride
(中段、左より) 1-ethylcyclopropanecarbonyl chloride, 2-ethylcyclopropanecarbonyl chloride, 1,2-dimethylcyclopropanecarbonyl chloride, 2,2-dimethylcyclopropanecarbonyl chloride, 2,3-dimethylcyclopropanecarbonyl chloride
(下段、左より) (1-methylcyclopropyl)acetyl chloride, (2-methylcyclopropyl)acetyl chloride, 1-cyclopropylpropionyl chloride (or, 1-cyclopropylpropanoyl chloride), 2-cyclopropylpropionyl chloride (or, 2-cyclopropylpropanoyl chloride)
酸塩化物の部分以外に二重結合をもつもの (一部のみ示す)
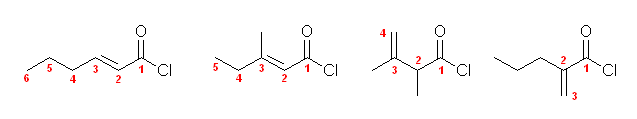
(左より) (E)-hex-2-enoyl chloride, (E)-3-methylpent-2-enoyl chloride, 2,3-dimethylbut-3-enoyl chloride, 2-propylprop-2-enoyl chloride
(b) C7H11NO の不飽和度は3。
酸アミド部分以外に環構造を2つ持つもの (一部のみ示す)
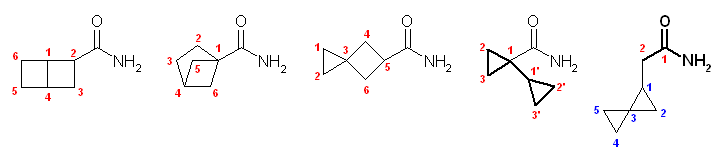
(左より)bicyclo[2.2.0]hexane-2-carboxamide, bicyclo[2.1.1]hexane-1-carboxamide, spiro[2.3]hexane-5-carboxamide, bicyclopropyl-1-carboxamide, 2-(spiro[2.2]pent-1-yl)acetamide
アミド窒素上に置換基がつくものや、環状アミドも可能である。
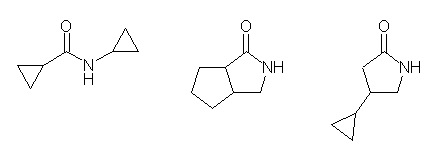
(左より)N-cyclopropylcyclopropanecarboxamide, hexahydrocyclopenta[c]pyrrol-1-one, 4-cyclopropylpyrrolidin-2-one
酸アミド部分以外に環構造を1つ持つもの (一部のみ示す)
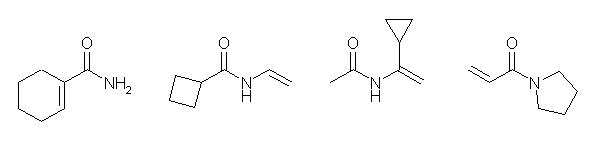
(左より)cyclohex-1-enecarboxamide, N-vinylcyclobutanecarboxamide, N-(1-cyclopropylvinyl)acetamide, 1-(pyrrolidin-1-yl)propenone
酸アミド部分以外に環構造は持たず二重結合を2つもつもの、三重結合を1つもつもの(一部のみ示す)
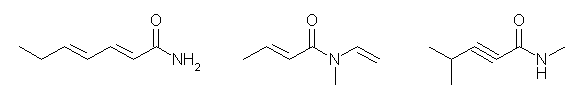
(左より)(2E,4E)-hepta-2,4-dienamide, (E)-N-methyl-N-vinylbut-2-enamide, N-methyl-4-methylpent-2-ynamide
(c) C5H7N の不飽和度は3。ただし、シアノ基中に三重結合がある。
シアノ基以外に環構造を持つもの
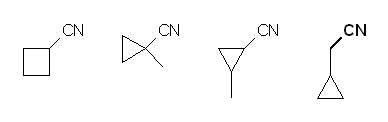
(左より) cyclobutanecarbonitrile, 1-methylcyclopropanecarbonitrile, 2-methylcyclopropanecarbonitrile, cyclopropylacetonitrile
シアノ基以外に二重結合をもつもの
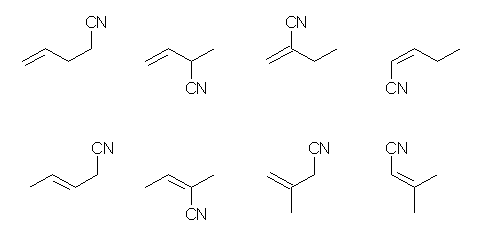
(上段左より) pent-4-enenitrile, 2-methylbut-3-enenitrile, 2-ethylpropenenitrile, (Z)-pent-2-enenitrile
(下段左より) (E)-pent-3-enenitrile, (Z)-2-methylbut-2-enenitrile, 3-methylbut-3-enenitrile, 3-methylbut-2-enenitrile
21.35, 43
まず、出発原料であるブタン酸と、各項目で問うている目的化合物の構造式を書いてみること。その上で、どこがどのように変化する反応かを見出し、関連しそうな反応を探すこと。
1段階で合成できないものもある。直接変換できそうにない場合には逆合成で考えること。
(解答例)
(a) R-CO2H → R-CH2OH の還元反応だから、ボラン BH3 を用いる。LiAlH4 を用いたヒドリド還元でもよい。
(b) R-CO2H → R-CHO の反応。カルボン酸を直接アルデヒドに還元するより、2段階で合成することを考える。
過程1:(a) で得た第1級アルコール R-CH2OH を PCC 酸化により目的のアルデヒドを得ることができる。
過程2:カルボン酸を塩化チオニル SOCl2 で処理し、酸塩化物 R-COCl にした後、-78℃で1モル当量の DIBAH を用いて部分還元することによっても目的のアルデヒドを得ることができる。
(c) R-CO2H → R-CH2Br の反応。直接の変換はできない。(a) で得たアルコールを PBr3 で処理すればよい。
(d) 炭素数が1つ増えたニトリルを合成したいのだからシアン化物イオン CN- を用いることができるような条件を考える。(c) で得た第1級のハロゲン化アルキルに対し、NaCN を作用させる。R-CH2Br → R-CH2CN
(e) 二重結合は脱離反応で合成が可能である。R-CH2CH2Br → R-CH=CH2 の脱離には、EtONa / EtOH のような強塩基の条件が必要である。第1級のアルコールは酸処理で脱離させることは難しい。また、二重結合は、酸性条件では H+ が付加、脱離することで二重結合の転位することが可能であるが、ここで目的としているアルケンは末端のアルケンだから、2-butene のような内部アルケンより(二重結合に置換しているアルキル基の数が少ないから)やや不安定であるから、その意味でも好ましくない。
(f) ペンタンニトリルを加水分解して得られる対応するカルボン酸から合成することが可能である。
塩化チオニルで処理して酸塩化物としたのち R-CO2H → R-COCl 、ひき続いてメチルアミンを用いてアミノリシスする。R-COCl → R-CO-NHCH3
(g) 2つの部分のカップリングによるケトンはいくつかの方法で合成できる。
酸塩化物とギルマン試薬の組み合わせ:教科書 10.9, 19.2, 21.4 節参照。
CH3COCl + (n-C4H9)2CuLi。反応条件は、エーテル中、-78℃で行う。
ギルマン試薬 (n-C4H9)2CuLi は (c) で得た 1-ブロモエタンをリチウム試薬に変換 n-C4H9Br → n-C4H9Li したのちに一価の銅塩を加えることで得ることができる。また、ペンタンニトリルを加水分解してえられるカルボン酸を塩化チオニルで処理して得られる n-C4H9COCl と (CH3)2CuLi の反応でもよい。
ニトリルとグリニヤル試薬の組み合わせ:教科書 教科書 20.9 節(第5版 21.8 節)を参照。
CH3CN + n-C4H9MgBr または、n-C4H9CN + CH3MgBr。グリニヤル試薬はハロゲン化アルキルと金属マグネシウムの処理で得る。ペンタンニトリルは (d) で得ている。
アルデヒドとグリニヤル試薬の組み合わせで得られる第2級のアルコールの酸化:教科書 19.8 節参照。
CH3CHO + n-C4H9MgBr → CH3CH(OH)C4H9 → CH3C(=O)C4H9。酸化条件には PCC などが使える。または、n-C4H9CHO + CH3MgBr でも同じ第2級アルコールを与える。このペンタナールは、ペンタンニトリルの DIBAH 還元などで得られる。ペンタン酸 → ペンタノール → ペンタナールでもよい。
アルキンの水和でもケトンを合成することができる。教科書 8 章参照。
HC≡CH → HC≡CLi, HC≡CLi + n-C4H9Br → HC≡C-C4H9。この末端アルキンは、硫酸水銀触媒で(マルコフニコフ配向性で)水和して得られるビニルアルコール CH2=C(OH)C4H9 は、ケト-エノール互変異性化して目的のケトンを与える。
また、アセト酢酸エステル合成については、教科書 22.8 節で学習する。
(h) ハロゲン化アリールとギルマン試薬のカップリングを用いることができる。教科書 10.9 節参照。
PhI + (n-C4H9)2CuLi
Friedel-Crafts のアルキル化反応では直鎖のアルキル基を導入することができない。まずアシル化したのち、カルボニル基をメチレンまで還元する手法をとる必要がある。
PhH + n-C3H7COCl → PhC(=O)C3H7。このカルボニル基は、Wolff-Kishner 反応(H2NNH2, KOH, ROH)などでメチレンまで還元できる。
Friedel-Crafts のアシル化で得られるのと同じ芳香族ケトンは、(g) と同様の手法で合成することができる。
21.36
思い出せない反応があれば、20章、21章の章末の「反応のまとめ」を参照すること。
(解答例)
青色で示したのが求核種。緑色の部分が脱離基である。
(a) 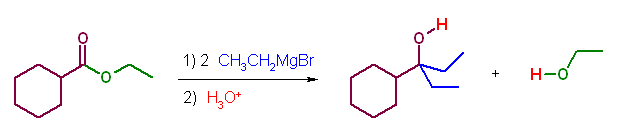
(b) 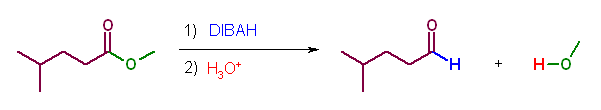
(c) 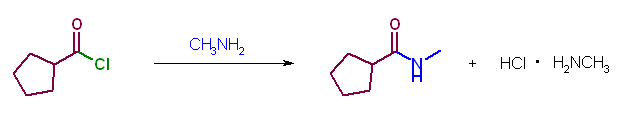
(d) 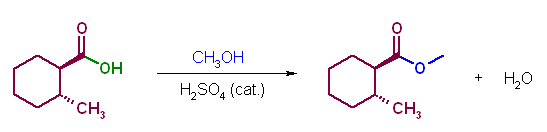
(e) 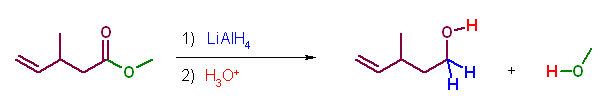
(f) 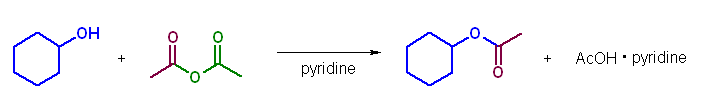
(g) 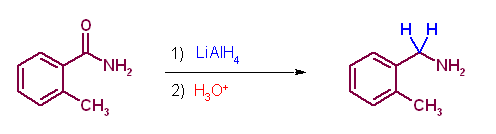
(h) 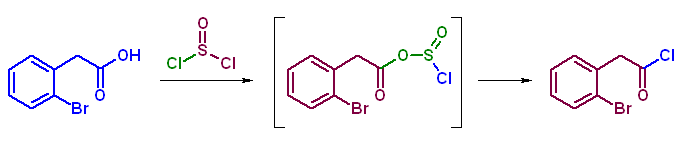
21.37, 47
21.37-39 は、いずれも同様のカルボニル求核置換反応である。基質が酸塩化物、エステル、酸アミドと変化していったときにどのようなことがおきるかを比較しておくこと。
(解答例)
(a) Gilmann 試薬は、酸塩化物などとカップリング反応する。
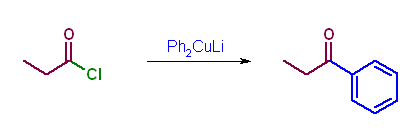
(b) LiAlH4 によるヒドリド還元。
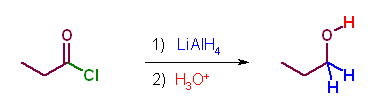
(c) Grignard 試薬は、カルボアニオンと等価で求核種として働く。系中で生じるケトンが更に求核反応を受けるため、2モル当量の試薬が反応する。
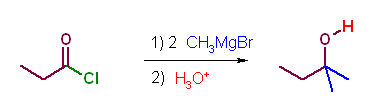
第5版(d) LiAlH(O-t-Bu)3 (LTBA) を用いると、DIBALH と同じように、低温で酸塩化物の部分還元をすることができる。ただし、低温ではエステルとは反応しない。
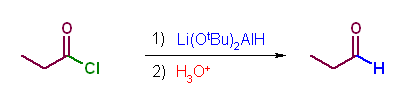
第5版(e)、第6版(d) H3O+ の条件は、加水分解を表している。
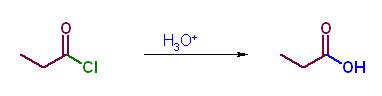
第5版(f)、第6版(e) アルコーリシスでエステルを与える。
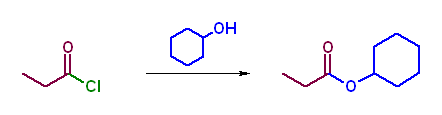
第5版(g)、第6版(f) アニリンは芳香族アミンなので、アミノリシスである。
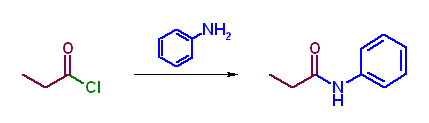
第5版(h)、第6版(g) カルボキシラートの求核攻撃がおきれば酸無水物となる。塩化物イオンの方がカルボキシラートより脱離しやすいから、酸ハロゲン化物から酸無水物を得ることができる。
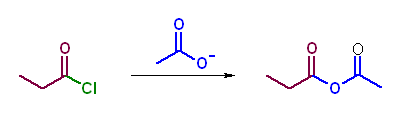
21.38, 48
21.37-39 は、いずれも同様のカルボニル求核置換反応である。
(解答例)
(a) Gilmann 試薬は、有機金属試薬であるが、求核性は小さく、ケトンやエステルとは反応しない。
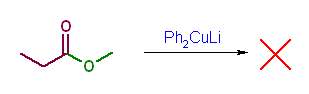
(b) LiAlH4 によるヒドリド還元。
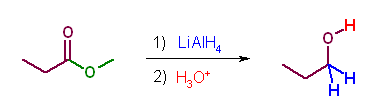
(c) Grignard 試薬は、カルボアニオンと等価で求核種として働く。系中で生じるケトンが更に求核反応を受けるため、2モル当量の試薬が反応する。
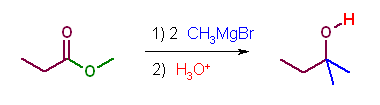
第5版 (d) LiAlH(O-t-Bu)3 (LTBA) は、DIBALH より反応性が低いから、低温では、酸塩化物の部分還元をすることができるがエステルはしない。
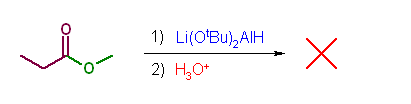
第5版 (e)、第6版(d) H3O+ の条件は、加水分解を表している。
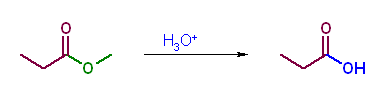
第5版(f)、第6版(e) エステルのアルコーリシスは生じない。酸触媒存在下では、可逆なのでエステル交換の平衡になる。またアルコキシドによる求核攻撃でもエステル交換は可能である。
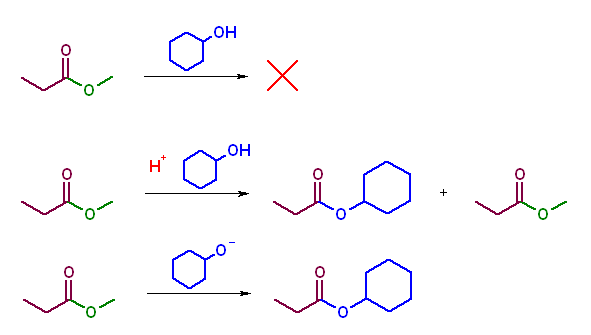
第5版(g)、第6版(f) アニリンは芳香族アミンなので、アミノリシスである。
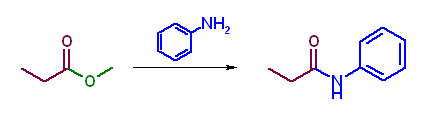
第5版(h)、第6版(g) カルボキシラートの求核攻撃がおきれば酸無水物となる。アルコキシドの方がカルボキシラートより脱離しにくいから、エステルから酸無水物を得ることはできない。
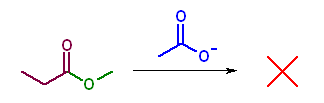
21.39, 49
21.37-39 は、いずれも同様のカルボニル求核置換反応である。
なお、第5版ではプロパンアミドだけではなく、プロパンニトリルに対する反応をも問うている。第6版での学習においても、同様に考えてみること。
(解答例)
(a) Gilmann 試薬は、反応しない。
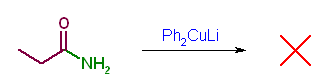
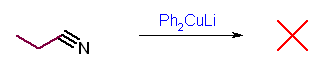
(b) LiAlH4 によるヒドリド還元では窒素は脱離しない。アミンを与える。
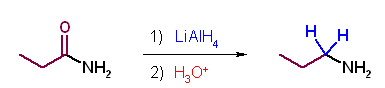
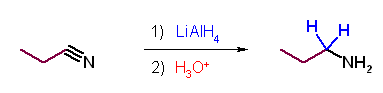
(c) Grignard 試薬に対しては、アミド水素が酸としてはたらく。
また、ニトリルは酸性水素を持たない。Grignard 試薬はシアノ基に求核付加してイミンアニオンを与える。このイミンアニオンが加水分解されるとケトンとなる。エステルと Grignard 試薬の反応とは異なり、系中ではケトンを与えず、加水分解を受けてはじめてケトンとなるから、このケトンは Grignard 試薬とは反応しない。
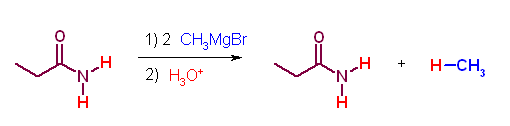
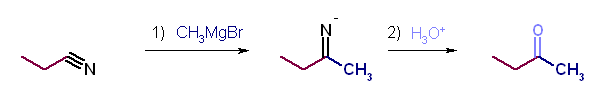
第5版 (d) LiAlH(O-t-Bu)3 (LTBA) は、第3級のアミドとは、反応してアルデヒドを与える。第3級以外のアミドとの反応は…、あとで調べます。
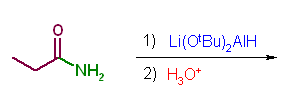
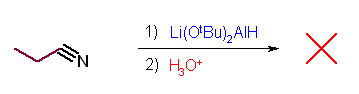
第5版 (e)、第6版(d) 酸性の加水分解でカルボン酸を与える。塩基性でも加水分解は進行する。
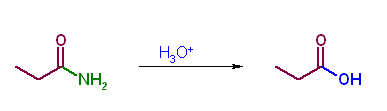
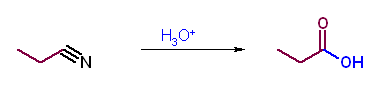
第5版(f)、第6版(e) アミドやニトリルのアルコーリシスは生じない。
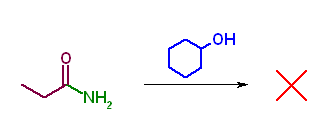
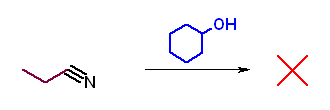
第5版(g)、第6版(f) アミドやニトリルのアミノリシスは生じない。
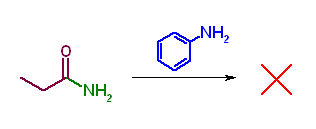
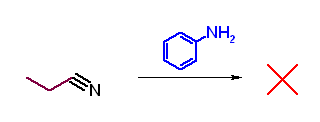
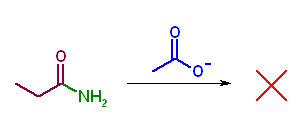
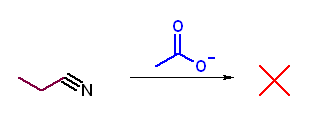
第5版(h)、第6版(g) カルボキシラートの求核攻撃がおきれば酸無水物となる。アミドから酸無水物を得ることはできない。ニトリルとも反応しない。
21.40, 44
エステルと Grignard 試薬の反応において、2回目の求核攻撃がおきる機構を思い出すこと。
(解答例)
3モルの Grignard 試薬と反応する。これは、反応の途中におけるメチルエステルからのメトキシドの脱離が2度生じるからである。
21.41-21.50 (38-55)
21.41
(a) 芳香族求電子置換反応を利用することができる。正の電荷をもつアシルカチオンが求電子種として働くと、ケトンを生じる。教科書 16.4 節参照。
(b) ハロゲン化アルキルとは異なり、ハロゲン化アリールでは求核置換反応は起きない。ハロゲン化アリールは Grignard 試薬、Gilmann 試薬などの有機金属に変換できる。これらの有機金属は、基本的に求核試薬としてはたらく。カルボン酸誘導体との反応を考える。
(c) 安息香酸などのカルボン酸は、Grignard 試薬経由で合成することができる。一般にハロゲン化アルキルからカルボン酸の合成は Grignard 試薬経由の方法以外に、シアン化物イオンによる求核置換反応でニトリルにしてから加水分解する方法がある。しかし、ハロゲン化アリールは芳香族求核置換をうけないから、ニトリルに合成するためには、逆にカルボン酸由来で酸アミドを脱水する方法をとる。
(d) ニトリルと Gilmann 試薬などの有機金属の反応を思い出すこと。
(e) スチレンのビニル基の二重結合は、Wittig 反応で合成するか、アルコールからの脱水で合成する。
(解答例)
(a) Friedel-Crafts 反応によるアシル化:CH3COCl, AlCl3 (1 mol eq.)
(b) Grignard 反応を利用した経路1:PhBr → PhMgBr → PhCO2H → PhCOCl → PhCOCH3
グリニヤル試薬に二酸化炭素を作用させ、安息香酸とし、酸塩化物に変換後、Gilmann 試薬とのカップリングにより目的とするケトンとする。
Grignard 反応を利用した経路2:PhBr → PhMgBr → PhCH(OH)CH3 → PhCOCH3
グリニヤル試薬にアセトアルデヒドを作用させ、得られるアルコールを酸化する。
Gilmann 試薬を経由する方法:PhBr → PhLi → Ph2CuLi → PhCOCH3
フェニルリチウム経由で調製した Gilmann 試薬を、塩化アセチル(CH3COCl)に作用させ、目的のケトンとする。ただし、この方法では原料の PhBr の半分(Gilmann 試薬のうち1方のフェニル基)は目的の生成物にならない。
(c) エステルとGrignard 試薬では2モル当量のGrignard 試薬が付加して、第3級のアルコールを与えるから、目的の生成物を与えるためには、エステルを加水分解し、(b) の一番上の経路に帰着させればよい。
(d) ニトリルは加水分解によりカルボン酸になるから、(c) と同様、(b) の一番上の経路に帰着させる方法もあるが、ニトリルは、Grignard 試薬1モル当量が付加してケトンを与えることを利用するのがよい。:CH3MgBr, then H3O+
(e) 二重結合は、酸化開裂により(条件により)アルデヒドやカルボン酸を与えるので、(c) と同様、(b) の一番上の経路に帰着させる方法もあるが、水和により PhCH(OH)CH3 とすれば、(b) の2番目の経路に帰着できる。:Hg(OAc)2, H2O, then NaBH4
21.42, 42
これらの置換基の中で、ニトロ基は電子吸引性がつよい。フェニル基のパラ位に結合した置換基はフェニル基を通して電子的効果を与えるから、ニトロ安息香酸エステルは、無置換の安息香酸エステルと比較したとき、カルボニル基に結合したアリール基が電子吸引性基としてはたらくことになる。このことが、水酸化物イオンによる求核アシル置換反応の速度にどのような影響を与えるかを考えればよい。
置換基ごとのもつ電子的効果については、教科書 16.5 節や、その中の図 16.10 を参照すること。
(解答例)
エステルのケン化(アルカリ性の加水分解)の反応(機構は、教科書 p831)は、水酸化物イオンがカルボニル基に求核攻撃をすることで生じる。そして、その反応中間体は水酸基が付加した正四面体型の炭素に負電荷をもつ酸素が結合した構造である(反応機構の図、上より2番目の構造)。このような中間体は、電子求引基によって安定化される。一般に、反応中間体が安定である( ~ 遷移状態のエネルギーが低い:活性化エネルギーが小さい)ような反応ほど速く進行すると予想される。
問い 20.45 や、問い 20.47 で議論したのと同様に考えると、共鳴効果を通した電子求引、および 電子供与効果は、o- 位や p- 位のカルボン酸のカルボニルの電子密度に大きな影響を持つ。
従って、o-, および p- 位にある共鳴効果を通した電子求引基は、置換安息香酸においては、その酸性度を上げ、また、置換安息香酸エステルにおいては、そのケン化の反応性を上げると予測できる。(p 815 に示された、種々のカルボン酸誘導体の間の相対的な反応性の大小に関連する議論を参照すること。)
シアノ基は、大きくわけて電子求引性基に分類される。また、アミノ基は電子供与性基に分類される。(芳香族求電子置換反応に対する置換基効果については、第16章、16.5節、表 16.1(p570)などを参照すること。)
図 16.10 を参照すると、反応性の順は、およそ以下のようになると予想される(実測すると、種々の要因により若干の入れ替えがあるかも知れない)。
-NO2 > -N+R3 > -CN > -SO3H > -COCH3 > -CO2H > -CO2R > -CHO > -I > -Br > -Cl > -F > -H > -Ph > -R > -NHAc > -OR > -OH > -NH2
21.43, 38
同じ酢酸のエステルである。電子的な効果で考えるより、立体的な要因を考えること。問題 21.11 の答えも参考にすること。(ハロゲン化アルキルの置換反応において、SN2 反応が立体効果を強く受けたことを思い出すこと。)
(解答例)
この一連の化合物では、上の問い、21.42 で議論したような電子的要因にはあまり差がない。従って、電子的な効果より立体的な要因で考える。
求核攻撃の起こる位置(カルボニル炭素)の近傍での立体的な混みあいが生じると、反応が抑制される。
次図には、PM3法で構造最適化した Methyl Acetate および t-Butyl Acetate について、溶媒等の周囲の分子に対する立体効果(溶媒の近接限界:Chem3D というソフトウェアで計算したもの、ここでは溶媒のサイズのパラメータを適当に選び、0.9 としている。)を表示させたものである。
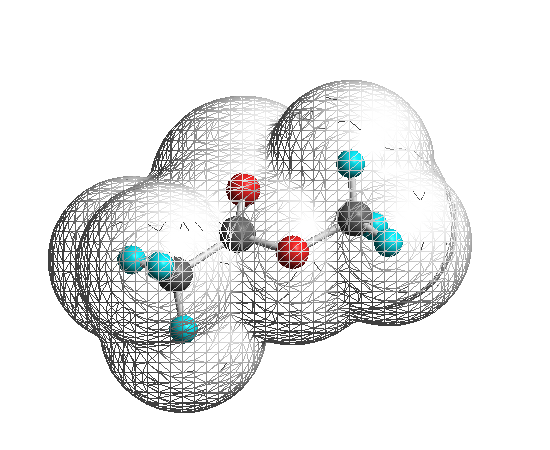
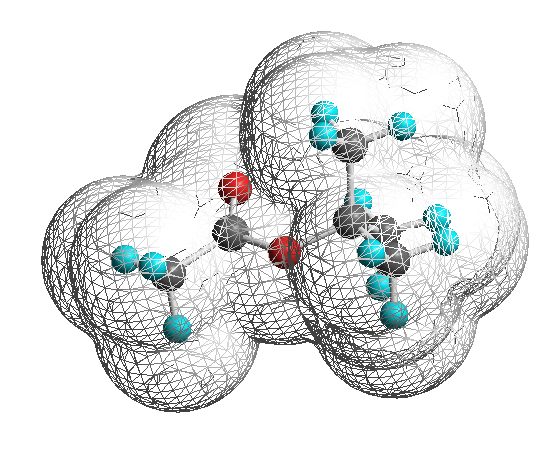
メチルエステルにくらべ、t-ブチルエステルで、カルボニルへの近接が制限されている様子が視覚的に見てとれると思う。
21.44, 39
問題 21.11 の答えも参考にすること。
2,4,6-トリメチル安息香酸 の3次元模型
(解答例)
Fischer のエステル化の反応機構は、図21.10(教科書 p832)に示されているように、カルボニル酸素がプロトン化(ルイス酸の配位)を受けたあと、カルボニル炭素に対してアルコールが求核攻撃することによりエステル化を生じる。
ここで、2,4,6-トリメチル安息香酸は、カルボキシ基の o-位のメチル基が、カルボキシ基に対して立体的に覆いかぶさるような構造を持つ。(ヒントの箇所に3次元模型へのリンクを貼ってあるのでクリックで表示させ、立体的な様子を観察すること。)これに基づき、2,4,6-トリメチル安息香酸を、カルボキシ基のカルボニル炭素(sp2混成である)の p 軌道の方向、すなわち、この部位に対しての求核攻撃が起きるべき方向から見た分子構造の表示と、同じ方向から見た、溶媒等の周囲の分子に対する立体効果(溶媒の近接限界:Chem3D というソフトウェアで計算したもの、ここでは溶媒のサイズのパラメータを適当に選び、0.9 としている。)を表示させた図を以下に示す。
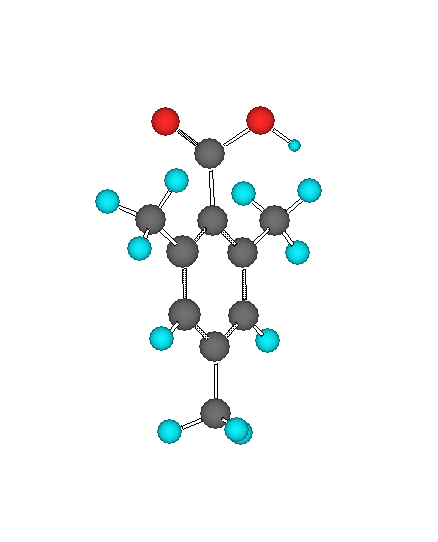
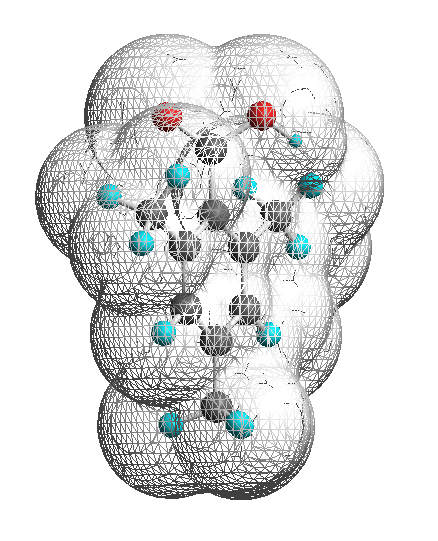
図から読み取れるように、この分子においては、カルボニルに対する攻撃は、立体的な要因のためにほとんど生じることができない。
(成功しそうな別のエステル化法)
反応位置がカルボニル炭素であるような反応は、同じ理由により生じない。カルボキシ基の酸素上で起きる反応であれば、立体障害をうけにくいために成功する可能性がある。そのような例として、たとえば次の反応が考えられる。
R-CO2- + CH3Br → R-CO2CH2 + Br-
これは、カルボキシラートの酸素がハロゲン化アルキルに対して求核攻撃(SN2)する反応である。
また、ジアゾメタンとカルボン酸の反応でも、メチルエステルを生じる。これは、カルボキシ基の酸素による求核攻撃で生じる。反応機構は次の通り。
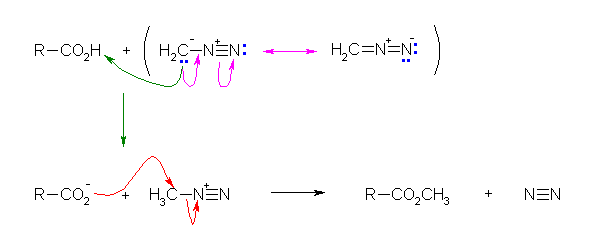
なお、ジアゾメタンによる反応(ジアゾメタンの希薄エーテル溶液を加える。生成物が目的のエステルと窒素のみで、また、未反応のジアゾメタンは沸点が低い(-24℃)ので、ワークアップは溶媒留去するのみで大丈夫。)は、非常に穏やかであるため、酸や塩基に対して不安定な基質に対して特に有効である。
(実験的な事実として、カルボニル求核置換反応でも、より反応活性の高い酸ハロゲン化物に変換すると、メタノールとの反応でエステルを与えることが知られているようである。ただし、上の議論:オルト位のメチル基による立体障害が反応を阻害する:は、Fischer のエステル化と同じはずである。)
21.45, 40
カルボン酸誘導体の加水分解の機構を思い出すこと。
(解答例)
次に示すように、溶媒である水がカルボニル基に求核付加した「オルトカルボン酸」(R-C(OH)3)を生じる平衡があると考えることにより、カルボン酸と水の間の酸素交換を説明することができる。(一般的にこの平衡定数は小さく、オルトカルボン酸の形では単離されない。)
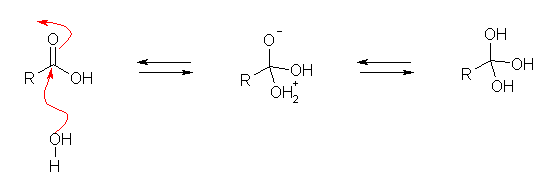
生じたオルトカルボン酸より脱水がおこればもとのカルボン酸の構造を再生するが、このとき、3つのヒドロキシ酸素のうちどの酸素が抜けるのかは区別できないため、確率的に抜けていく。その結果、溶媒中の酸素とカルボン酸の酸素は平衡になるから、大過剰の溶媒として標識酸素を持つ水を用いた場合、この標識酸素は、速やかに両方の酸素原子中に取り込まれることになる。
2つの酸素が区別されない出来ない事実のみは、次のようにも示すことができる。
カルボン酸が酸(pKa は約5前後)であるということは、[A-][H+]/[AH] = 10-5 となる程度に酸解離することを示す。
AH ←→ A- + H+
C(1-α) ←→ Cα + Cα
より、α が1にくらべて特に小さいとき、Ka = Cα2 と近似できるので、この式を使うと α を見積もることができる。いま、カルボン酸 Ka = 10-5 に対して、その全濃度 C が 0.1 mol/L になるように水に溶かしたとき、全量のうちの 1 % が解離していることになる。0.001 mol/L 程度の希薄溶液では全量のうちの 10 % 程度が解離し、これより希薄な場合は更に解離度は大きくなる。このような希薄溶液では共役塩基の形(カルボキシラート)が有意な量だけ存在しているが、次の共鳴式から判断できるように、この形において2つの酸素は区別されない。
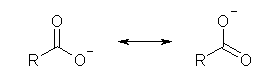
しかしながら、この説明のみでは「カルボン酸と水の間で酸素の交換が起こること」を説明できないので、この問いに対する解答としてはふさわしくない。
21.46, 45
Fischer エステル化(酸性条件下のエステルの生成反応, 図 21.10, p832)は可逆であったことを思い出すこと。
本質的には、問い 21.45 と同じ種類の質問である。
(解答例)
Fischer エステル化反応および酸性での加水分解の機構(下図の上半分)において、水分子を別のアルコール分子に置き換えてエステルと反応させることで、このエステル交換の反応機構(下図の下半分)を書くことができる。
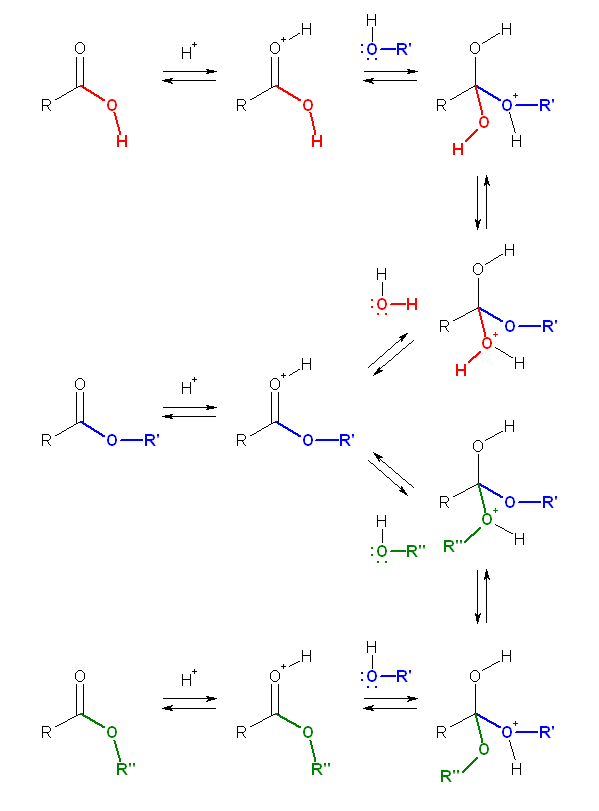
21.47, 46
NaN3 は、N3- とナトリウムイオンから生じた塩である。N3- は、塩化物イオンなどと同様に求核種としてはたらきうる。
(解答例)
N3- が求核種、塩化物イオン Cl- が脱離基。
21.48, 50
RC(=O)-O*R' → RC(=O)-OH + HO*R'
という反応でエステルが加水分解する。この逆反応で標識化されたエステルを得るためには、HO*R' という形のアルコールが必要である。
(解答例)
プロパン酸エチルは、プロパン酸とエタノールの縮合による化合物である。そのため、18O 標識を酸由来で合成するか、アルコール由来で合成するかの選択肢がでてくる。しかし、教科書 21.6 節の記述を見ると、ここでは、エステル中のカルボニル酸素は標識せずにアルコキシ基の酸素のみ標識したようなものが必要(合成したいもの)であることに注意する。
18O 標識されたエタン酸をなんらかの方法でプロパン酸に変換し、これをエチルエステル化する経路や、18O 標識されたエタン酸をエステル化したあと、なんらかの方法で酸部分の炭素鎖を伸ばす反応を行うなどによってプロパン酸エチルを合成する経路では、エステル中の2つの酸素を区別することができない。これは、カルボン酸やそのエステルを酸性で溶媒としての水やアルコールと処理すると、可逆な反応(溶媒中の酸素による求核攻撃に由来するエステル化や加水分解、または、エステル交換:21.45 や 21.46 の解説に示したのと同様の機構、または、オルトエステル R-C(OR)3 を経由した機構)により、すべての酸素が溶媒と交換されてしまう可能性があるからである。また、アルカリ性条件下でのエステル化やジアゾメタンによるエステル化も、2つの酸素はともに保持されるが、この時、カルボニル酸素とアルコキシ酸素を区別することは出来ない。
そこで、可能性があるのが、18O 標識されたエタン酸からエタノール-18O を生じさせ、プロパン酸との反応でエステル化する方法である。ただし、Fischer エステル化(酸性条件下のエステル化)により、エタノール中の 18O をエステル中に導入することが可能であるが、上述のようにカルボニル酸素も 18O と交換してしまう可能性があるので解答として適していない。そこで、プロパン酸を酸塩化物に変換したのちに、18O を含むエタノールと反応させる方法をとれば解決できる。
このエタン酸からエタノールへの還元は、ジボラン還元などが適している。
21.49, 51
脱離基の違いで考えること。
酸塩化物 RC(=O)-Cl が塩化物イオン Cl- を脱離基として持つアシル化合物(カルボン酸誘導体)であると捉えることができるのに対して、同様に酸無水物 RC(=O)-OC(=O)R を、脱離基としてカルボキシラート -OC(=O)R を持つアシル化合物(カルボン酸誘導体)であるものとして捉えたとき、その脱離したイオンの安定性、すなわち脱離しやすさは、その共役酸の酸性度と密接に関係する。
すなわち、カルボニル求核置換反応に対して、より反応活性の高い酸塩化物からの脱離基、塩化物イオンは、強酸 HCl の共役塩基であり、相対的に反応性の低い酸無水物からの脱離基、カルボキシラートは相対的には弱酸であるカルボン酸 HOC(=O)R の共役塩基である。実際、更に弱い酸であるアルコール HOR の共役塩基 -OR を脱離基として持つアシル化合物、すなわちエステル RC(=O)-OR は、酸無水物よりも更にカルボニル求核置換反応の活性が低い。
同じ酸無水物でも、脱離基となる部分の構造の異なるもの同士で比較する場合、カルボニル求核置換反応の活性に差があることが考えられる。
(解答例)
2つの脱離基、-OC(=O)CH3 と -OC(=O)CF3 とを比較すると、前者は 酢酸 CH3CO2H (pKa ~ 4.75)の共役塩基、後者はトリフルオロ酢酸 CF3CO2H (pKa ~ 0.23)の共役塩基であるから、後者の方がずっと脱離性能が高い。そのため
(a) 酸無水物の交換反応は、次図のような平衡の反応から進行するが、中間体からは -OC(=O)CF3 の脱離(赤矢印)が優先する。
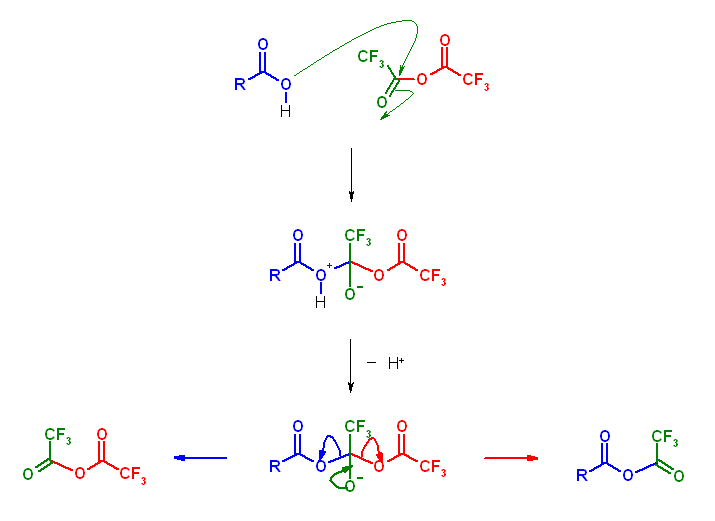
青矢印による左への反応は、原料の無水トリフルオロ酢酸を再生する経路。
(b) 上述したように、より強酸の共役塩基が脱離する(脱離後のイオンが安定である)ため。
(c) 酸無水物によるエステル化反応は、次図のような反応機構により進行するが、脱離は -OC(=O)CF3 が優先するため。
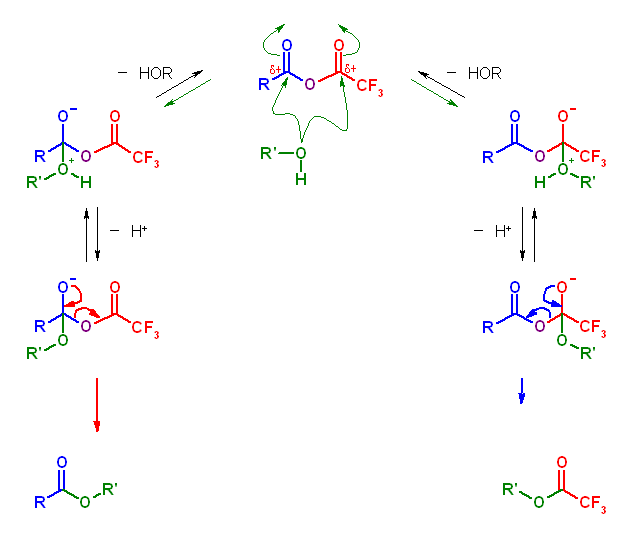
21.50, 53

で示される反応だから、炭素数が増えている。これをどのようにクリアするかで分けて考えればよい。
(解答例)
次の3類型に分けて解説する。(詳細な反応条件はそれぞれ調べること。)
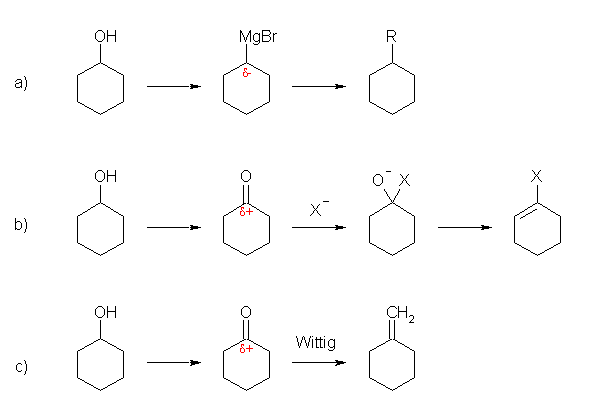
(a) まずアルコールをハロゲン化したのち、グリニヤル試薬、リチウム試薬などの有機金属にする方法。
グリニヤル試薬との反応の候補としては、二酸化炭素、ホルムアルデヒド、などがあるだろう。その他、有機金属試薬と DMF や オルトギ酸エチル HC(OEt)3 などを反応させることで、直接ホルミル化する方法もある。(ギ酸エステルとの反応では、系中でアルデヒドを生じるが更にもう1分子の有機金属試薬と反応するため、生成物として、アルデヒドを与えない。)
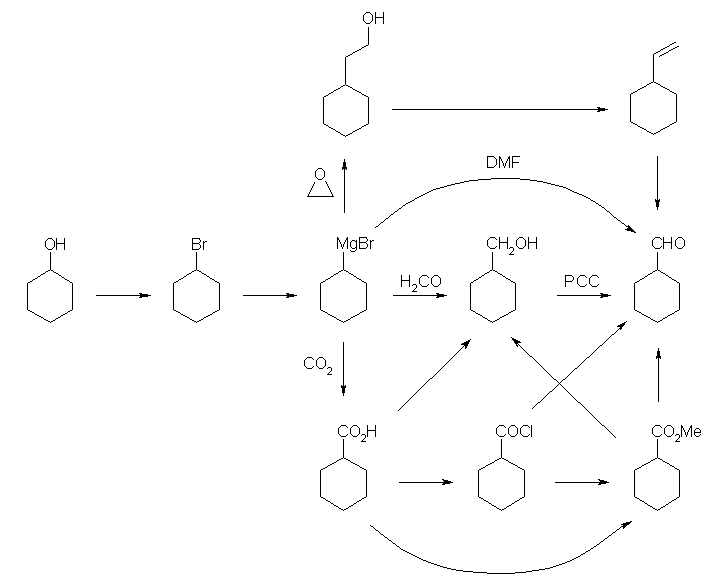
(b) シクロヘキサノンまで酸化したのち、カルボニルに対する求核攻撃を利用する方法。
求核付加により生じるアルコールは、脱水して二重結合にするときには、より多置換の(安定した)構造すなわち、シクロヘキサン環上で二重結合になっていくから、求核種の種類を選ばないと、アルデヒドにもっていくための取っ掛かりとなるような置換基を側鎖上に導入するのに苦労することになる。ひとつの可能性としては、シアン化物イオンによりシアノヒドリン形成を用いることが可能である。
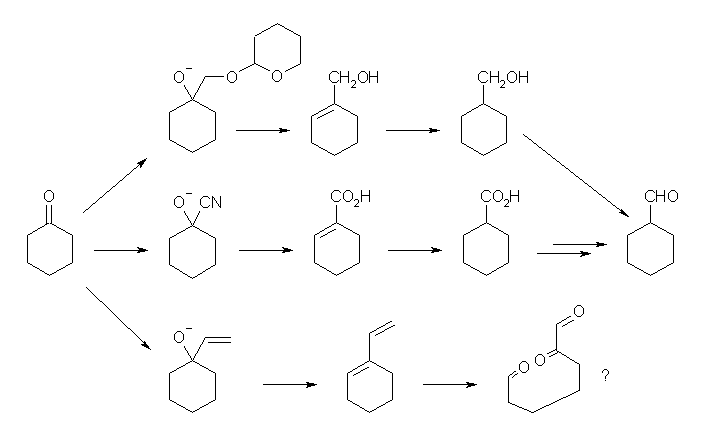
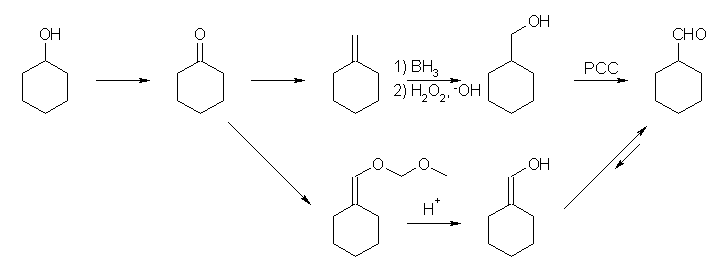
(c) (b) の変形でもあるが、Wittig 反応によりメチレンシクロヘキサンとすることができれば、ヒドロホウ素化によってシクロヘキシルメタノールとなるため、この1級アルコールを酸化して目的のアルデヒドとすることができる。また、Br-CH2-OCH3 のようなハロゲン化アルキルから得ることのできるホスホニウム塩を用いて Wittig 反応をすると、=CH-OCH3 (メトキシメチレン)を二重結合として導入することができる。このメトキシを加水分解してアルコールに変換してやるとエノール RR'=CHOH を与えるが、すみやかにケト=エノール互変異性化により、 RR'-CHO を与えるため、酸化反応を必要としない。下例では、水酸基の保護基として、メトキシ基の代わりにメトキシメトキシ基を用いている(メトキシメチルエーテル: MOM エーテル)。MOM エーテル中にはアセタール構造を有するので、通常のエーテルよりも弱い酸の条件で加水分解することが可能である。
21.41
(解答例)
21.52
(解答例)
21.54
(解答例)
21.51-21.60 (55-64)
21.51, 55
酸無水物のアミノリシスによるアミド生成の反応機構を参照すること。また、温度については、一般的に、反応温度を上げることによって進行しにくい反応でも起きるようになる。
なお、アンモニウムイオン NH4+ には、求核性はない。
(解答例)
酸無水物がルイス塩基として働き、アンモニウムイオン NH4+ よりプロトン化を受け、生じたアンモニア NH3 が求核攻撃するような反応機構を描いた。
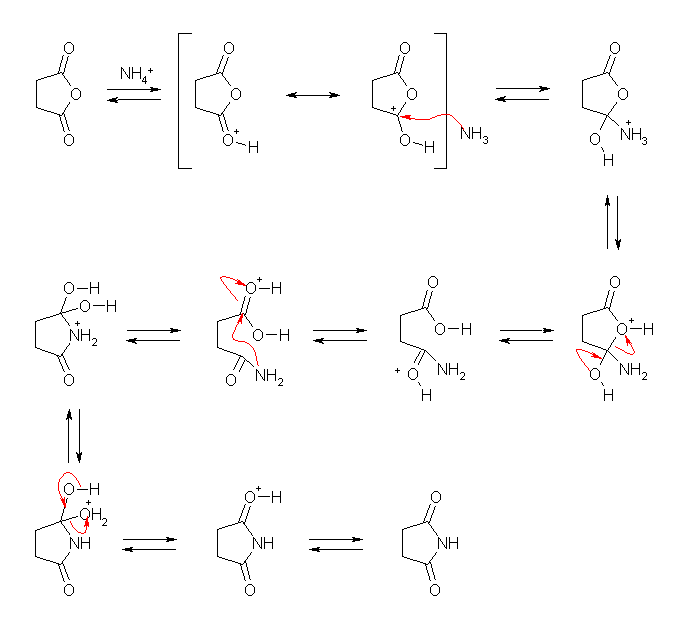
アミド窒素( -C(=O)NH2 )は、孤立電子対がカルボニルのπ系との共役により求核性が低い(アミド窒素は、塩基性も低い)ので、アミド窒素による分子内でのカルボキシ基への求核反応には、高温が必要であると考えられる。(上機構2段目、左より2番目では、プロトン化をうけたカルボキシ基への求核反応として描いてある。)
21.52, 56
ニトロ基は、アミノ基やアミン誘導体へ変換可能である。
また、p-位のエーテル基は、求電子置換反応では導入できない。芳香族求核置換反応は、π 電子密度が低い場合でのみ進行する。
(解答例)
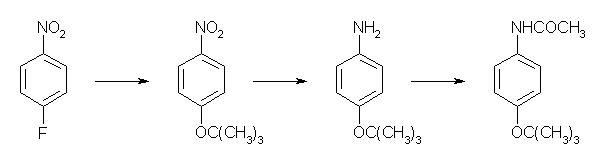
1st step:芳香族求核置換反応は、π 電子密度が低い場合でのみ進行するから、ニトロ基の変換よりも先に行う必要がある。(ニトロ基の電子求引性の効果は、o-位、p-位で大きい。)試薬には、t-ブトキシカリウムなど((CH3)3C-O- K+)を用いる。
2nd step:ニトロ基の還元。SnCl2-HCl など。
3rd step:アミンのアセチル化。AcCl など。
21.53, 57
カルボキシ基のエステル化、ニトロ基のアミンへの還元が含まれる。アミノ基には求核性があるので反応の順序に注意すること。
(解答例)
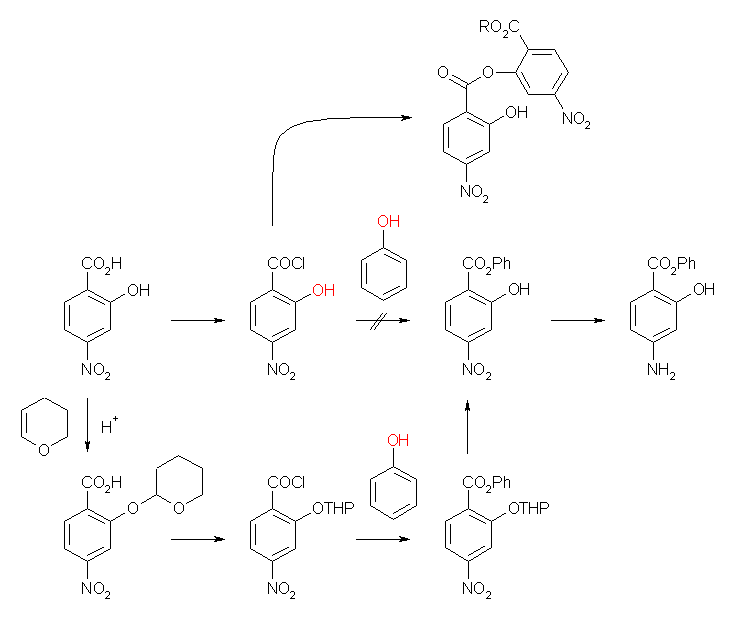
1) フェノールとカルボン酸のエステル化では、Fischer のエステル化条件は使うことができない。これは、フェノールがアルコールよりも小さな pKa を持つことからも推測されるように、フェノールの酸素はフェニル基との共役によって孤立電子対が非局在化しているため、水やアルコールに比べて求核力に乏しいからである。そのため、カルボン酸を酸塩化物に変換し、これにフェノールを作用させるなどの条件が必要である。その際に、分子内にアミノ基があると副反応が予測されるため、先にエステル化を行う必要がある。
2) ここで、「4-ニトロ-2-ヒドロキシ安息香酸塩化物とフェノールの反応」というのが、問題の解き方に示された例解なのであるが、これでは基質中の2位の水酸基も同様の反応をするため、水酸基を持つ酸塩化物を単離することはおそらく難しいであろう。そのため、水酸基になんらかの保護基が必要となるはずである。(とはいえ、分子内に(m-位なので効果は小さいが)ニトロ基、そしてカルボキシ基と電子求引性基があることで、フェノール酸素の求核性は落ちるから、反応の条件を上手にえらべば、フェノールとの反応を優先させることも可能であるかもしれない。)
3) 上の反応式では、酸触媒により DHP と反応させることで THP エーテルとした。THP エーテルは分子内にアセタール構造を有するため、酸触媒により加水分解が可能である。エステルも加水分解される可能性があるが、条件を選べば優先的に THP エーテルのみを加水分解することも可能であるかもしれない。(ここでは、それが可能なものとして示している。)
4) ニトロ基の還元には、SnCl2-HCl などを用いることができる。この条件でエステルは影響を受けない。
21.54, 58
電子求引性基を持たないから、臭素に対して、芳香族求核置換反応を行うことは不可能である。
(解答例)
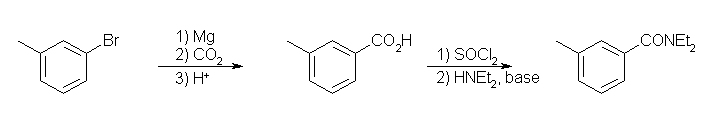
Grignard 試薬を経由してカルボン酸を合成する経路を例にして示す。
21.55, 59
メチル基をカルボキシ基に酸化することを考えた場合、シアノ基 -CN は、ヒドリド還元では -CH2NH2 に変換することが可能であるが、同条件でカルボキシ基も還元されて -CH2OH を与えてしまう。シアノ基の還元を先に行った場合、メチル基の酸化条件にベンジルアミンが同様にベンジル位で酸化を受けることが予想される。従って、メチル基をカルボキシ基にする以外に方法を考えた方が良い。
(解答例)
ルートのみ示したので反応条件は各自で調べるように。
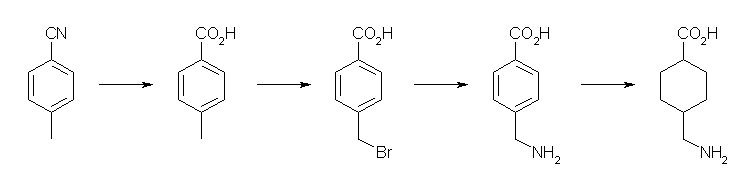
ヒントに書いた理由により、シアノ基を加水分解してカルボキシ基にしたあと、メチル基をベンジル位のハロゲン化とアミノリシスによってベンジルアミンとした。シアノ基の加水分解は、酸性または塩基性の条件下で行われるが、塩基性の加水分解を行う場合、先にハロゲン化によってブロモメチル基をもっていると加水分解されてベンジルアルコールになってしまうので注意。(その場合でも、塩化チオニルでハロゲン化し、同時に生じる酸塩化物のみを水との処理でカルボキシ基に戻すことが可能。)
21.56, 60
問い 21.44 の解説にも書いた。
(解答例)
問い 21.44 で示した反応機構の図を再掲。

ジアゾメタンの共鳴構造のうち左の極限構造式は、炭素上に負電荷があることから炭素が求核性をもち、同時に、炭素がオクテットを満たさず、従って求電子性をもつ、ということを示唆している。孤立電子対をもつので、ルイス塩基でもある。これによりプロトン化を受けて生じるメチルジアゾニウムイオンは、芳香族のジアゾ化によって生じたジアゾニウム塩が、窒素の脱離性能の高さによって、芳香族求核置換反応に対する活性が高かったのと同じように、求核置換反応(N2 を脱離基とする SN2)をうけて相手のカルボキシラートからのメチル化を容易に行う。
21.57, 61
カルボカチオンの転位においてもフェニル基は橋架け構造を経由して転位しやすかったことを思い出すこと。
(解答例)
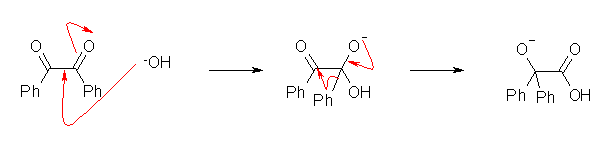
上のようにカルボニルに対する求核攻撃の結果、(カルボニル求核置換反応において、酸ハロゲン化物がハロゲン化物イオンを脱離基として放出するのと同様に、)フェニルアニオンが形式的に脱離して隣接するカルボニル基へ転位する。このときには、次図のような橋架け構造をとることができるが故に、(通常のフェニルケトンでは起きないような)フェニルアニオンの形式的な脱離が可能となると考えられる。
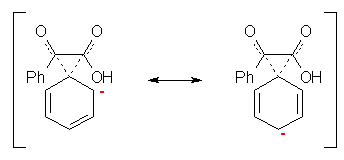
ベンジル酸転位は、脂肪族α-ジケトンにおいても同様の反応を起こすが、α位プロトンを持つ場合には、エノール化に伴う副反応のため、収率が低くなるとのこと。また、類似の反応機構を持つ転位反応に、Favorskii転位 などがある。
21.58, 62
問い 21.57 の反応機構を見て考えること。
(解答例)
2-hydroxy-2-phenylacetic acid を生じると考えられる。
反応機構において、ヒドリドが転位しても、フェニル基が転位しても生成物は同じである。
ただし、アルデヒド基のカルボニルの方が、フェニルケトンのカルボニル基に比べて、立体的にも電子的にも求核攻撃を受けやすい。
21.59, 63
アミドの加水分解の反応機構を参照し、アミンによるアミノリシス(アミドのアミン部分の交換反応)を考えてみよ。
(解答例)
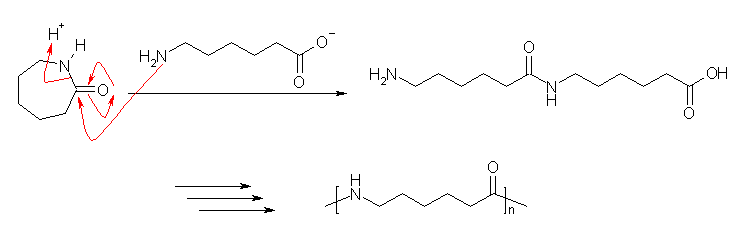
加水分解の反応機構は省略した。加水分解によって生じる 6-アミノへキサン酸のアミノ基により、アミノリシスを生じる。
21.60, 64
カッコで示されている繰り返し単位の、端の部分は一方が R-C(=O)- で、もう一方が R'-NH- である。このカッコを2つ隣合わせで書いてみると、R-C(=O)-NH-R' というアミド結合ができる。カッコの中にも、もう一箇所アミド結合があることに注目すると、最も単純な繰り返しのためのモノマー構造が見えてくる(はず)。
(解答例)
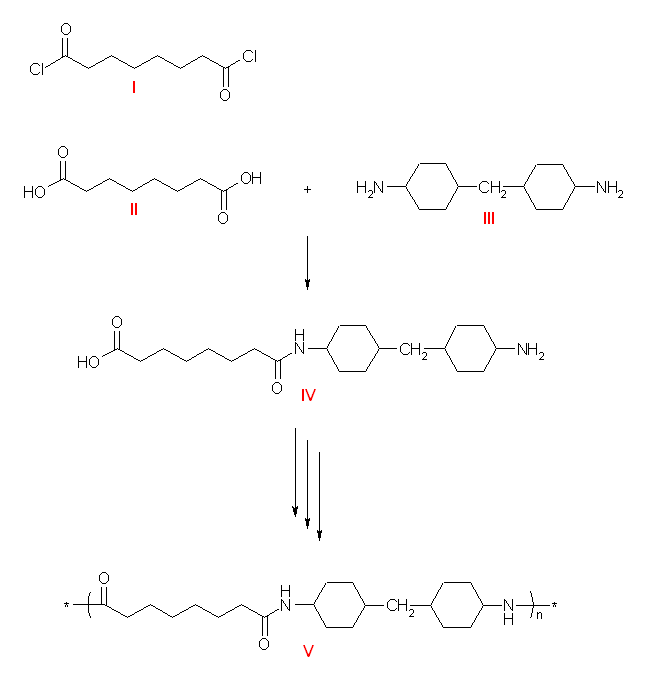
上図中、IV で示したような、アミノ基とカルボキシ基をもつ化合物が最小の繰り返し単位で、その脱水縮合による繰り返しでポリマー qiana キアナを生じる。しかし、この IV の構造をよく見ると、分子内に更にアミド結合があり、左右対称なジカルボン酸 II と、左右対称なジアミン III に分けることができる。(ジカルボン酸同士、ジアミン同士ではアミド結合をしないのでポリマーにはならないと考える。:ジカルボン酸は、酸無水物の形にはなってポリマーを形成しうるが、酸無水物は容易に加水分解される。)
合成上は、octanedioic acid, II の代わりに、octanedioyl dichloride, I を使うこともできる。
21.61-21.68 (65-73)
21.61, 65
21.59 でラクタム(環状のアミド)に対して起きたのと同様のことが、ラクトン(環状のエステル)でもおきる。
(解答例)
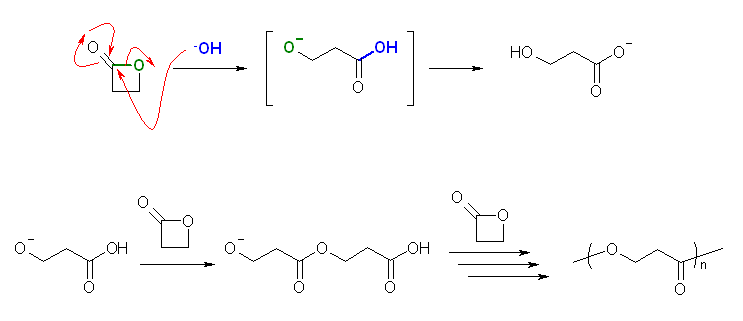
上段のようなラクトンに対する求核的な開環反応により、アルコラートを生じ、分子内のプロトン移動により(より酸性の高いカルボキシ基が解離し、より酸性の低い水酸基が遊離することで)右のような水酸基を持つカルボキシラートとなる。
反応は塩基性条件(触媒量の水酸化物イオン)なので、プロトン化を受けて活性化されたカルボニルが存在するわけではないから、中性の水酸基による求核攻撃は、たとえ4員環で結合角歪みが大きいとは言え、考えないものとすると、上段のような反応で生じたアルコラートが分子内のプロトン移動を生じる前に、近傍にある別のラクトンと反応するという経路を考える必要がでてくる。そのようにして書いたのが上図、下段の反応式である。
このようにして生じるポリマーは、形式的には「ポリエステル」である。
21.62, 66
酸無水物とアミンより、イミドを得る反応については、問い 21.51 を参照せよ。また、問い 21.60 との構造の類似にも着目せよ。
(解答例)
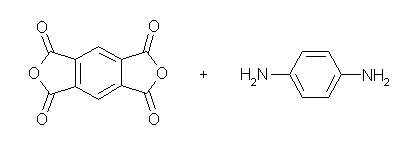
1,2,4,5-benzenetetracarboxylic dianhydride (慣用名:pyromellitic dianhydride) と、benzene-1,4-diamine (p-phenylenediamine) とを脱水縮合させる。
(21.63-21.66 は、分光学の問題なので省略しました。)
21.67, 72
エポキシ環への求核攻撃は、酸性条件(プロトンなどのルイス酸がエポキシ酸素に配位している条件)では、より級数の高い炭素上で起こり、それ以外の条件では立体的にすいている側の炭素上で起こる。
(解答例)
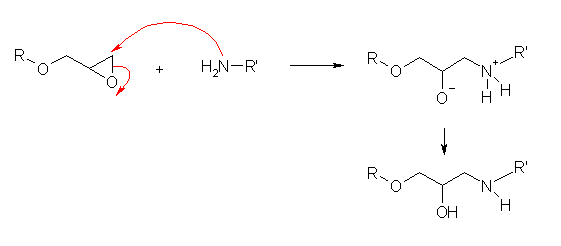
1級アミンでエポキシ環の末端側の炭素上を求核攻撃し、エポキシドの開環重合が起きる。
21.68, 73
生成物から予測せよ。
(解答例)
第1段階目では、次図のようにカルボニル求核置換反応により CI3- が脱離する。
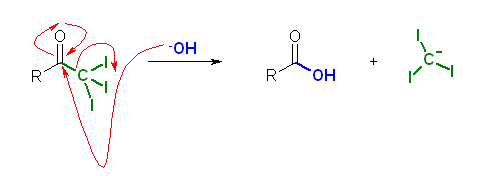
次いで、生じたカルボン酸は、アニオン CI3- にプロトンを与えることで、カルボキシラートイオンとヨードホルム(HCI3)とを与える。