20.01-20.10 (01-10)
20.01, 01
教科書 20.1 節を参照すること。
(解答例)
第6版の答え:
(a) 3-methylbutanoic acid
(b) 4-bromopentanoic acid
(c) 2-ethylpentanoic acid
(d) (Z)-4-hexenoic acid
(e) 2,4-dimethylpentanenitrile
(f) cis-cyclopentane-1,3-dicarboxylic acid
第5版の答え:
(a) 3-methylbutanoic acid
(b) 4-bromopentanoic acid
(c) hexa-2,4-dienoic acid
(d) 2-ethylpentanoic acid
(e) cis-cyclopentane-1,3-dicarboxylic acid
(f) 2-phenylpropanoic acid
20.02, 02
教科書 20.1 節を参照すること。
(解答例)
(a) 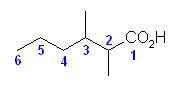
(b) 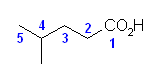
(c) 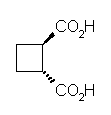
(d) 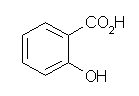
(e) 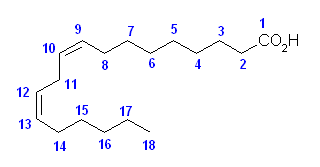
(f) 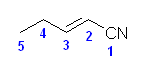
20.03, 03
酸性であるということは、塩基との反応で中和して塩をつくり、水にとけるということである。pKa = 5 の酸 AH は、水溶液の pH を 5 に調製してやれば、その半量が塩 A-、残りの半量は未解離の酸形 AH で溶けていることになる。pH を1上げてやれば全体の1割が未解離の酸形、pH を2上げてやれば全体の1%が未解離の酸形となり、残りは塩となっている。

(解答例)
ナフタレンはほとんど水に溶けない。安息香酸は有機溶媒に可溶だが、同時に、一部水にもとける。塩基性の水溶液では、安息香酸は塩をつくり完全に水にとける。
ナフタレン、安息香酸の混合物を有機溶媒(トルエンなど)に完全に溶解させる。ここに塩基(水酸化ナトリウムなど)を溶かしたアルカリ性水溶液を加え、よく攪拌する。安息香酸は塩をつくり水相に移動する。(有機相から安息香酸を完全に除くためには、このアルカリ溶液での洗浄を数回繰り返せばよい。)
有機相から溶媒を留去すると、ナフタレンのみが残る。
アルカリ溶液を塩酸などを用いて酸性化すると、安息香酸の塩が酸形にもどり、固体として析出するので、これをろ過により集めて乾燥させればよい。酸性化しても固体が析出しないような酸を用いている場合は、酸性化したのち、この酸溶液から有機溶媒を用いての抽出をおこなえばよい。
20.04, 04
20.3 のヒントに書いたように、酸解離平衡の平衡定数から考える。全濃度を C、解離度をαとおくと、解離した酸の濃度は Cα、未解離の酸の濃度は C(1-α)である。
(解答例)

20.05, 05
教科書 20.4 節参照。いずれも共役塩基が安定となるような酸が強酸である。
(a) いずれも酢酸 CH3CO2H の誘導体 X-CH2-CO2H として考えることができる。プロパン酸は -X = -CH3、ブロモ酢酸は -X = -Br、フルオロ酢酸は -X = -F
(b) アルコール、およびアミンについてはすでに学習済みの内容を思い出すこと。
(解答例)
(a) CH3-CH2CO2H < Br-CH2CO2H < F-CH2CO2H
(b) CH3CH2NH2 < CH3CH2OH < CH3CH2CO2H
20.06, 06
「酸性度が強い」=「共役塩基が安定」:共役塩基の共鳴形がたくさん書ける、負電荷が電気陰性度の高い原子上に書ける、などから判断できる。
逆に、酸性度が弱いのはなんらかの原因により共役塩基が安定でなくなるからである。
シュウ酸の第一段解離と第二段解離の平衡式を書いてみること。また、それぞれについて共役塩基の共鳴形を書いてみること。
(解答例)
第2段解離では、ジアニオンが生じる。他のジカルボン酸にくらべてシュウ酸はその負電荷間の距離が短いため、負電荷の反発が大きく、これによる不安定化があるため、第1のカルボキシ基に比べて第2のカルボキシ基は酸性が弱い。
20.07, 07
p-シクロプロピル安息香酸の pKa 4.45 は、無置換の安息香酸の pKa 4.19 よりも大きく、酸として弱い。併せて 20.5節 および 表 20.5 などを参照すること。
(解答例)
シクロプロピル基がメチル基などと同じように弱い電子供与性基としてはたらいている。したがって、シクロプロピル基は、芳香族求電子反応に対して活性化基としてはたらく。
20.08, 08
共役塩基のカルボキシラートが安定な方が強酸だから、電子吸引性基が結合したほうが強酸となる。また、(b) では、酢酸と安息香酸の酸性度の比較をすることを求められている。フェニル基は、負電荷を非局在化するはたらきがあることに注意。
(解答例)
(a) 弱酸: p-メチル安息香酸 < 安息香酸 < p-クロロ安息香酸 :強酸
(b) 弱酸: 酢酸 < 安息香酸 < p-ニトロ安息香酸 :強酸
20.09, 09
教科書 20.6 節を参照すること。ただし、グリニヤル試薬を用いる方法、ニトリルとしたのち加水分解する方法があるが、どちらにも反応の限界がある。
(解答例)
ハロゲンの付け根の炭素が sp2 炭素である (a) bromobenzene と、第3級炭素である (b) 2-chloro-2-methylpropane は、ともに求核置換反応を受けにくい基質であるから、ニトリルに変換する方法は適さない。したがって、(a) および (b) は、マグネシウムで処理してグリニヤル試薬としたのち、二酸化炭素を吹き込んでカルボン酸とすることができる。
(c) は、(a) や (b) と同じようにグリニヤル試薬経由でカルボン酸にすることができるほか、シアン化ナトリウム NaCN で処理して butanenitrile としたのち加水分解してカルボン酸にすることができる。
20.10, 10
教科書 20.8 節「カルボン酸の還元」についての問題であるから、その応用で考えることができる。(カルボン酸を経由しない方法もある。)
(解答例)
benzylbromide から phenylacetic acid への変換
2つの方法が可能である。benzylbromide をシアン化ナトリウム NaCN で処理すると、シアン化物イオンによる求核置換反応により phenylacetonitrile を生じる。これを加水分解すると、phenylacetic acid を得る。また、benzylbromide をマグネシウムで処理してグリニヤル試薬としたのち、二酸化炭素を吹き込むことによっても phenylacetic acid を得る。
phenylacetic acid から 2-phenylethanol への変換
カルボン酸は、LiAlH4 または BH3 により直接還元して対応する1級アルコールとすることができる。また、以上は教科書的な解となるが、実際の実験を行う際には、LiAlH4 によるヒドリド還元はエステルの還元よりも遅いから、反応の段数は増えるがエステル化したのちにヒドリド還元する方法を採ることもある。
別法:
benzylbromide をグリニヤル試薬としたのち、ホルムアルデヒドと反応させると 2-phenylethanol となる。
20.11-20.20 (11-17)
20.11, 11
アルコールは、ハロゲン化アルキルに変換することが可能である。
(解答例)
cyclopentylmethanol から bromomethylcyclopentane への変換
PBr3 で処理するとアルコールは臭化アルキルに変換される。
以下、問い 20.10 と同様にして、カルボン酸に変換の後、これを還元するとよい。または、グリニヤル試薬をホルムアルデヒドと反応させてもよい。
20.12, 21.25
(a), (b) (第5版では (a) と (c)) は、ケトンを生じる。(第5版の (b) ではアルデヒドを生じる。)教科書 20.9 節(第5版では、教科書 21.8 節)を参照すること。
ニトリルは、グリニヤル試薬との反応でケトンに変換することができる。非対称なケトンである (b) (第5版では (c))は、反応に2通りの原料およびグリニヤル試薬の組み合わせが考えられる。
ニトリルは、LiAlH4 のようなヒドリド試薬で還元すると、第1級アミンを与える。これは、シアノ基に対するヒドリド H- の求核付加反応である。
シアノ基に対してヒドリド H- の求核付加がおこると、シアノ基に対するグリニヤル試薬の求核付加で生じるのと同じ、イミンアニオン中間体を生成する。イミンアニオンを加水分解するとカルボニル化合物を生成するのだが、LiAlH4 を用いた場合では、ヒドリドによる第2段階目の求核攻撃も起こり、第1級アミンまで還元されるのである。(以下、第5版のみの記述。)より弱い還元剤である DIBAH (DiIsobutyl Alminum Hydride) を用い、極低温(-78℃など)で反応を行うと、ヒドリドの第2の付加は起こらず、水を付加させることによりイミン中間体をアルデヒドに加水分解することができる。これは、エステルの DIBAH によるアルデヒドへの還元(教科書 21.6 節:第5版、第6版とも)と類似の反応である。
(解答例)
(a) propanenitrile に、ethylmagnesium bromide を作用させる。生じるイミンアニオン中間体を加水分解すると、3-pentanone を得る。
(b) 2通りの合成ルートが考えられる。(第5版 (c)) benzonitrile と methylmagunesium bromide を作用させる。または、acetonitrile に phenylmagnesium bromide を作用させる。生じるイミンアニオン中間体を加水分解すると acetophenone を得る。
第5版 (b) 2-methylpropanal
2-methylpropanenitrile を、DIBAH (DiIsobutyl Alminum Hydride) を用い、極低温(-78℃など)で反応させる。生じたイミンアニオン中間体を加水分解すると 2-methylpropanal を得る。
20.13, 21.26
ハロゲン化アルキルは、グリニヤル試薬にすることができる。ニトリルとグリニヤル試薬からカルボニル化合物をつくることが可能である。前問を参照のこと。
(解答例)
2通りの合成ルートを考えることができる。その1。benzylbromide をグリニヤル試薬にした後、propanenitrile に作用させ、加水分解する。その2。benzylbromide を NaCN で処理して phenylacetonitrile とし、これに対し ethylmagnesium bromide を作用させ、加水分解する。
(20.14-20.15 は、分光学の問題なので省略しました。)
20.16, 14
カルボン酸の命名は、教科書 20.1 節を参照のこと。
(解答例)
(a) 3-bromo-4-methoxybenzoic acid
(b) 3-methyl-2-butenoic acid
(c) 1,3-cyclopentadienecarboxylic acid
(d) (S)-3-cyclopentyl-2-methylpropanoic acid
註:(d) は第6版のみの問題。
20.17, 15
構造式を読み取り、教科書 20.5 節を参照して、置換基効果を考慮すること。
(解答例)
(a) 4-bromobenzoic acid
p-位の臭素は電子吸引性基としてはたらくから、共役塩基を安定化する。従って、安息香酸よりも強酸である。
(b) 4-(N,N-dimethylamino)benzoic acid
ジメチルアミノ基は電子供与性基であるから、共役塩基を相対的に不安定にする。従って、安息香酸よりも弱酸である。
20.18, 16
4-hydroxy-2,2-dimethylbutanoic acid が目的となるカルボン酸である。ハロゲン化アルキルからグリニヤル試薬経由、またはニトリル経由でカルボン酸を合成する場合、カルボキシ基の代わりにハロゲンとなった物質が原料である。
(解答例)
ハロゲン化アルキルからニトリルへの変換
カルボキシ基は第3級の炭素に結合しているから、原料となるハロゲン化アルキルも3級であると、シアン化物イオンとの求核置換反応( SN2 反応)は使用することができない。
グリニヤル試薬への変換
グリニヤル試薬は、酸性の高い水素をもつ水酸基があると合成することができない。あらかじめ、水酸基をなんらかの方法で保護する必要がある。
20.19
色の違いからよみとれるベンゼン環上の電子密度に注目する。より強い電子供与性基が結合している場合、より電子密度は高くなるはずである。
(解答例)
チオメチル基よりもメトキシ基の方が相対的に強い電子供与性基としてはたらいている。電子供与性基は酸性度を下げる。したがって、p-methoxybenzoic acid よりも p-(methylthio)benzoic acid の方が強い酸であると判断できる。
20.20, 17
教科書 20.1 節、命名法について復習すること。
(解答例)
(第6版)
(a) 2,5-dimethylhexanedioic acid
(b) 2,2-dimethylpropanoic acid
(c) 3-cyanobenzoic acid
(d) (E)-cyclodec-2-enecarboxylic acid
(e) 2,2-dimethylpropanenitrile
(f) 3-ethylhexanoic acid
(g) 4,5-dibromopentanoic acid
(h) cyclopent-2-enecarbonitrile
上記のうち、(c) は 3- の代わりに m- を用いることもできる。
(第5版)
(a) 2,5-dimethylhexanedioic acid
(b) 2,2-dimethylpropanoic acid
(c) 3-propylhexanoic acid
(d) 4-nitrobenzoic acid
(e) (E)-cyclodec-1-enecarboxylic acid
(f) 4,5-dibromopentanoic acid
上記のうち、(d) は 4- の代わりに p- を用いることもできる。
20.21-20.30 (18-26)
20.21, 18
教科書 20.1 節、命名法について復習すること。
(解答例)
(a) 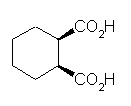
(b) 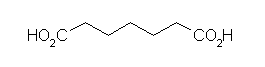
(c) 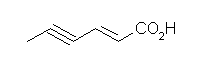
(d) 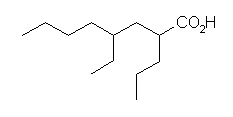
(e) 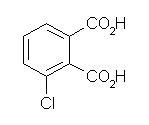
(f) 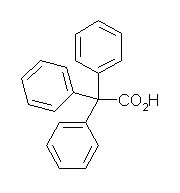
(g) 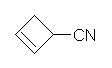
(h) 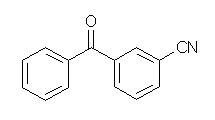
(g),(h) は、第6版のみ。
20.22, 19
(a) 第6版では、あきらかにミスプリントあります。カルボン酸の分子式は、C6H12O ではなく、C6H12O2 です。8種の異性体は、主鎖の長さごとに分類して書けば、書き落としがないです。
(b) (第6版のみの問題)C5H7N の分子式をもつニトリルは、不飽和度が1なので、二重結合または環構造が1つある。このような異性体は(たぶん数え忘れがなければ)12種類ある。このうち3つを書く。
(解答例)
構造式は省略し、名称のみを挙げる。各自の書いた分子構造および対応する名称と照合して確認すること。
(a) hexanoic acid, 2-methylpentanoic acid, 3-methylpentanoic acid, 4-methylpentanoic acid, 2-ethylbutanoic acid, 2,2-dimethylbutanoic acid, 2,3-dimethylbutanoic acid, 3,3-dimethylbutanoic acid
(b) 2-pentenenitrile,
3-pentenenitrile,
4-pentenenitrile,
2-methyl-2-butenenitirile,
2-methyl-3-butenenitirile,
2-ethyl-2-propenenitrile,
3-methyl-2-butenenitrile,
3-methyl-3-butenenitrile,
cyclobutanecarbonitrile,
1-methylcyclopropanecarbonitrile,
2-methylcyclopropanecarbonitrile,
cyclopropylacetonitrile (cyclopropylethanenitrile)
20.23, 20
基本は置換基効果で、共役塩基が安定化される場合、強酸となるから、電子吸引性基が結合するほうが強酸である。
(a) X-CO2H の構造までが共通である。電子的効果を考えるべき -X の部分は、酢酸は -CH3、シュウ酸は -CO2H、ギ酸は -H
(b) すべて安息香酸の誘導体だから、ベンゼン環上の置換基の電子的効果を考える。
(c) X-CH2CO2H の構造までが共通である。電子的効果を考えるべき -X の部分は、フルオロ酢酸は -F、3-フルオロプロパン酸は -CH2F、ヨード酢酸は -I
(解答例)
(a) 弱酸: acetic acid < formic acid < oxalic acid :強酸
(a) 弱酸: p-bromobenzoic acid < p-nitrobenzoic acid < 2,4-dinitrobenzoic acid :強酸
(a) 弱酸: 3-fluoropropanoic acid < iodoacetic acid < fluoroacetic acid :強酸
20.24, 21
それぞれの組の中で陰イオンの部分(すなわち、酸の共役塩基の形である)が塩基として強いか弱いかを決めればよい。弱酸の共役塩基は強い塩基で、強酸の共役延期は弱い塩基である。
(a) では、酢酸、水、メタンが、比較すべき塩基に対する共役酸である。
(b) では、安息香酸、p-ニトロ安息香酸、アセチレンが比較すべき塩基に対する共役酸である。
(c) では、水、エタノール、ギ酸が比較すべき塩基に対する共役酸である。
(解答例)
(a) 弱塩基: Mg(OAc)2 < Mg(OH)2 < H3C-MgBr :強塩基
(b) 弱塩基: O2N-C6H4-CO2Na < C6H5-CO2Na < CH≡CNa :強塩基
(c) 弱塩基: HCO2Li < HOLi < CH3CH2OLi :強塩基
20.25, 22
(a),(b),(d) は同じ炭素数での変換。
(c) は炭素数が1増えている。グリニヤル試薬経由またはニトリル経由で合成できる。
(e) は炭素数が倍である。二量化反応を利用できる。
(解答例)
試薬や条件のみを示す。それぞれの作成する解答においては、かならず反応式の形で示すこと。
(a) BH3 または LiAlH4 で還元。エステル化してから LiAlH4 で還元しても可。
(b) (a) で 1-butanol としたのち、PBr3 で処理。
(c) (b) で合成した 1-bromobutane をc
(d) (b) で合成した 1-bromobutane を強塩基(NaOEt/EtOH など)で処理することにより、E2 脱離させる。
(e) (b) で合成した 1-bromobutane をリチウム試薬としたのち、一価のヨウ化銅と反応させ、ギルマン試薬に変換する。これを 1-bromobutane と反応させることでカップリング反応させる。
20.26, 23
(a),(b),(c) は同じ炭素数での変換、(d) は炭素数が1増やすのだから、グリニヤル試薬経由またはニトリル経由で合成できる。(e) は炭素数が半分になる。二重結合の位置での開裂反応が利用できる。
(解答例)
(a) 酸性 CrO3 などで酸化する。PCC ではアルデヒドまでしか酸化されない。
(b) 水酸化ナトリウムなどで加水分解すると、ハロゲン化アルキルは対応するアルコールになる。これは (a) に帰着される。
(c) ヒドロホウ素化を用いて1級のアルコールにする。酸性水溶液での水和反応やオキシ水銀化法を用いると、2級のアルコールである 2-butanol となってしまう。1級のアルコールは (a) に帰着される。
(d) グリニヤル試薬としたのち、二酸化炭素で処理。または、シアン化ナトリウムで処理し、シアン化物イオンによる SN2 反応で butanenitrile とした後、加水分解。
(e) 酸性 KMnO4 での酸化開裂を用いると、直接カルボン酸 butanoic acid が得られる。オゾン酸化開裂(酢酸中の亜鉛での処理を含む)では、アルデヒド butanal が得られるから、これをさらにマイルドな条件、アンモニア性硝酸銀(Tollens 試薬)で酸化してもよい。
20.27
第6版教科書 20.9 節(第5版 21.8節)「ニトリルの化学」などを参照すること。
(解答例)
(a) ニトリルの加水分解(強酸、または強塩基)後、BH3 または LiAlH4 で還元する。エステル化してから LiAlH4 で還元しても可。
(b) ニトリルを LiAlH4 で還元する。
(c) グリニヤル試薬 isopropylmagnesium bromide をニトリルに対して求核反応させる。生じるイミンアニオン中間体を加水分解してケトンを得る。
20.28, 24
いずれも多段階反応が必要である。そのような場合は、逆合成の手法で考える。すなわち、最終生成物を与えることが可能な前駆体の構造を考え、次にその前駆体を与えることができる構造を考え、ということを出発物質に辿り着くまで繰り返す。
(解答例)
反応のルートの一例のみを示す。ベンゼン環への置換基の導入は、その反応が芳香族求電子反応である場合、電子供与性の置換基はオルト、パラ配向性をもち、電子吸引性の置換基はメタ配向性をもつ。これらに注意する。
(a) 3-chlorobenzoic acid の前駆体として可能性があるのは、benzoic acid または、3-chlorotoluene である。前者を塩化鉄存在下、塩素で処理して塩素化すると、カルボキシ基が電子吸引性なので選択的にメタ位を塩素化できる。また、後者の3-chlorotoluene は、芳香環の側鎖の酸化条件で安息香酸誘導体へ変換することができる。(ただし、トルエンのメチル基は弱い電子供与性基だから、トルエンを塩素化してもメタ位ではなく、オルト、パラ位で反応が起きてしまう。また、ハロゲン基も、電子吸引性基でありながらオルト、パラ配向性であったことを思い出すこと。従って、3-chlorotoluene を合成するためには、長い工程が必要となると思われる。)
benzoic acid は、toluene の芳香環側鎖を酸化すれば得られる。これは benzene に対し、CH3Cl などを用いて Friedel-Crafts によりアルキル化して得られるが、benzene よりも電子供与性基であるアルキル基が置換した toluene の方が基質として活性が高いから、アルキル基が2つ、3つとはいった xylene や trimethylbenzene などの混合物を生じるため、実験室での少量実験には向いていない。むしろ、benzene を臭素化して bromobenzene としたのち、マグネシウムで処理してグリニヤル試薬 phenylmagnesium bromide としたのち、二酸化炭素で処理することにより安息香酸を得るほうが優れていると思われる。(とはいえ、実際にトルエンをベンゼンから合成する羽目に陥ることはほとんどない。トルエンもベンゼンと同じ程度にポピュラーな試薬として売られているから、ベンゼンの代わりにトルエンを購入すればよいだけである。だから、ここでは「教科書的には変換が可能」というレベルで考えてもさしつかえないだろう。)
(b) 4-bromobenzoic acid の前駆体として可能性があるのは、4-bromotoluene で、側鎖のメチル基を酸化することにより 4-bromobenzoic acid とすることができる。ハロゲン基、メチル基ともにオルト、パラ配向性であるから、どちらの置換基を先にベンゼン環に導入しても反応スキーム上は可能であるが、ハロゲン基は不活性化基、メチル基は活性化基だから、ハロゲンを先に導入するよりメチル基を先に導入する方がすぐれていると考えられる。従って、4-bromotoluene は toluene の臭素化(Br2 / FeBr3)で合成する。
また、教科書的な方法ではないが、1,4-dibromobenzen を経由することも考えられる。これをグリニヤル試薬や、リチウム試薬を経由して、臭素をカルボキシ基に変換することが可能であるが、上手に条件を設定してやれば、一方の臭素のみを選択的に有機金属試薬に変換することも可能かもしれない。この有機金属化の部分が選択的に進行しないと、1,4-dibromobenzen、4-bromobenzoic acid、1,4-benzenedicarboxylic acid の混合物となってしまう。
(c) (a),(b) 同様に toluene としたのち、ベンジル位の臭素化(NBS/BPO)により benzylbromide とすることができれば、ハロゲン化アルキルから炭素数の1多いカルボン酸への変換の常道に従い、グリニヤル試薬としたのち二酸化炭素で処理するか、またはシアン化ナトリウムを用いて SN2 反応により phenylacetonitrile とした後に加水分解すればよい。
また、benzylbromide は、toluene の臭素化以外の方法として、benzyl alcohol よりの合成が可能である。benzyl alcohol は、bromobenzene をグリニヤル試薬としたのち、これをホルムアルデヒドと反応させることで得られる。
20.29, 25
酸性度定数の定義の問題。すでに2年生でも学習済みである。第2章のブレンステッド-ローリーの酸塩基の定義の辺りを復習のこと。
(解答例)
pKa = -log(Ka) であるから、
(a) -log10(8.4×10-4)= 3.076
(b) -log10(5.6×10-6)= 5.252
20.30, 26
関数電卓を使えばすぐに求まるが、たとえば 10-3.14 という値を計算した結果に対して、10-3 (すなわち 0.001)と 10-4 (すなわち 0.0001)の間であるはずであるといった感覚を持つこと。そのような感覚を持つことが、ケアレスミスの減少につながる。
(解答例)
(a) 10-3.14 = 7.244 × 10-4
(b) 10-2.98 = 1.047 × 10-3
20.31-20.40 (27-34)
20.31, 27
ΔG゜= - RT loge( Ka ) という式は、対数の底を e から 10 に変換(自然対数から常用対数への変換)のための係数、2.303 を用いて次式のように表される。
ΔG゜= -2.303 RT log10( Ka )
ここで、pKa = -log10( Ka ) であったことを思い出すと、上式を、そのまま次のように変形することが可能である。
ΔG゜= -2.303 RT log10( Ka ) = 2.303 × RT × pKa
なお、この問いで求めるのは、酸の解離平衡の平衡定数 Ka に対し、ΔG゜を計算するのであるから、HA の状態(解離前)と、H+ + A- の状態(解離後)の自由エネルギー差を求めることになる。この自由エネルギー差が大きく解離後の状態が安定になるほど、平衡時において解離した分子の割合が増える。
(解答例)
(a) エタノール(pKa = 16.0)では、
ΔG゜= -2.303 RT log10( Ka ) = 2.303 × RT × pKa = 2.303 × 8.315(J/K mol)×300(K) × 16.0
= 91917 (J/mol) ~ 91.9 (kJ/mol)
(b) 酢酸(pKa = 4.75)では、
ΔG゜= -2.303 RT log10( Ka ) = 2.303 × RT × pKa = 2.303 × 8.315(J/K mol)×300(K) × 4.75
= 27288 (J/mol) ~ 27.3 (kJ/mol)
20.32, 28
問い 2.6 なども参照とすること。
(解答例)
第2イオン化(2段目の酸解離)の平衡は、近傍にある負電荷を帯びたカルボキラートイオンによる影響を受け、相対的に解離形(共役塩基の形)が不安定化をうける。このため、第2段目の酸は、第1段目の酸より弱くなる。この不安定化は、誘起効果によるもので、σ 結合を介して伝わるから間の結合の数が増えれると影響も小さくなると考えられる。
20.33, 29
章末の「反応のまとめ」のスキームを見て、該当する反応を探し、その部分の解説をよく読んでおくこと。
(解答例)
(a) 4-methylbenzyl alcohol
カルボン酸はボラン BH3 で第1級アルコールまで還元される。ヒドリド還元との反応性の違いについて整理しておくこと。ヒドリド還元では、アルデヒドやケトンが最も反応しやすいが、ボランを用いた場合は、カルボン酸が一番反応しやすい。次いでアルデヒドやケトンのカルボニルが反応するが、ボランは、炭素炭素二重結合との反応もおきる。これはヒドロホウ素化反応である。
(b) 4-(bromomethyl)benzoic acid
N-ブロモスクシンイミド( NBS ) は、Br2 をごく少量ずつ与える試薬。四塩化炭素のように低極性溶媒中で、BPO などの開始剤を加えてラジカル機構で臭素化が進行する。ラジカル臭素化では、ベンゼン環上には反応がおきず、ベンジル位が臭素化される。
(c) 反応しない。
カルボン酸は酸性水素をもつから、methylmagnesium bromide CH3-MgBr の求核種の部分、CH3- が H+ と反応して、CH4 を与えてしまう。
(d) 1,4-benzenedicarboxylic acid
酸性条件では、KMnO4 は、芳香環側鎖をカルボン酸にまで酸化する。
(e) 4-methylbenzyl alcohol
カルボン酸は LiAlH4 で第1級アルコールまで還元される。
20.34, 30
二酸化炭素は、分子内にカルボニル基と同じ炭素酸素二重結合をもつから、中央の炭素は求核攻撃を受けることができる。そのため、グリニヤル試薬との反応でカルボン酸を調製するのに用いることができる。
(解答例)
(a) ethylmagnesium bromide + 13CO2 → CH3CH213CO2H
(b) methylmagnesium bromide + 13CO2 → CH313CO2H
この反応で得られる標識された酢酸を、BH3 (または、LiAlH4)で還元すると、CH313CH2OH を与える。
PBr3で処理して、bromoethane に変換したのち、再度グリニヤル試薬としたのち二酸化炭素を作用させる(または、bromoethane をシアン化ナトリウムと反応させて propanenitrile としたのち、加水分解する)ことにより、目的の化合物を得る。
CH313CH2OH →
CH313CH2Br →
CH313CH2MgBr →
CH313CH2CO2H
CH313CH2OH →
CH313CH2Br →
CH313CH2CN →
CH313CH2CO2H
20.35, 31
カルボキシ基の炭素1つ分だけ、炭素数の増えたものが目的生成物である。また、このカルボキシ基は、出発物質である methylenecyclohexane の二重結合の炭素に結合している。二重結合への位置選択的な反応の重要なものとして、水和反応がある。水酸基は容易にハロゲンに変換できる。
(解答例)
methylenecyclohexane の水和反応は、オキシ水銀化法を用いるとマルコフニコフ配向で 1-methylcyclohexanol を与え、また、ヒドロホウ素化法を用いると逆マルコフニコフ配向で 2-cyclohexylethanol を与える。これらのアルコールを PBr3 で処理すると、対応する臭素化物を与えるから、グリニヤル試薬としたのち二酸化炭素を反応させると目的の2種のカルボン酸を与える。1-bromo-1-methylcyclohexane は第3級のハロゲン化アルキルなので SN2 反応を受けないが、(bromomethyl)cyclohexane はシアン化ナトリウムとの反応によりcyclohexylacetonitrile を与えるから、これを加水分解してもよい。
20.36, 32
グリニヤル試薬は、酸性水素をもつ官能基などを分子内にもつと調製できない。また、ハロゲン化アルキルからニトリルに変換する反応は、SN2 機構で進行するから、ハロゲン化アルキルが第1級であることが望ましい。第2級でも反応はおきるが、第3級では反応しない。
(解答例)
(a), (d) これらは、分子内に水酸基を持つから、グリニヤル試薬を経由して反応させるためには、水酸基を DHP-エーテルなどの形で保護する必要がある。一方、シアン化物イオンによる求核置換でのニトリルは問題なく生成される。したがって、この基質の場合はニトリルの加水分解の過程の方が優れているといえる。
(b) いずれの方法も適用可能である。ただし、臭素が不斉炭素に結合しているような光学活性なハロゲン化アルキルを、光学活性なカルボン酸にしたい場合には、ニトリル経由で調製する必要がある。このとき、ハロゲン化アルキルからニトリルへの変換は、SN2 機構で進行するから、不斉炭素上でワルデン反転が起き、立体は反転となる。
(c) カルボニル基はグリニヤル試薬と反応してしまうから、分子内のカルボニル基を保持したままグリニヤル試薬とすることはできない。あらかじめアセタールとして保護すればよい。一方、シアン化物イオンによる求核置換でのニトリルは問題なく生成される。したがって、この基質の場合はニトリルの加水分解の過程の方が優れているといえる。
20.37
1,3-butadiene の炭素数は4、目的生成物である 1,6-hexanediamine の炭素数は6と増えている。ニトリルの還元で第1級アミンを得ることができたことを思い出すこと。
(解答例)
次の反応ルートで合成が可能である。
CH2=CH-CH=CH2 → HO-CH2-CH2-CH2-CH2-OH → Br-CH2-CH2-CH2-CH2-Br → NC-CH2-CH2-CH2-CH2-CN → H2N-CH2-CH2-CH2-CH2-CH2-CH2-NH2
ヒドロホウ素化反応(BH3, then H2O2/-OH)で逆マルコフニコフ配向で水和すると、1,4-butanediol とすることができる。つづけて PBr3 で処理すれば 1,4-dibromobutane を得る。シアン化ナトリウム NaCN との SN2 反応により炭素数の2つ増えた hexanedinitrile に変換されるので、これを LiAlH4 で還元すると、目的生成物である 1,6-hexanediamine となる。
20.38, 33
出発原料として選択された 2-chloro-2-methylpentane および、目的物である 2,2-dimethylpentanoic acid の構造を書いてみること。問い 20.36 のヒントなども参照すること。
(解答例)
2-chloro-2-methylpentane は、第3級のハロゲン化アルキルなので、SN2 反応は進行しない。代わりに、シアン化物イオンが塩基として働き、E2 反応により 2-pentene が生じるような副反応のみが起きる。
20.39
逆反応の手順で考えること。最後の段階は、ハロゲン化アルキルからグリニヤル試薬またはニトリル経由でカルボン酸にする反応を利用することができる。
(解答例)
ibuprofen ( 2-(4-isobutylphenyl)propanoic acid ) は、1-(1-bromoethyl)-4-isobutylbenzene から、グリニヤル試薬またはニトリル経由で合成することが可能である。
1-(1-bromoethyl)-4-isobutylbenzene は、対応するアルコール、1-(4-isobutylphenyl)ethanol を PBr3 などで処理することで得られる。
1-(4-isobutylphenyl)ethanol は、対応するケトンのヒドリド還元で得られる。対応するケトンは、1-(4-isobutylphenyl)ethanone で、ヒドリド還元剤には NaBH4 または LiAlH4 を用いることができる。(acetophenone は、IUPAC の命名規則において、4-isobutylacetophenone というような誘導体をつくることは推奨されない。)
1-(4-isobutylphenyl)ethanone は、isobutylbenzene に対する Friedel-Crafts 反応によるアセチル化で合成することができる。反応条件は、CS2 などの溶媒中、CH3COCl、および1モル当量の AlCl3 を用いる。Friedel-Crafts アルキル化では、ルイス酸は触媒量でよいが、アシル化反応では、ルイス酸が、生成するケトンと錯体を作るから酸クロリドに対して1モル当量以上が必要である。
また、別の合成ルートとして、上記反応で得たアセチル体、1-(4-isobutylphenyl)ethanone から、対応するシアノヒドリン ( 2-hydroxy-2-(4-isobutylphenyl)propanenitrile ) へ変換したのち、酸性条件下でシアノ基を加水分解してもよい。この条件下で脱水(E1 脱離)が同時におき、フェニル基やカルボキシ基のカルボニルと共役した二重結合をもつ化合物、2-(4-isobutylphenyl)prop-2-enoic acid を与える。これを接触水素添加すれば、目的の ibuprofen を与える。
20.40, 34
(a) と (b) は、反応条件が間違っている。式で与えられたような生成物を得るための反応条件を答えよ。
(c) および (d) は、生成物の構造が間違っている。与えられた反応条件に対して得られる生成物を答えればよい。特に、(d) は、分子内に3級の水酸基があるが、酸性条件下、どのようになるか考えること。
(解答例)
(a) BH3 は、toluene には反応しない。(BH3 は、カルボニル化合物のほか、炭素=炭素の二重結合とも反応するが、芳香環の二重結合は反応しない。)芳香環の側鎖をカルボキシ基まで酸化するためには、酸性で KMnO4 を用いるとよい。
(b) ハロゲン化アルキルをカルボン酸にするためには、1) Mg によりグリニヤル試薬としたのち、(NaCN ではなく、)CO2 を作用させる、または 2) (グリニヤル試薬にせず)NaCN と反応させて SN2 反応によりニトリルに変換したのち、加水分解する、のいずれかの条件を用いる。(この問いでは、これらの条件が入り混じってしまっている。)
(c) LiAlH4 によるヒドリド還元では、カルボン酸は第1級アルコールまで還元される。2-phenylethanol は、そのままでは LiAlH4 による還元はこれ以上進行しないが、まず PBr3 で処理して banzylbromide とすれば、LiAlH4 でヒドリドによる求核攻撃でethylbenzene とすることができる。また、2-phenylethanol から脱水(POCl3/pyridine など)させ、stylene とすれば、接触水素化により目的として与えられている ethylbenzene とすることができる。
(d) ハロゲン化アルキルの部分は、ニトリルに変換され、酸性条件下での加水分解によりカルボキシ基に変換できるが、このとき同時に第3級のアルコールは、E1 脱離する。(水酸基 -OH がプロトン化されると、-OH2+ となり、中性の水分子が脱離して安定な第3級のカルボカチオンを容易に生成する。これが中間体である。)これにより、ザイツェフ則に従ったアルケン 4-methyl-3-pentenoic acid を生成する。生じた二重結合に、再度マルコフニコフ配向性で水和させる(オキシ水銀化法など)ことにより、4-hydroxy-4-methylpentanoic acid を与えることができる。
20.41-20.50 (35-43)
20.41
シアノ基 -C≡N: は、カルボニル基と同様に多重結合が分極している。炭素上に正の部分電荷をもつ。窒素の孤立電子対にプロトンなどのルイス酸が配位すると、この分極がより大きくなるので、水分子(のように、比較的弱い求核種)による求核反応が生じる。この求核反応は、ニトリルに対してグリニヤル試薬が求核攻撃するときの反応機構を参考にして描くことができる。
(解答例)
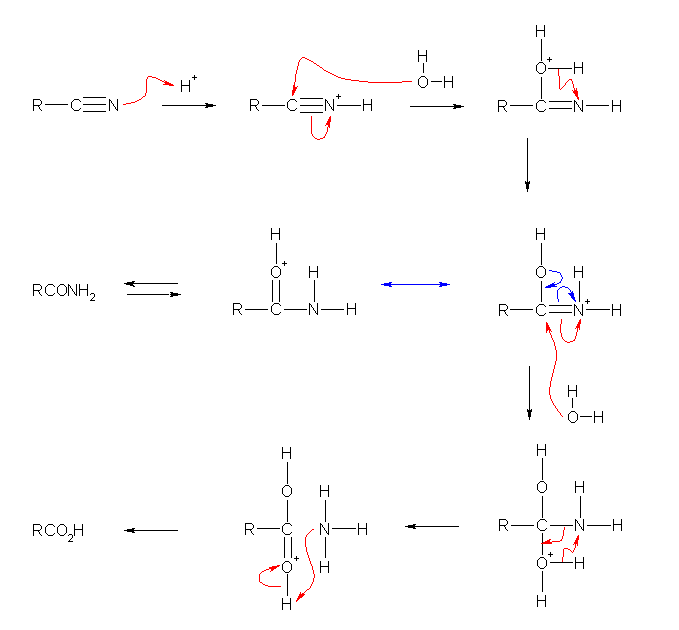
まず、窒素上にプロトン(ルイス酸)が配位し、炭素への水の求核付加を生じさせる。これにより、酸素上に正電荷が生じるので、ここよりプロトンが移動する。その移動先は、分子内で最も塩基性の高い部位、すなわち窒素である。この構造(上図、右列、上より2番目)は、プロトン化されたアミドの極限構造との間に共鳴関係がある(すなわち、本質的に同じ構造を電子の位置を変えて別の方法で描いたにすぎない)。つまり、ここまで反応させた時点で、ニトリルの加水分解は、アミドの加水分解に帰着された。
さらに二重結合炭素に水の求核付加を生じさせ、分子内でプロトン移動を起こしたあと、中性のアンモニアを脱離させると、加水分解は終了である。生じるカルボン酸はプロトン化された形であるから、このプロトンを放出し、生じたアンモニアがこのプロトンを受け取る形とした。
酸性条件下のエステルの加水分解は可逆であるが、酸アミドやニトリルの場合は可逆ではない。これは、上記解答例にも示したように加水分解によりアンモニアを生じるのであるが、これが酸性下ではプロトン化を受けてしまうため、逆反応に必要な窒素からの求核攻撃を起こすことができなくなるからである。
20.42, 35
アミノ基は、ニトロ基の還元により得ることができる。カルボキシ基はメチル基の酸化で得ることができる。これらの反応の順序に気をつけること。
(解答例)
1)混酸(硝酸/硫酸)により、トルエンをニトロ化。メチル基の電子供与性により、芳香族求電子置換反応は、o, p- 配向性なので、主生成物として、p-ニトロトルエンを得る。
2)過マンガン酸水溶液で処理し、側鎖アルキル基のベンジル位での酸化反応により、p-ニトロ安息香酸を得る。ニトロ基は酸化反応に対して不活性。(先に還元してしまうと、酸化反応の条件に対して保持できない。)
3)塩酸-塩化スズにより、ニトロ基を還元。この条件では、カルボキシ基は反応しない。これにより、p-アミノ安息香酸を得る。
20.43, 36
それぞれの条件で、反応する箇所は1箇所ずつしかない。また、これらの条件の中には、リトコール酸が反応しない条件もある。それぞれの条件で判らないものがある場合は、章末の「反応のまとめ」を見ながら、その条件がどの官能基をどのように変換するかを探すこと。
(解答例)
反応する部位についてのみ述べる。各自の解答においては、「反応生成物を予測せよ」という問題なので、反応生成物の構造を答えるのが適当だろう。
(a) 第2級アルコールのケトンへの酸化。
(b) アルデヒド基を持たないため反応しないので、原料を回収。
(c) カルボキシ基の第1級アルコールへの還元。
(d) アルコールのシリルエーテル化。R-O-Si(CH3)3 を与える。
(e) リトコール酸中に酸性水素(カルボキシ基および水酸基)があるため、先ず2モル当量のグリニヤル試薬は、塩基として働き、この酸性水素を引き抜いて CH4 を与える。ここまでではリトコール酸自体は、変化しない。(正確には、マグネシウム塩などになるため、酸による処理で元の構造に戻る。)
(f) リトコール酸中に酸性水素(カルボキシ基および水酸基)があるため、先ず2モル当量のヒドリドは、塩基として働き、この酸性水素を引き抜いて H2 を与える。ここまでではリトコール酸自体は、変化しない。もし、過剰のヒドリド試薬( LiAlH4 )が加えられ、エーテル中で還流するなどの条件があれば、カルボキシ基は第1級アルコールまで還元することができる。
20.44, 37
逆合成の手法で考えること。フェニル基に2つの置換基を導入する。導入する順序に気をつける必要がある。
α-ヒドロキシカルボン酸は、シアノヒドリンの加水分解により合成できることを思い出すこと。
(解答例)
(考え方1:置換基の導入の順序について)
1) ベンゼン環上のハロゲンは、求電子置換反応に対し、不活性化基ではあるが、o-, p- 配向性を示す。従って、シクロヘキシル基の p- 位にある置換基(塩素から見たら m- 位)よりも後から導入する。
2) シクロへキシル基(アルキル基)は、求電子置換反応に対し、 弱い o-, p- 配向性を示す。はじめにシクロヘキシル基の p- 位にある置換基を導入することで問題ない。
3) ベンゼン環上で塩素化を行う際、シクロヘキシル基の p- 位にある置換基が m- 配向性を持っている必要がある。従って、なんらかの電子吸引的なものをはじめに導入し、塩素の導入後、与えられたような構造に変換すればよい。
(考え方2:シクロヘキシル基の p- 位の置換基の変換)
4) ベンジル位の塩素の導入の仕方には、一般的には2通りの考えがあり得る。1つはベンジル位の直接的な塩素化反応で、もうひとつはベンジルアルコール型の化合物からの変換である。この化合物においては、シクロヘキシル基にもベンジル水素があることを考えると、前者の方法では、なんらかの工夫なしには選択的に欲しいものが得られない。そうすると、1-carboxy-1-chloromethyl 基は、1-hydroxy-1-chloromethyl 基から誘導する。ただし、1) ~ 3) の考察により、電子吸引性基である必要から、1-hydroxy-1-chloromethyl 基をなんらかの方法で カルボニル基を持つ置換基から誘導することを考える。
5) カルボキシ基は、アルコールやアルデヒドの酸化反応によって生じさせるか、エステル、シアノ基の加水分解により生じさせることができる。二重結合や三重結合の酸化開裂(ベンゼン環の二重結合は反応しない)によってもカルボキシ基とすることが可能である。
(反応例)
アルデヒド基から、シアノヒドリンを経由してシアノ基の加水分解によりカルボキシを得る経路。
cyclohexylbenzene →(途中省略)→ 4-cyclohexylbenzaldehyde → 3-chloro-4-cyclohexylbenzaldehyde → 2-(3-chloro-4-cyclohexylphenyl)-2-hydroxyacetonitrile → 2-(3-chloro-4-cyclohexylphenyl)-2-hydroxyacetic acid →
2-chloro-2-(3-chloro-4-cyclohexylphenyl)acetic acid
(反応例2)
シュウ酸の酸塩化物によるフルーデルクラフト反応により、β-ケトカルボン酸を導入する経路。
cyclohexylbenzene → 2-(4-cyclohexylphenyl)-2-oxoacetic acid → 2-(3-chloro-4-cyclohexylpheny)-2-oxoacetic acid → 2-(3-chloro-4-cyclohexylpheny)-2-hydroxyacetic acid → 2-chloro-2-(3-chloro-4-cyclohexylphenyl)acetic acid
上の反応例のいずれも、構造式で書き下して、どこが変換されているか確認すること。また、反応条件についても、適宜調べること。
fenclorac は、酢酸の誘導体として命名される。
chloro-(3-chloro-4-cyclohexylphenyl)acetic acid
20.45, 38
教科書 20.5 節等を参照すること。ベンゼン環上の π 電子密度が上がると、芳香族求電子反応は活性化され、また、置換安息香酸においてはその共役塩基が不安定化されるから、酸性度は下がる。
(解答例)
| 置換基 | π 電子密度 | 共役塩基 | 酸性度 | 求電子反応の反応性 |
|---|---|---|---|---|
| 電子供与性 | 上がる | 不安定化 | 下がる。 従って、pKa は、4.19 よりも大きくなる | 活性化 |
| 無置換 | (基準) | (基準) | pKa = 4.19 | (基準) |
| 電子求引性 | 下がる | 安定化 | 上がる。 従って、pKa は、4.19 よりも小さくなる | 不活性化 |
上表のような関係になるから、反応が大きい順(大きい方から小さい方へ)に並べると、それは、pKa の値では大きいほうから小さい方へ並べることになる。
(活性化基):-Si(CH3)3 のみ。
(不活性化基):5つの選択肢中、上以外のすべて。
20.46, 39
いずれも、カルボン酸を対応するハロゲン化アルキルから合成するルートで得ることができる。この変換は、グリニヤル試薬としたのち二酸化炭素を作用させるか、あるいは、NaCN による反応でニトリルとしたのち加水分解することで達成する。
(a) Friedel-Crafts のアルキル化を用いる場合は、まずイソプロピル基を導入し、isopropylbenzene (慣用名:クメン, cumene)とするとよい。また、Friedel-Crafts のアルキル化ではモノ置換生成物のみを選択的に得ることは難しいから、モノ置換体を選択的に生じることのできる Friedel-Crafts のアシル化反応を用いる場合は、まずアセチル化により acetophenone とすればよい。
(b) グリニヤル反応を使うことができる。
(解答例)
(考え方)
1) RR'C=O + -CN でシアノヒドリンを形成させると、RR'C(OH)CN となる。一見、この水酸基は、スルホン酸エステルまたはハロゲン化を経て置換させることが可能なように見えるが、立体的な要因を考えるとあまり良い選択肢ではないように思われる。
2) R-Br + -CN → R-CN のように、ハロゲン化アルキルの求核置換反応によりシアノ基を導入することを考えると、生成物の構造を見たとき第3級の位置にカルボキシ基があり、第3級のハロゲン化アルキルを基質としなければならない。これも、立体的な要因を考えるとあまり良い選択肢ではないように思われる。
3) R-MgBr + CO2 → R-CO2- のように、グリニヤル試薬(ハロゲン化アルキルから調製)と二酸化炭素との反応を考える場合、求核反応が起きる位置は二酸化炭素上であるから、ハロゲン化アルキルの立体的な要因には左右されない。しかしながら、グリニヤル試薬の調製時には、分子内の他の官能基の制約(酸性を示すようなアルコール、カルボン酸、あるいはグリニヤル試薬と容易に反応するようなカルボニル基などは、保護基などを適切に用いて、マスクしておかなければならない)ことにも留意すること。
(反応例)
(a) Friedel-Crafts のアルキル化でイソプロピル基を導入し、NBS を用いてベンジル位のみを選択的に臭素化、Grignard 試薬として二酸化炭素と反応させる経路。
PhH + Cl-CH(CH3)2 → Ph-CH(CH3)2
→ Ph-CBr(CH3)2 → Ph-C(MgBr)(CH3)2 → Ph-C(CO2H))(CH3)2
(b) まず PhMgBr を反応させ、生じるアルコールをハロゲン化し、更に Grignard 試薬に変換してから二酸化炭素と反応させる経路。
RR'C=O + PhMgBr → RR'C(OH)Ph → RR'C(Br)Ph → RR'C(MgBr)Ph → RR'C(CO2H)Ph
20.47, 40
「酸性度を増加させる」ということは、電子密度が下がっていることを意味する。水酸基やメトキシ基の酸素が、電子供与基としてはたらくのは、酸素上の孤立電子対の共鳴効果によるものである。酸素の孤立電子対がベンゼン環上にあたえらるような共鳴構造を書けるだけ描いてみること。また、これらとは別に、酸素は電気陰性度が大きいから(オルト位やパラ位では打ち消されてしまっているものの)誘起効果ももつ。
(解答例)
2.45 の表を一部変更の上、再掲
| 置換基の効果 | カルボキシ基の結合位置での π 電子密度 | 共役塩基 | 酸性度 |
|---|---|---|---|
| 電子供与性 | 上がる | 不安定化 | 下がる。 従って、pKa は、4.19 よりも大きくなる |
| 無置換 | (基準) | (基準) | pKa = 4.19 |
| 電子求引性 | 下がる | 安定化 | 上がる。 従って、pKa は、4.19 よりも小さくなる |
上記表と m- および p- ヒドロキシ安息香酸の酸性度とを見比べても判るように、p-位の水酸基は、カルボキシ基の結合位置の π 電子密度を上げている。これは、次図に表すような共鳴効果による。
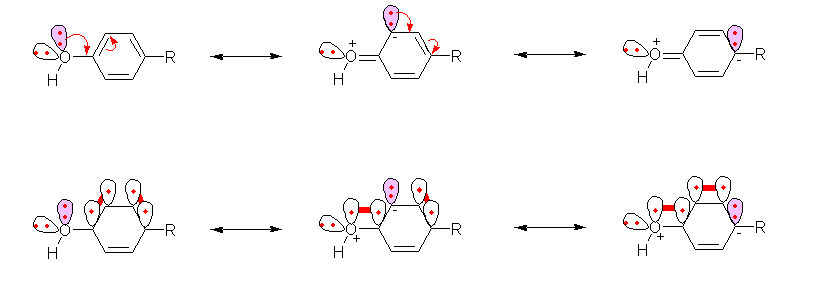
上が通常の共鳴式。下は、π 結合を、p軌道を使って模式的に表現したもの。この共鳴効果は、o- および p- 位にのみ働く。いわば、この共鳴式は、
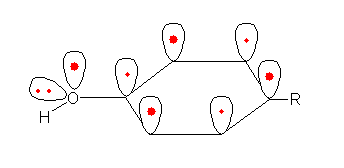
のように o- および p- 位における π 電子密度の増加を極限構造式で表現したものと考えればよい。ただし、上図において、p 軌道のローブはベンゼン環の面の上のみを示した。
従ってこの共鳴効果は m- 位に対してはほとんど効果がない。そればかりか、酸素原子は、窒素やハロゲンと同様に、炭素よりも電気陰性度の高い原子である。そのため、誘起効果(シグマ結合を通した電気陰性度の差に由来する分極)により、炭素上の電子密度が下がる傾向がある。上図のような共鳴効果がない m- 位では、この誘起効果の影響のみが見られるから、無置換の安息香酸よりも π 電子密度が下がり、結果として m- ヒドロキシ安息香酸の酸性度は上がることになる。 (発展)
上記解答例で述べた理屈は、「何故、ハロゲンが求電子置換反応に対して不活性気であるのに、m- ではなく、o-、p- 配向性を示すのか」の説明に通じる。
20.48, 41
逆合成の手法によって考えること。
(解答例)
いくつかの反応経路を図に示した。この経路において、鍵となるのは二重結合の導入と、カルボキシ基の導入である。
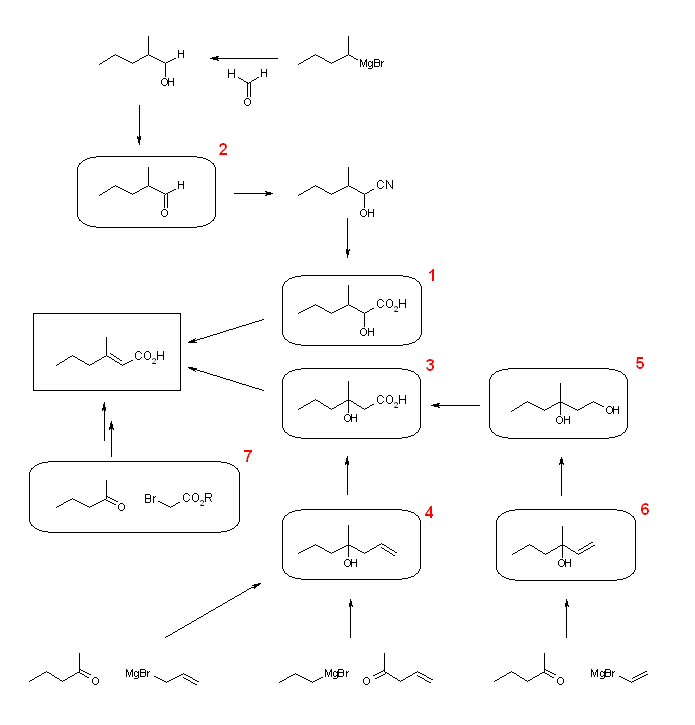
(考え方)
1) 条件として、炭素数5以下の原料を用いなければならないから、目的生成物を2つ(以上)のパーツから作ることを考えなければならない。その際に、すぐに目がいくのが二重結合である。この位置での切断を考えることにする。二重結合をつくる反応は、大きくわけて、Wittig タイプの反応、カルボニルに対する求核攻撃によって生じるアルコールの脱水、の2通りである。
2) Wittig タイプの反応の原料の一例を、上図7で示した。Wadsworth-Emmons-Horner 反応が適用できるであろう。RR'C=O + (EtO)2P(=O)CH2CO2Et, 反応条件は、NaH を塩基として加え、溶媒(MeOCH2CH2OMe など)中で還流。
3) 脱水による二重結合の生成を考える場合、上図1、3の2通りのアルコールが考えられる。3のアルコールから出発した場合でも、生じ得る可能性のある二重結合の位置異性体3種類のうちで、目的生成物の構造が一番安定であるから、反応の位置選択性については問題ない。(3-methyl-2-hexenoic acid は、二重結合が3置換になっているばかりか、カルボキシ基のカルボニルと共役しているため、3-methyl-3-hexenoic acid よりも安定である。)
4) ヒドロキシカルボン酸1は、アルデヒド2からのシアノヒドリン化と、その加水分解により生じることができる。ただし、アルデヒド2が、まだ炭素数で6なので、これを更に 2-bromopentane から生じた Grignard 試薬と formaldehyde の反応生成物を酸化して得るなどしなければならない。
5) 3のカルボキシ基は、(たとえエステル化などしても)Grignard 反応などにおいて共存させることができない。従って、ここでは、カルボキシ基を別の官能基から変換する経路を例として示している。ひとつは、1級アルコール5の酸化によりカルボキシ基とする方法(第3級のアルコールはこの条件では反応しない)、もうひとつは二重結合の酸化開裂によりカルボキシ基とする反応を示した。アルコール5は、アルケン6の位置選択的な水の付加(たとえば、ヒドロホウ素化反応を利用)により得ることができる。アルケン4や6はまだ炭素数が5より大きいので、水酸基の部分に注目し、適当なカルボニル化合物と有機金属試薬との反応で合成することができる。
6) 3を得るための他の方法として、反応性の低い有機金属試薬を用いることができる。その1つは Reformatsky 反応(α-ハロエステルと亜鉛から生成する亜鉛エノラートがアルデヒドやケトンに付加する反応)で、エステル基は反応しない。(同様に活性の下がった有機金属試薬として、19章では Gilman 試薬について学んだ。これは、ケトンなどとも反応せず、酸ハロゲン化物、共役エノンなど、限られた基質と反応する。)
20.49, 42
a) 位置選択性に注意せよ。
f) ヒドリド還元では、カルボニル基はメチレンまで還元できないことに注意する。
(解答例)
a) ヒドロホウ素化反応: BH3, THF then H2O2, -OH
b) PBr3
c) グリニヤルと二酸化炭素の反応:Mg, then CO2, and then H3O+
or シアノ基の加水分解:-CN, then H3O+
d) ヒドリド還元:esterification (ROH, H+), then LiAlH4, Et2O, then H3O+
or ボラン還元(教科書 p788):BH3, THF, then H3O+
e) PCC
f) Wolff-Kishner 反応(教科書 p738):N2H4, KOH, ROH
20.50, 43
NaOH 水溶液で処理した後、「酸性化する」とカルボン酸のナトリウム塩からカルボン酸が遊離する。すなわち、NaOH 水溶液によりカルボン酸(の塩)が生じる。これは、はじめに、OH- による求核反応がおき、引きつづく数段階の過程を含む。Favorskii 反応では炭素の数は増減していないから、転位反応で骨格の組み換えが起きている。出発物質と生成物の構造を比較して、どの部分が転位しているのかを見出すこと。
(解答例)
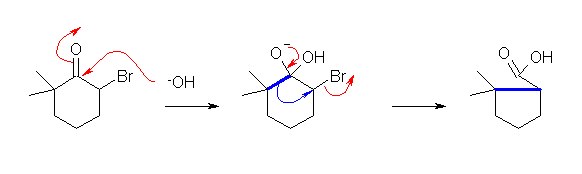
骨格の転位の部分を青で示した。この反応機構では明示していないが、アルカリ処理条件なので、生成物のカルボン酸は、中和により塩を生じている。これを酸で処理することにより、カルボン酸の形で単離できることになる。
20.51-20.59 (44-51)
(20.51-20.57 は、分光学の問題なので省略しました。)
20.58, 50
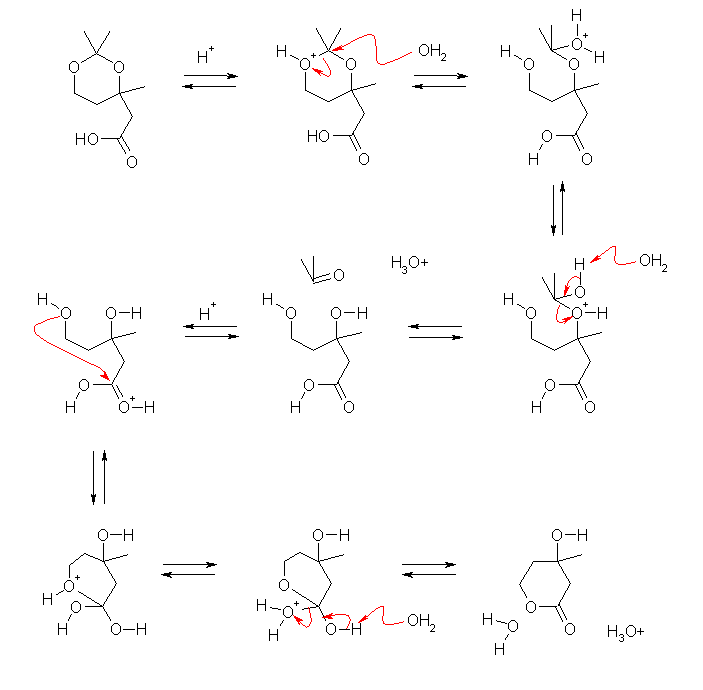
出発物質は、アセタール構造を有している。アセタールは酸性条件で水が過剰にあると、加水分解される。アセタールの生成/分解、およびエステルの形成/加水分解は、いずれも酸性条件下、平衡である。
(解答例)
(正しくない反応機構の例)
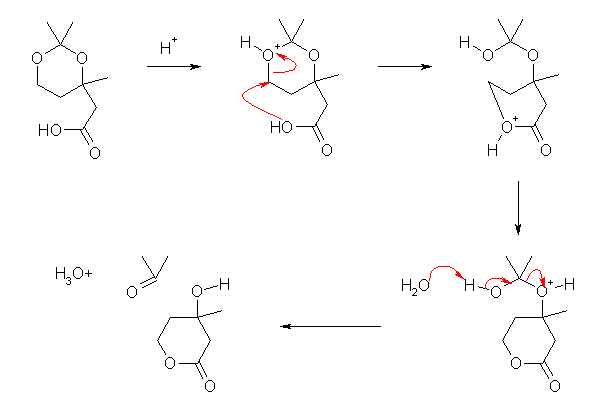
酸素がプロトン化(ルイス酸の配位)を受けると、正の形式電荷を持つため、その結合の根元の炭素は求核攻撃を受けやすくなる。アセタールの加水分解では、このように酸素へのプロトンの配位に引きつづいて、溶媒である水分子の求核攻撃が起こり、加水分解が進行した。ここでは、水よりも求核力は劣るものでも分子内反応であれば競争できると考え、カルボキシ基による分子内の求核攻撃により、エステル化と同時にアセタールの加水分解が進行する機構を考えた。
しかしながら、酸性条件でのエステル化反応の機構(図 21-10, p832)を参照すると、上記機構はおそらく正しくないことが予想できる。すなわち、酸性でエステルが生じる反応では、カルボキシ基の酸素が求核攻撃するのではなく、プロトン化を受けたカルボキシ基のカルボニルが求核攻撃を受けるのである。そのため、まずアセタールを加水分解し、生じる 3,5-dihydroxy-3-methylpentanoic acid から分子内のエステル化を起こすように考えてやればよい。
なお、3,5-dihydroxy-3-methylpentanoic acid の2つの水酸基のうち、分子内のエステルを生じるのは、より結合角歪みの少ない6員環を与えるところの5位の水酸基のみである。
20.59, 51
カルボキシ基の水酸基は、β カルボニル基に対して水素結合している。6員環になるようにこの水素結合を描いてみること。その上で、(ベンゼン環の共鳴のように)環状に電子を動かしてみること。
(解答例)
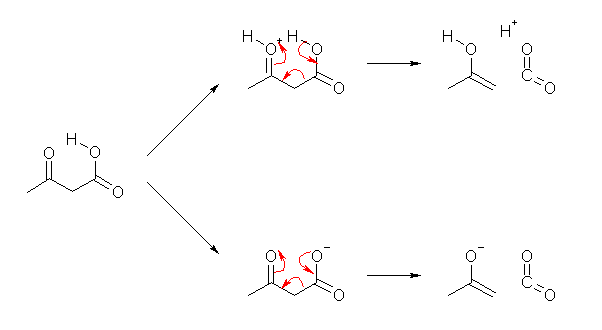
上段は酸触媒、下段は塩基触媒に対しての、β-ケトカルボン酸の脱炭酸の反応機構。いずれも、形式的に、二酸化炭素が気体として発生する。(二酸化炭素はアルカリ水溶液に炭酸イオンとして溶け込む。)